
题目列表(包括答案和解析)
1. 下列关于烃的说法中,正确的是( )
A.烃是指分子里含有碳、氢元素的化合物
B.烃是指分子里含有碳元素的化合物
C.烃是指燃烧反应后生成二氧化碳和水的有机物
D.烃是指仅由碳和氢两种元素组成的有机物
22.(8分)将7.8gNa2O2投入到100g10%的NaOH溶液中充分反应。求:
⑴所得溶液的质量分数
⑵向该溶液中通入一定量CO2,然后小心低温蒸干,所得固体冷却干燥,称重为28.5g,通过计算推出该固体物体的组成和质量
21.(6分) 一根铁棒100 g ,插入100 g 一定质量分数的CuSO 4 溶液中,充分反应后取出烘干后质量为100 . 6 g ,则:
⑴ 求被氧化的物质的质量? ⑵ 求原CuSO 4 溶液中溶质的质量分数?
20、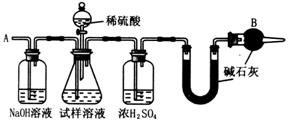 已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰(为CaO和NaOH的混合物)的U形管的质量,得到bg
④从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U形管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为dg
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明__________________。
(2)装置中干燥管B的作用是_____________________________________。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果_________(填“偏高”“偏低”或“不变”)。
(4)步骤⑤的目的是_____________________________。
(5)步骤⑦的目的是_____________________________。
(6)该试样中纯碱的质量分数的计算式为_______________________。
19.A、B、C、D、E五种物质的焰色都呈黄色,A、B与水反应都有气体放出,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,同时都生成溶液C,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能生成D.
⑴写出下列物质的化学式: B ,E 。
⑵写出A→C的化学方程式,并标出电子转移的方向和数目: 。
⑶写出C→D的离子方程式: 。
⑷写出化学方程式:E+B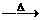 D+C+O2↑:
。
D+C+O2↑:
。
18.(1)写出下列物质溶于水后的电离方程式:
KHCO3 : Al2(SO4)3 :
(2)写出下列反应的化学方程式:
① 钠在空气中燃烧: ;
② 碳酸氢钠受热分解: ;
③ 过氧化钠与水反应: 。
17.(1)22克CO2的物质的量为 ,其中含有O原子约为 个;
(2)11.7 g NaX中含有0.2 mol Na+ ,NaX的摩尔质量是 。
16. 氧化钠与过氧化钠的共同之处是
A.均是淡黄色固体 B.均是碱性氧化物
C.均能与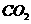 反应且放出
反应且放出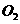 D.均能与水反应生成强碱
D.均能与水反应生成强碱
第 Ⅱ 卷(共52分)
14.在反应3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO ↑+ 8H2O中,1mol还原剂失去电子的物质的量为
A.6mol B. 8mol C.10mol D.12mol
5uo15.在由NaOH、Na2O2组成的混合物中钠元素的质量分数为58%,则混合物中氢元素的质量分数约是 A.62% B.55% C.40% D.2%
13.a mol H2O和a mol CO2一定相同的是
A. 所含电子数 B. 相同条件下的密度 C. 分子个数与原子个数 D. 质量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com