
5£Æ”≤÷¨À·∏ ”Õı•æ≠‘̪Ø∫Û,∑¥”¶µ√µΩµƒ”≤÷¨À·ƒ∆‘⁄ÀÆ¿Ô–Œ≥…µƒ∑÷…¢œµ Ù”⁄°°°°°°°°°°°°°° (°°°° )
°°°° A£Æ»Ð“∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£Æ◊«“∫°°°°°°°°°°°°°°°°°°°°
°°°° C£ÆΩ∫ð°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°° D£Æº”¬»ªØƒ∆∑€ƒ©∫Û∑÷Œ™¡Ω≤„,”≤÷¨À·ƒ∆‘⁄…œ≤„
4£Æ”√1- Æ∂˛¥º\±Ω\≈®¡ÚÀ·÷∆±∏∫¨”–12∏ˆÃº‘≠◊”µƒ∂‘ Æ∂˛ÕȪ˘±Ωª«À·,∑¥”¶Ãıº˛∫Õ¥þªØº¡»Œ—°,”√µΩµƒªØ—ß∑¥”¶¿ý–Õ∞¥◊≈œ»∫ÛÀ≥–Ú’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° ¢Ÿ»°¥˙∑¥”¶°°°°°°°°°°°°°° ¢⁄º”≥…∑¥”¶°°°°°°°°°°°° ¢€œ˚»•∑¥”¶°°°°°°°°°°°°°° ¢Ðªπ‘≠∑¥”¶
°°°°°° ¢ðº”æ€∑¥”¶°°°°°°°°°°°°°° ¢ÞÀıæ€∑¥”¶
°° A£Æ¢Ÿ¢€¢⁄°°°°°°°°°°°°°°°° B£Æ¢€¢⁄¢Ÿ°°°°°°°°°°°°°°°° C£Æ¢€¢ð¢Þ°°°°°°°°°°°°°° D£Æ¢€¢Ð¢⁄
3£Æœ¬¡–≤˙∆∑µƒ π”√≤ªª·∂‘ª∑æ≥‘Ï≥…Œ€»æµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°° °° A£Æ∫¨¡◊œ¥“¬∑€°° °° B£Ææ∆æ´°°°° °°°°°°°°°°°° C£Æ∑˙¿Ô∞∫°°°° °°°°°°°° D£Æ∫¨πصÁ≥ÿ
2£ÆƒÚÀÿ «µ⁄“ª∏ˆ»Àπ§∫œ≥…µƒ”–ª˙ŒÔ£¨œ¬¡–πÿ”⁄ƒÚÀÿµƒ– ˆ≤ª’˝»∑µƒ «°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£ÆƒÚÀÿ «“ª÷÷µ™∑ °°°°°°°°°°°° °°°°°°°°°°°° B£ÆƒÚÀÿ «»ÀÖ¬≥¬¥˙–ªµƒ“ª÷÷≤˙ŒÔ
C£ÆƒÚÀÿƒÐ∑¢…˙ÀÆΩ‚∑¥”¶°°°°°°°° °°°°°°°°°°°° D£ÆƒÚÀÿ «“ª÷÷À·–‘ŒÔ÷
1£Æ“‘œ¬Àµ∑®’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£Æƒ…√◊≤ƒ¡œ «÷∏“ª÷÷≥∆Œ™°∞ƒ…√◊°±µƒ–¬ŒÔ÷ ÷∆≥…µƒ≤ƒ¡œ
B£Æ¬Ã…´ ≥∆∑ «÷∏≤ª∫¨»Œ∫ŒªØ—ߌÔ÷ µƒ ≥∆∑
C£Æ…˙ŒÔπõ™ «÷∏÷≤ŒÔÕ®π˝“∂√Ê÷±Ω”Œ¸ ’ø’∆¯÷–µƒµ™∆¯
D£Æπ‚µºœÀŒ¨ «“‘∂˛—ıªØπËŒ™÷˜“™‘≠¡œ÷∆≥…µƒ
24£Æ(15∑÷)œ¬Õºº◊ «øŒ±æ÷–—È÷§Õ≠∫Õ≈®œıÀ·∑¥”¶µƒ◊∞÷√£¨““°¢±˚ « ¶…˙∂‘—ð æ µ—È∏ƒΩ¯∫Û
µƒ◊∞÷√£∫
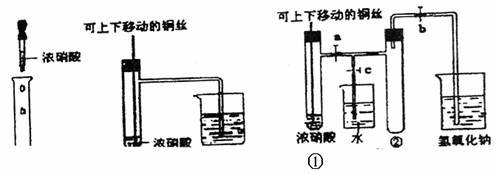
°° (1)(2∑÷)–¥≥ˆÕ≠∫Õ≈®œıÀ·∑¥”¶µƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°° (2)(4∑÷)∫Õº◊◊∞÷√œý±»£¨““◊∞÷√µƒ”≈µ„”–°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°° (3)(2∑÷)Œ™¡ÀΩ¯“ª≤Ω—È÷§NO2∫ÕÀƵƒ∑¥”¶£¨ƒ≥—ß…˙…˺∆¡À±˚◊∞÷√£¨◊ˆ µ—È ±œ»πÿ±’µØª…º–°°°°°°°° £¨‘Ÿ¥Úø™µØª…º–a∫Õ°°°°°°°° £¨≤≈ƒÐ πNO2∆¯ÃÂ≥‰¬˙¢⁄ ‘πа£
°° (4)(3∑÷)–¥≥ˆNO∫ÕNO2∞¥1£∫1ªÏ∫œ±ªNaOH»Ð“∫Œ¸ ’µƒªØ—ß∑Ω≥Ã Ω°°°°°°°°
°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°£
°° (5)(4∑÷)»Ù π◊∞÷√±˚µƒ¢⁄ ‘πÐ÷–µƒNO2∫ÕÀÆ≥‰∑÷∑¥”¶£¨‘ÚÀ˘µ√»Ð“∫ŒÔ÷ µƒ¡ø≈®∂»µƒ◊Ó¥Û÷µ «°°°°°°°°°°°°°°°° (∆¯ÃÂê˝∞¥±Í◊º◊¥øˆº∆À„)°£
23£Æ(14∑÷)ƒ™∂˚—Œ[(NH4)2SO4°§FeSO4°§6H2O]ø’∆¯÷–±»“ª∞„—«Ã˙—ŒŒ»∂®£¨ «ªØ—ß∑÷Œˆ÷–≥£”√µƒªπ‘≠º¡°£ƒ≥—–æø–‘—ßœ∞–°◊È”√œ¬ÕºÀ˘ 浃 µ—È◊∞÷√¿¥÷∆»°ƒ™∂˚—Œ£¨ µ—È≤Ω÷Ë»Áœ¬£∫
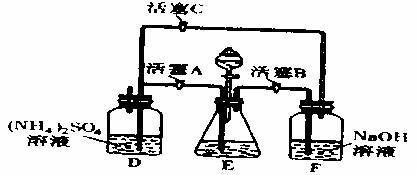
°°°° ¢Ÿ ”√30%µƒNaOH»Ð“∫∫Õ∑œÃ˙–ºªÏ∫œ°¢÷Û∑–°¢¿‰»¥°¢∑÷¿Î£¨Ω´∑÷¿Î≥ˆµƒNaOH»Ð“∫◊∞»ÎF÷–£ª
°°°°°° ¢⁄ ¢⁄‘⁄E÷–”√¢Ÿ¥¶¿Ìπ˝µƒÃ˙–º∫Õœ°H2SO4∑¥”¶÷∆»°FeSO4£ª
°°°°°° ¢€ Ω´¢⁄÷∆µ√µƒFeSO4»Ð“∫”Î(NH4)2SO4»Ð“∫ªÏ∫œ£¨Ω·æßµ√µΩƒ™∂˚—Œ°£
°°°° ‘ªÿ¥œ¬¡–Œ £∫
°° (1)(4∑÷)¿˚”√Ã˙–º∫Õœ°¡ÚÀ·∑¥”¶≤˙…˙µƒ«‚∆¯∏œ◊þ◊∞÷√÷–µƒ—ı∆¯º∞¡ÚÀ·Ô߻Г∫÷–»ÐΩ‚µƒ—ı£¨∆‰ƒøµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ªÃ˙–º∫Õœ°¡ÚÀ·∑¥”¶≤˙…˙µƒ«‚∆¯µƒ¡ÌÕ‚“ª∏ˆ◊˜”√ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°° (2)(4∑÷)»Á∫Œ…˺∆“ª∏ˆºÚµ•µƒ µ—È÷§√˜µ√µΩµƒ≤˙∆∑÷–”–Fe2+£ø
°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
°° (3)(4∑÷)Œ™¡À»∑∂®≤˙∆∑÷–—«Ã˙¿Î◊”µƒ∫¨¡ø£¨—–æø–°◊È”√µŒ∂®∑®¿¥≤‚∂®°£»Ù»°≤˙∆∑24.50g≈‰≥…100mL»Ð“∫£¨»°≥ˆ10mL”√0.10mol°§L-1KMnO4À·–‘»Ð“∫µŒ∂®£¨œ˚∫ƒKMnO4»Ð“∫10.00mL°£
°°°°°°°° ¢Ÿ(2∑÷) ‘≈‰∆Ω∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫
°°°°°°°° °°°°°°MnO-4+°°°°°° Fe2++°°°° H+ == °°°°°°Fe3++°°°° Mn2+ + °°°°°°H2O
°°°°°°°° ¢⁄(4∑÷)«Û≤˙∆∑÷–ƒ™∂˚—Œµƒ÷ ¡ø∑÷ ˝°°°°°°°°°° °£(ƒ™∂˚—Œµƒœý∂‘∑÷◊”÷ ¡øŒ™392)°£
22£Æ(16∑÷)µÁΩ‚‘≠¿Ì‘⁄ªØ—ß𧓵÷–”–π„∑∫”¶”√°£œ¬Õº±Ì 擪∏ˆµÁΩ‚≥ÿ£¨◊∞”–µÁΩ‚“∫a£∫X°¢
Y «¡ΩøȵÁº´∞£¨Õ®π˝µºœþ”Î÷±¡˜µÁ‘¥œý¡¨°£«Îªÿ¥“‘œ¬Œ £∫
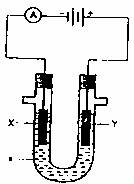
°° (1)»ÙX°¢Y∂º «∂Ë–‘µÁº´£¨a «±•∫ÕNaCl»Ð“∫£¨ µ—Èø™ º ±£¨Õ¨ ±‘⁄¡Ω±þ∏˜µŒ»Îº∏µŒ∑”Ù ‘“∫£¨‘Ú
°°°°°°°° ¢Ÿ(4∑÷)µÁΩ‚≥ÿ÷–Xº´…œµƒµÁº´∑¥”¶ ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°°°° °£
‘⁄Xº´∏ΩΩ¸π€≤ÏµΩµƒœ÷œÛ «°°°°°°°°°°°°°° °£
¢⁄(4∑÷)YµÁº´…œµƒµÁº´∑¥”¶ ΩŒ™ °°°°£¨ºÏ—È∏√µÁº´∑¥”¶≤˙ŒÔµƒ∑Ω∑® «°°°°°° °£
°° (2)»Á”√µÁΩ‚∑Ω∑®æ´¡∂¥÷Õ≠£¨µÁΩ‚“∫a—°”√CuSO4»Ð“∫£¨‘Ú
¢Ÿ(4∑÷)XµÁº´µƒ≤ƒ¡œ «°°°°°°°°°°°°°° £¨µÁº´∑¥”¶ ΩŒ™°°°°°°°°°°°°°°°° °£
¢⁄(4∑÷)YµÁº´µƒ≤ƒ¡œ «°°°°°°°°°°°° £¨µÁº´∑¥”¶ ΩŒ™ °°°°°°°°°°°°°°°°°£(Àµ√˜£∫‘”÷ ∑¢…˙µƒµÁº´∑¥”¶≤ª±ÿ–¥≥ˆ)
21£Æ(15∑÷)ŒÔ÷ µƒ◊™ªØπÿœµ»Áœ¬ÕºÀ˘ æ(”–µƒ∑¥”¶ø…ƒÐ‘⁄ÀƻГ∫÷–Ω¯––)°£∆‰÷–AŒ™ªØ∫œŒÔ£¨º◊ø…”…¡Ω÷÷µ•÷ ÷±Ω”ªØ∫œµ√µΩ£¨““Œ™Ω Ùµ•÷ £¨GŒ™À·£¨““‘⁄Gµƒ≈®»Ð“∫÷–∑¢…˙∂€ªØ°£
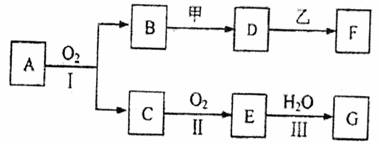
°° (1)»ÙAŒ™¡ÚÀ·π§“µµƒ÷ÿ“™‘≠¡œ£¨CƒÐ π∆∑∫Ï ‘“∫Õ …´£¨DµƒÀƻГ∫÷–º”»ÎHNO3À·ªØµƒAgNO3»Ð“∫”–∞◊…´≥¡µÌ…˙≥…°£‘Ú
°°°° °°°°¢Ÿ(4∑÷)𧓵…œ∑¥”¶II‘⁄°°°°°°°°°° ÷–Ω¯––(ÃӅ˱∏√˚≥∆)£¨π§“µ…œ∑¥”¶III”√”⁄Œ¸ ’Eµƒ ‘º¡ «°°°°°°°°°°°°°°°°°°°°°° °£
¢⁄(2∑÷)DµƒÀƻГ∫≥ °°°°°° –‘(ÃÓ°∞À·°±°¢°∞ºÓ°±ªÚ°∞÷–°±)
¢€(2∑÷)∑¥”¶IµƒªØ—ß∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°° °£
°° (2)»Ùº◊Œ™µ≠ª∆…´πÃã¨D°¢Fµƒ»Ð“∫æ˘≥ ºÓ–‘£¨”√¡Ω∏˘≤£¡ß∞Ù∑÷±’∫»°A°¢Gµƒ≈®»Ð“∫£¨≤¢ πÀ¸√«Ω”Ω¸£¨”–¥Û¡ø∞◊—Ã…˙≥…°£‘Ú
°°°°°°°° ¢Ÿ(2∑÷)º◊µƒµÁ◊” Ω «°°°°°°°°°°°°°°°°°°°°°°°° °°°£
°°°°°°°° ¢⁄(2∑÷)–¥≥ˆB∫Õº◊∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «°°°°°°°°°°°°°°°° °£
°°°°°°°° ¢€(3∑÷)»Ù17gA”ÎO2∑¥”¶…˙≥…∆¯Ã¨µƒB∫ÕC ±∑≈≥ˆ226.7kJ»»¡ø£¨–¥≥ˆ∏√∑¥”¶µƒ»»ªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
20£Æ∞—–ø∆¨∫ÕÃ˙∆¨∑≈‘⁄”–œ° ≥—ŒÀƵƒ∑”ٻГ∫µƒ±Ì√Ê√Û÷–£¨»Áœ¬ÕºÀ˘ ææ≠π˝“ª∂Œ ±º‰∫Û£¨◊Óœ»π€≤ÏµΩ±‰∫ϵƒ«¯”Ú «°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°(°°°° )
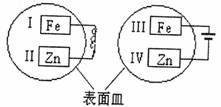
°°°°°° A£ÆI∫ÕIII°°°°°°°°°°°°°°°° B£ÆI∫ÕIV
°°°°°° C£ÆII∫ÕIII°°°°°°°°°°°°°° D£ÆII∫ÕIV
µ⁄¢ÚæÌ
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com