
9.常温下,c(H+)=0.1mol·L-1的无色透明溶液中,下列各组离子一定能大量共存的是( )
A.NH+4、Mg2+、SO42-、C1- B.Mg2+、I-、NO3-、SO42-
C.K+、MnO4-、SO42-、C1- D.Na+、K+、NO3-、CO32-
8. 如图,利用培养皿探究氧气的性质。实验时向NaOH固体上滴几滴浓氧水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是 ( )
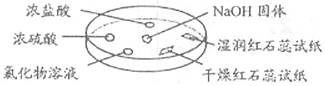
|
选项 |
实验现象 |
解释 |
|
A |
浓盐酸附近产生白烟 |
NH3与浓盐酸反应产生了NH4C1固体 |
|
B |
浓硫酸附近无明显现象 |
NH3与浓硫酸不发生反应 |
|
C |
氯化物溶液变浑浊 |
该溶液一定是A1C13溶液 |
|
D |
干燥红石蕊试纸不变色,湿润红石蕊试纸变蓝 |
NH3是一种可溶性碱 |
7. 2008年9月25日21时10分。“神舟”顺利升空。飞船的太阳能电池板有“飞船血液”之称,它可将太阳能直接转化为电能,我国在砷化镓太阳能电池研究方面国际领先。砷(As)和镓(Ca)都是第四周期元素,分别属于VA和IIIA族。下列有关说法正确的是 ( )
A.As的非金属性强于P B.AsH3的沸点低于PH3
C.Ca的原子序数比Ca大1 D.太阳能电池不属于原电池
6.下列实验方法合理的是 ( )
A.用乙醇将碘水中的碘提取出来
B.用渗析的方法精制Fe(OH)3胶体
C.用石灰水鉴别Na2CO3、NaHCO3两种溶液
D.用加浓溴水并过滤的方法除去苯中混有的苯酚
5.针对能源、环境、水资源等方面的危机,以下四条设想合理可行的是 ( )
A.大量开采地下水,以满足社会对水的需求
B.生活中严禁使用塑料制品,以解决“白色污染”问题
C.面对金属矿物储量有限不能再生的危机,努力寻找金属的代用品
D.工业上禁止开发和使用化石燃料,以应对全球能源危机
29.(16分)已知A、B均为无色液体,具有芳香气味,在工业上常用做香精,可发生如下图所示的转化。其中A、B、C、E、G均为芳香族化合物,D的分子式为C2H4O2,E的分子式为C7H6O2。
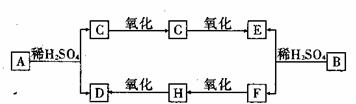
请根据图示回答下列问题:
(1)D的结构简式为 ,E的结构简式为 ;
(2)A与B的相互关系属于(填编号) ;
①同系物 ②同分异构体 ③同一种物质 ④同一类物质
(3)写出下列转化的化学方程式:H→D: ;B→E+F= ;
(4)符合下列3个条件的A的同分异构体的数目有 个。
i)含有苯环结构;ii)苯环上的一氯代物有两种;iii)能与NaHCO3发生反应放出CO2。写出其中任意一个同分异构体的结构简式 。
28.(15分)实验室有一瓶亚硫酸钠固体,已部分被氧化变质。下面是某实验小组通过实验确定其纯度的实验,请你一起来完成该实验的有关问题:
(1)该实验有以下实验步骤,其正确的操作顺序应为(用编号排序) ;
①称取样品W1g ②加盐酸酸化 ③用蒸馏水溶解 ④过滤
⑤加入过量氯化钡溶液 ⑥洗涤 ⑦干燥 ⑧称量沉淀质量为W2g
(2)加盐酸酸化的目的是 ;
(3)氯化钡溶液为什么要过量 ;
(4)如何检验沉淀已洗涤干净? ;
(5)根据题中已知条件,样品中Na2SO3纯度可表示为 ;
(6)该实验设计中,若将操作“②加盐酸酸化”改为“加硝酸酸化”,将会导致最终所得样品中Na2SO3纯度的测量结果 ;(填“偏大”、“偏小”或“无影响”)。
26.(11分)已知X、Y、Z、W都是短周期的非金属元素,其原子序数依次增大。W原子的质子数是Y原子质子数的两倍,X原子与W原子的最外层电子数之和是Y和Z原子的质子数之和的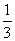 。Y的氢化物分子中有三个共价键。
。Y的氢化物分子中有三个共价键。
(1)X、Z的元素名称分别是 、 ,W元素原子结构示意图为 。
(2)Y的氢化物分子的空间构型为 ,属于 分子(填“极性”或“非极性”)
(3)由以上任意三种元素组成的化合物中,其水溶液显酸性的有(填写化学式) 、
。(任写两种)
(4)写出一个离子反应方程式,要求反应物与生成物的离子或分子均是由以上元素中的两种元素组成且各微粒所含的电子数相同。 。
(5)我国材料学家已成功制备了W元素与Y元素组成的耐高温的新型材料W3Y4。工业上可用W的氢化物与Y的氢化物反应制得耐高温化合物和氢气,此反应的化学方程式为 。
|
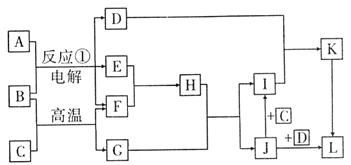
请根据图示回答下列问题:
(1)工业上利用反应①生产出的主要产品为 ;
(2)B+C→F+G对应的化学方程式为 ,该反应属于(填反应类型) ;
(3)在溶液中,K转化为L时,可以观察到的现象为 ;对应的化学方程式为
;
(4)图中H+G-I+J的转化在溶液中发生时,对应的离子方程式为 。
(5)若将J的溶液蒸干、灼烧,最终可得到的固体是 ;原因是(用离子方程式和简要文字说明) 。
13.常浊下,0.1mol·L-1某一元酸(HA)溶液中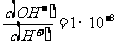 ,下列叙述正确的是( )
,下列叙述正确的是( )
A.该溶液中水电离出的c(H+)=1×10-10mol·L-1
B.该溶液中c(H+)+c(A-)+c(HA)=0.1 mol·L-1
C.该溶液与0.05 mol·L-1NaOH溶液等体积混合后:c(A-)>c(Na+)>c(OH-)>c(H+)
D.向该溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大
12.某有机物的结构简式为: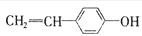 ,它可能具有的性质是 ( )
,它可能具有的性质是 ( )
①能使用KMnO4酸性溶液褪色
②遇FeCI3溶液显紫色
③能发生聚合反应
④能够跟1mol该化合物起反应的H2的最大用量是4mol
⑤能够跟1mol该化合物起反应的Br2的最大用量是2mol
A.只有①② B.只有②③
C.只有①②③④ D.①②③④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com