
19.有机物M的结构简式为: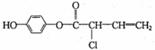 ,下列有关M的叙述正确的是( )
,下列有关M的叙述正确的是( )
A.可与H2反应,1mol M最多消耗5molH2
B.可与浓溴水反应,1molM最多消耗4mol Br2
C.可与NaOH溶液反应,1molM最多消耗4mol NaOH
D.常温下,M在水中的溶解度大于苯酚在水中的溶解度
18.常温下,0.1mol·L-1某一元酸(HA)溶液中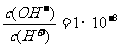 ,下列叙述正确的是
,下列叙述正确的是
( )
A.该溶液中由水电离出的c(H+)=10-3mol·L-1
B.该溶液中c(H+)+c(A-)=0.1mol·L-1
C.该溶液中与0.05mol·L-1NaOH溶液等体积混合后所得溶液中
c(A-)+2c(OH-)=c(HA)+2c(H+)
D.向该溶液中加入一定量的水,溶液中离子的浓度均减小
17.下列实验操作中,正确的是 ( )
A.称取16.25gFeCl3,用100mL蒸馏水溶解,配制1.0mol/L FeCl3溶液
B.为测定硫酸铜晶体中结晶水含量,称样时,先称取一定量的晶体,后放入坩埚
C.为检验酸性溶液中的Cl-和SO2-4,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液
D.向乙酸乙酯中加入饱和Na2CO3溶液,振荡,分液,除去乙酸乙酯中的少量乙酸
16.在一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+ B(g)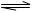 xC(g)+ 2D(g)。2 min末该反应达到平衡,生成0.8mol
D,并测得C的浓度为0.2 mol·L-1。下列判断错误的是 ( )
xC(g)+ 2D(g)。2 min末该反应达到平衡,生成0.8mol
D,并测得C的浓度为0.2 mol·L-1。下列判断错误的是 ( )
A.x=1
B.2min内A的反应速率为0.3mol·(L·min)-1
C.B的转化率为40%
D.若混合气体的密度不变,则表明该反应已达到平衡状态
15.常温下,取物质的量浓度相同的NaOH和HCl溶液,以3:2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为 ( )
A.0.01mol/L B.0.017mol/L C.0.05mol/L D.0.50mol/L
14.向一定量Fe、FeO、Fe2O3的混合物中加入120mL 4mol·L-1的稀硝酸恰好使混合物完全溶解,放出1.344L(标准状况)气体,往所得溶液中加入KSCN溶液,无血红色出现,若用足量的氢气在加热条件下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.14mol B.0.16mool C.0.21mol D.0.24mol
13.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:
Cd +2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
( )
A.充电时阳极反应:Ni(OH)2-e- + OH- == NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
12.关于如图装置的叙述中,正确的是 ( )
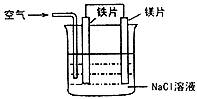
A.镁片为负极,镁片上产生黄绿色气体 B.铁片为阳极,铁片上产生无色气体
C.溶液中铁片与镁片之间产生白色沉淀 D.溶液中Na+向镁片方向定向移动
11.下表为元素周期中短周期的一部分。下列有关A、B、C、D、E五种元素的叙述中,不正确的是 ( )
|
|
|
|||
|
A |
|
B |
C |
|
|
|
|
D |
E |
|
A.D在过量的B中燃烧的主要产物为DB3
B.C的氢化物的沸点比E的氢化物的沸点高
C.A与B形成的阴离子可能有AB2-3、A2B2-4
D.由这五种元素中的几种形成的只含极性键的非极性分子不少于4种
10.已知中学化学中常见反应形式为:A+B→C+D+H2O,对于该反应的下列叙述不正确的是 ( )
A.该反应可能是氧化还原反应 B.该反应可能是非氧化还原反应
C.C和D有一种一定是盐 D.A和B不一定是酸或碱
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com