
28.(12分)氮元素是生命活动、物质间转化的常见元素。
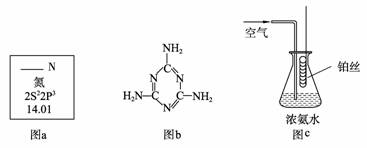
(1)图a是元素周期表中N元素的有关信息,图a中横线上缺失的信息是 。
15N是N元素的一种重要核素,其一个原子核中含有的中子数为 。
(2)“三鹿”奶粉中含有超标的三聚氰胺引起了人们对食品安全的极大关注。三聚氰胺的结构简式如上图b,根据你的了解,下列关于三聚氰胺的表述中,正确的是
(填字母序号)。
a.属于蛋白质b.是氨基酸c.是食品添加剂d.和氨基酸含有相同种类的原子团
e.属于高分子化合物
(3)如上图c装置,将灼热的铂丝伸入锥形瓶中,同时通过导管鼓入空气,发现在锥形瓶口有少量的红棕色气体生成。写出导致该现象的主要化学方程式: 、
。
(4)金属与不同浓度的硝酸反应时,往往生成多种不同价态的还原产物。图d是各种不同密度的硝酸与铁反应时(相同温度)还原产物的分布图。
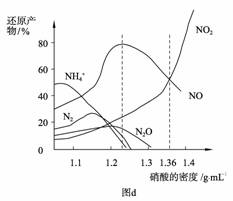
① 某硝酸试剂瓶的标签注明:密度1.26 g·mL-1,质量分数 50.0%;若取该试剂10 mL配成1000 mL溶液,所得溶液的pH= 。
② 当硝酸溶液的密度为1.36 g·mL-1时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是 (填序号)
a.2Fe+10HNO3==2Fe(NO3)3+NO↑+3NO2↑+5H2O
b.4Fe+18HNO3==4Fe(NO3)3+3NO↑+3NO2↑+9H2O
c.2Fe+6HNO3=2Fe(NO3)2+NO↑+NO2↑+3H2O
2.第Ⅱ卷所有题目的答案考生须用黑色0.5 mm的墨水签字笔答在答题纸上,在试题卷上答题无效。
[必做部分]
15.几种短周期元素的原子半径和主要化合价见下表,下列有关说法中,正确的是( )
|
元素代号 |
X |
Y |
Z |
L |
M |
Q |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.099 |
0.077 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+7、-1 |
+4、-4 |
-2 |
A.等物质的量的X、Y的单质与足量盐酸反应,生成H2一样多
B.Y与Q形成的化合物不可能跟氢氧化钠溶液反应
C.Z的氢化物的稳定性强于L的氢化物的稳定性
D.在化学反应中,M原子与其它原子易形成共价键而不易形成离子键
第Ⅱ卷(必做120分+选做32分,共152分)
做题中选择2个物理、1个化学和1个生物题作答。不按规定选做者,阅卷时将根据所选科目题号的先后顺序只判前面的2个物理题、1个化学题和1个生物题,其他作答的题目答案无效。
14.下列说法中,正确的是 ( )
A.0.1 mol·L-1的醋酸溶液加水稀释,c(H+)、c(OH-)同比例减小
B.体积相同、pH相同的NH4Cl溶液、盐酸,完全溶解少量且等同的锌粉,前者用时少
C.若常温下H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1 ,
则H+(aq)+NH3·H2O(aq)=NH4(aq)+H2O(l)ΔH=-57.3 kJ·mol-1
D.少量NaHSO4溶液与足量Ba(OH)2溶液反应离子方程式为:
2H++SO2-4+Ba2++2OH-=BaSO4↓+2H2O
13.下图为一原电池的结构示意图,下列说法中,不正确的是( )
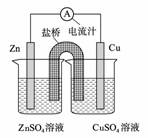
A.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu,该反应一定为放热反应
B.原电池工作时,Zn电极流出电子,发生氧化反应
C.原电池工作时,铜电极上发生氧化反应,CuSO4溶液蓝色变深
D.如果将Cu电极改为Fe电极,Zn电极依然作负极
12.若NA代表阿伏加德罗常数,则下列说法中,正确的是 ( )
A.22.4 LHBr气体中,含有NA对共用电子
B.在SiO2+2C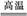 Si+2CO↑的反应中,每当有1 mol气体生成,就有4NA个电子转移
Si+2CO↑的反应中,每当有1 mol气体生成,就有4NA个电子转移
C.在1 L明矾[KAl(SO4)2·12H2O]溶液中,若n(Al3+)=0.2 NA时,则
c(SO2-4)>0.4 mol·L-1
D.分别处于第二、三周期的两种元素的原子各1 mol,其最外层电子数最多相差8 NA
11.下列有关结论中,正确的是 ( )
A.浓度为0.1 mol·L-1CuSO4溶液,温度升高,溶液的pH降低
B.一元酸与一元碱恰好完全反应后的溶液中一定存在c(H+)=c(OH-)
C.浓度相同的AlCl3、NH3·H2O、Ba(OH)2三物质的溶液,等体积混合时没有沉淀生成
D.在所有能够溶解Al(OH)3的溶液中,Cu2+、ClO-、Cl-、Ca2+一定能够大量共存
10.以下说法中,不正确的是 ( )
A.石油的分馏主要是物理变化而煤的干馏主要是化学变化
B.CH2==CH-COOCH3既能够使Br2的四氯化碳溶液退色,也可使酸性KMnO4溶液褪色
C.淀粉、纤维素的化学式都可表示为(C6H10O5)n,二者互为同分异构体
D.生活中食用的食醋、植物油、动物蛋白等物质是混合物
9.下列说法中,符合科学事实的是 ( )
A.在海水中,所含有的元素多数以游离态存在
B.混浊的黄河水是溶液、浊液、胶体共存的分散系
C.生产生活中排放的SO2、NO2等,是导致温室效应的主要物质
D.目前所认识和应用的高分子化合物全部是人工制得的有机高分子
23.(10分)A、B、C、D、E 5种元素,A元素所处的周期数、主族序数、原子序数均相等;B是地壳中含量最多的元素;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.E的单质既能与强酸反应,又能与强碱反应放出氢气
(1)B在周期表中的位置第 周期,第 族;
(2)C的最高价氧化物的化学式: ;
(3)D的最高价氧化物的水化物与E单质反应的化学方程式:
。
(4)这五种元素形成的盐的化学式: ,含有化学键 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com