
5.下列化学实验事实及其解释都正确的是
A.升高温度化学反应速率加快,是因为单位体积内活化分子百分数增加
B.将SO2通入BaCl2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸
C.鸡蛋清溶液中加入饱和CuSO4溶液析出沉淀,说明蛋白质发生了盐析
D.滴有酚酞的Na2CO3溶液中滴加BaCl2溶液后红色变浅,说明BaCl2溶液有酸性
4.下表所列各组物质中,物质之间通过一步反应不能实现如下图所示转化的是
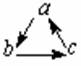
|
选项 |
a |
b |
c |
|
A |
Fe |
FeCl3 |
FeCl2 |
|
B |
Al(OH)3 |
NaAlO2 |
Al2O3 |
|
C |
HNO3 |
NO |
NO2 |
|
D |
CH2=CH2 |
CH3CH2Br |
CH3CH2OH |
3.设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.标准状况下,11.2 L乙醇完全燃烧生成CO2分子数为NA
B.pH=13的氢氧化钠溶液中所含Na+数为0.1NA
C.14 g乙烯和丙烯的混合气体中所含原子总数为3NA
D.5.6 g铁与足量的氯气反应失去电子数为 0.2NA
2.生产、生活中的有些现象看上去很相近,但原理相差甚远。下列现象中产生原理相同的是
A.在两只烧杯中分别放置干冰和浓硝酸,都有白雾产生
B.碘和锌在少量水作用下剧烈反应,钠在氯气中燃烧,都有烟产生
C.铁酸钾(K2FeO4)和氯化亚铁与氯水的混合物,都可用于自来水消毒及净化
D.在空气中亚硫酸钠与偏铝酸钠都会变质
1.石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如下),可由石墨剥离而成,具有极好的应用前景。下列说法正确的是
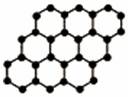
A.石墨烯与石墨互为同位素
B.0.12g石墨烯中含有6.02×1022个碳原子
C.石墨烯是一种有机物
D.石墨烯中的碳原子间以共价键结合
32.(6分)在一个容积为500 mL的密闭容器中,充入5 mol H2和2 mol CO。在一定温度和一定压强下,发生如下反应:2H2(g) + CO(g)  CH3OH(g),经过5 min后达到平衡状态。若此时测得CH3OH蒸汽的浓度为2 mol/L,求:
CH3OH(g),经过5 min后达到平衡状态。若此时测得CH3OH蒸汽的浓度为2 mol/L,求:
(1)以H2的浓度变化表示该反应的速率;
(2)达平衡时CO的转化率;
(3)平衡混合气体的密度与相同状况下的氢气密度之比。
31.(6分)已知CH4的燃烧热为890 kJ/mol,现有CH4和CO的混合气体共0.75 mol,完全燃烧后,生成CO2气体和18 g液态H2O,并放出515 kJ热量,请写出CO燃烧的热化学方程式(要求写出求算过程)。
30.(6分)室温下,向盛有2 mL 0.05 mol/L FeCl3溶液的试管中加入2 mL 0.01 mol/L KSCN溶液。
(1)上述反应的离子方程式为 ;
(2)再向该试管中滴入数滴0.01 mol/L NaOH溶液,可以观察到的实验现象是____________________,出现该现象的原因是_____________________________;
(3)你认为本实验还需要进一步完善之处为_______________________________
_____________________________________________________________。
29.(8分)将1 mol I2(g)和2 mol H2置于2 L密闭容器中,在一定温度下发生反应: I2(g) + H2(g)
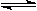 2HI(g),△H<0,并达平衡。HI的体积分数ω(HI)随时间变化如图曲线(Ⅱ)所示:
2HI(g),△H<0,并达平衡。HI的体积分数ω(HI)随时间变化如图曲线(Ⅱ)所示:
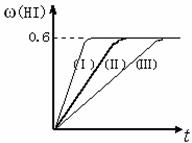
(1)达平衡时,I2(g)的物质的量浓度为 。
(2)若改变反应条件,在甲条件下ω(HI)的变化如曲线
(Ⅰ)所示,在乙条件下ω(HI)的变化如曲线(Ⅲ)所示,则甲条件可能是 ,乙条件可能是 。(填入下列条件的序号)
①恒容条件下,升高温度; ②恒容条件下,降低温度;
③恒温条件下,缩小反应容器体积;④恒温条件下,扩大反应容器体积;
⑤恒温恒容条件下,加入适当催化剂。
(3)若保持温度不变,在另一个相同的2 L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.6,则a、b、c的关系是 。
28.(8分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g) + H2(g)
 CO(g) + H2O(g),
CO(g) + H2O(g),
其化学平衡常数K和温度t的关系如下表:
|
t/℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是 。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2) = c(CO)·c(H2O),试判断此时的温度为 ℃。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com