
3.已知两个向量 ,若
,若 ∥
∥ ,则
,则 的值是 ( )
的值是 ( )
A.1 B.2 C. D.
D.
2.已知集合 ,则
,则 ( )
( )
A. B.
B. C.
C. D.
D.
1.若i是虚数单位,则 ( )
( )
A.i B.-1 C.1 D.-i
25.(10分)黄铜(由锌和铜形成的合金)有较强的耐磨性能,在生活中有广泛的用途。晓军同学为了测定黄铜屑样品组成,分四次取样品与稀硫酸反应,其实验数据记录如下表:
|
|
1 |
2 |
3 |
4 |
|
样品质量/g |
25.0 |
25.0 |
25.0 |
30.0 |
|
稀硫酸质量/g |
80 |
100 |
120 |
100 |
|
产生气体质量/g |
0.4 |
0.5 |
0.5 |
0.5 |
计算:
(1)第 次实验样品与稀硫酸恰好完全反应。
(2)黄铜样品中铜的质量分数是 。
(3)所用稀硫酸中溶质质量分数,写出计算过程。
 2010年中考模拟考试试题
2010年中考模拟考试试题
24.(7分)儿童缺锌会引起食欲不振、发育不良。右图为某种
补锌口服液说明书的一部分,请回答:
(1)该口服液中的锌属于 (填:“常量”或“微量”)元素;
葡萄糖酸锌分子中的碳、氢元素的质量比为 。
(2)每支口服液中锌的质量分数为 (1g=1000mg)。
(3)若儿童1kg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半;体重为20kg的儿童每天还须服该口服液 支,才能满足身体的需要.
23.(13分)化学实验小组的同学将一定量的Ca(OH)2溶液与Na2CO3溶液混合,充分反应后过滤,得到无色滤液,他们对滤液的成分进行探究。
[提出问题]滤液里可能含有哪些溶质呢?
(1)[猜想与假设]
甲同学猜想可能含有NaOH和Ca(OH)2;乙同学猜想可能含有NaOH、Na2CO3和Ca(OH)2
丙同学猜想可能恰好完全反应只含 ;
丁同学猜想可能含有 。
(2)[实验验证]请你对甲同学的猜想,设计一个简单的实验加以证明。
|
实验步骤 |
实验现象 |
实验结论 |
|
|
|
甲同学的猜想成立 |
(3)[反思与评价]
你认为乙同学的猜想合理吗?请分析原因是 。
4)[物质鉴别]化学小组同学选用了两种不同类别的试剂进行实验,鉴别丁同学猜想,并得出结论--Na2CO3存在。请将鉴别的化学方程式填在下表中。
|
|
化 学 方 程 式 |
|
试剂1 |
|
|
试剂2 |
|
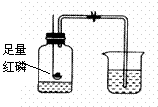
22. (14分)下列A ~ F是初中化学中的六个实验,请按要求填空:
(14分)下列A ~ F是初中化学中的六个实验,请按要求填空:
 |
|||||||||||||
 |
|||||||||||||
|
|||||||||||||
 |
|||||||||||||
 |
|||||||||||||
 |
|||||||||||||
|
|||||||||||||
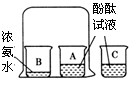
(1)A实验中盛放稀盐酸的仪器名称是 ,F实验中搅拌的目的是 。
(2)B实验中红磷燃烧的化学方程式为 ,实验说明氧气的体积约占空气的 ,实验成功的关键是 (填序号)。
①装置气密性好; ②实验前夹紧止水夹; ③红磷过量或足量;
④冷却后再打开止水夹; ⑤要选用教室内的空气。
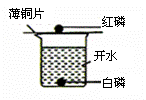
(3)E实验的全过程观察到的现象是
;发生反应化学方程式为
。
(4)上述实验中能达到实验目的且正确的是 (填字母)。
21.(9分)今年,我国部分地区普降大雪,给人们出行带来诸多不便,生产生活受到很大影响,损失十分严重。在道路除雪过程中,融雪剂发挥了很大的作用。已知某公司生产的融雪剂由NaCl 、NaNO3 、MgCl2、、CuSO4中的两种物质组成。小明为探究其成分,设计并完成了如下图所示的实验。

根据以上实验,请你推断:
(1)该融雪剂一定没有的成分是 。
(2)该融雪剂中的组成可能为:(Ⅰ) ;(Ⅱ) 。
(3)写出融雪剂溶于水后与氢氧化钠溶液反应的化学方程式 。
20.(9分)我国科学家侯德榜创造了一种著名的纯碱生产方法-“联合制碱法”。请你回答:
(1)纯碱(Na2CO3)属于 类物质(填“酸”、“碱”或“盐”)。向纯碱的水溶液中滴入酚酞试液,试液变 色,其pH 7(填“=”、“<”或“>”)。
(2)“联合制碱法”生产过程用化学方程式可简要表示为:
① NH3+CO2+H2O=NH4HCO3
② NH4HCO3+NaCl=NaHCO3↓+NH4Cl
 ③ 2NaHCO3 Na2CO3+H2O+CO2↑
③ 2NaHCO3 Na2CO3+H2O+CO2↑
该过程中没有涉及到的基本反应类型是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(3)第②步中加入的是磨细食盐粉。食盐磨细的目的是:
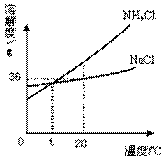
(4)将第②步所得滤液(NH4Cl与剩余NaCl的混合溶液)降
温,NH4Cl晶体大量析出,而NaCl却仍留在了溶液中。
(参考如右图)
你认为NH4Cl先结晶的原因可能是什么:
所得NH4Cl属于化学肥料中的 肥。
19.(6分)雨水资源化是一种发展趋势,2008年奥运会所使用的奥运场馆都建立了雨水利用系统,大大提高了雨水利用率。
(1)雨水在降落过程中常受NO2、SO2的污染形成酸雨。若要测定某雨水酸度,可使用
(2)雨水受到SO2污染时,将发生SO2与水的反应,写出该反应的化学方程式: ;空气中的SO2主要来源于 ;
(3)收集的地面雨水常携带树叶、塑料袋等不溶杂物,处理雨水时应进行沉降、 ;
(4)要使主要受SO2污染的酸雨可被回收利用,必须对其酸性进行中和,你认为以下较为 经济有效的方法是加入适量的 固体(填序号)。
A.NaOH B.Ca(OH)2 C.CaCl2 D.Na2CO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com