
31.(13分)已知有机物A、B、C、D、E有如下图所示转化关系:
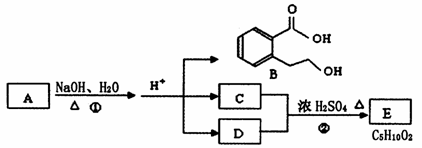
其中C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合
物。根据上图回答问题:
(1)B分子中的含氧官能团名称是_________________________;
写出一个同时符合下列四个条件的B的同分异构体的结构简式______________。
a.含苯环结构,取代基位于间位 b.能发生水解反应
c.能发生银镜反应 d.与FeCl3溶液发生显色反应。
(2)写出②的反应方程式:___________________________________________。
(3)写出D与浓硫酸在加热条件下发生的反应 。
(4)A的结构筒式是______________________。K^S*5U.C#
(5)若B分子(发生分子间脱水)发生酯化反应生成高分子的结构简式为 。
30. [化学-物质结构与性质] (13分) 目前,全世界镍的消费量仅次于铜、铝、铅、
锌,居有色金属第五位。镍行业发展蕴藏着巨大潜力。K^S*5U.C#
(1)配合物Ni(CO)4常温为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
晶体;基态Ni原子的电子排布式为 。
(3)配合物 分子内的作用力除共价键外,还存在的两种作
分子内的作用力除共价键外,还存在的两种作
用力是 (填编号)。K^S*5U.C#
A.氢键 B.离子键 C. 范德华力 D.配位键
(3)很多不饱和有机物在Ni催化下可以与H2发生加成反应。K^S*5U.C#
如:①CH2=CH2、②CH≡CH、③ 、④HCHO等,其中碳原子采取sp2杂化的分子有
(填物质序号),HCHO分子的立体结构为
形。K^S*5U.C#
、④HCHO等,其中碳原子采取sp2杂化的分子有
(填物质序号),HCHO分子的立体结构为
形。K^S*5U.C#
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据如下表。据此分析
Mn2+比Fe2+ (填 “更易” 或“更难 ”)再失去-个电子,从微粒结
构的角度简述其原因是

29.[物理-选修3-5](本题共有两小题,每小题6分,共12分。每小题只有一个选项符合题意。)
(1)在高速公路上发生一起交通事故,一辆质量为1500kg向南行驶的长途客车迎面撞
上了一质量为3000kg向北行驶的卡车,碰后两车接在一起,并向南滑行了一小段
距离后停止,根据测速仪的测定,长途客车碰前以20m/s的速率行驶,由此可判断
卡车碰前的行驶速率是

A.小于10m/s B.大于10m/s小于20m/s
C.大于20m/s小于30m/s D.大于30m/s小于40m/s
(2)近段时间,朝鲜的“核危机”引起了全世界的瞩目,其焦点问题就是朝鲜核电站采
用的是轻水堆还是重水堆。因为重水堆核电站在发电的同时还可以产出供研制核武
器的钚239( )。这种
)。这种 可由铀239(
可由铀239( )经过衰变而产生,则下列判
)经过衰变而产生,则下列判
断中正确的是
A. 与
与 的核内具有相同的中子数
的核内具有相同的中子数
B. 与
与 的核内具有相同的质子数
的核内具有相同的质子数
C.  经过2次
经过2次 衰变产生
衰变产生
D. 经过1次
经过1次 衰变产生
衰变产生
28.[物理-选修3-3](本题共有两小题,每小题6分,共12分。每小题只有一个选项符合题意。)
(1)小草、树叶上的小露珠常呈球形,其主要原因是 。(填选项前的编号)
A.受到重力的作用 B.因为表面张力的作用
C.重力和大气压力的同时作用 D.重力和表面张力互相平衡
(3)科学考察队到某一地区进行考察时携带一种测量仪器。该仪器导热性能良好,且
内部密闭有一定质量的气体(可视为理想气体),仪器的部分参数为:环境温度为
270C时,内部的气体压强为1.O×105Pa。若该地区的气温为-230C,不考虑密闭气
体的体积变化,则该仪器的内部气体压强为
 (填选项前的编号)
(填选项前的编号)
A.8.3×104Pa B.8.5×104Pa C.9.9×104 Pa D.1.2×105Pa
27.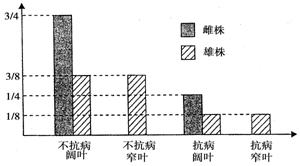 (15分)芦笋(2n=20)属于XY型性别决定植物,其嫩茎挺直,可供食用,当年养分的制造和积累的多少,会影响第二年嫩茎的产量,雄株产量明显高于雌株。芦笋种群中抗病和不抗病受基因A 、a控制,窄叶和阔叶受B、b控制。两株芦笋杂交,子代中各种性状比例如下图所示:
(15分)芦笋(2n=20)属于XY型性别决定植物,其嫩茎挺直,可供食用,当年养分的制造和积累的多少,会影响第二年嫩茎的产量,雄株产量明显高于雌株。芦笋种群中抗病和不抗病受基因A 、a控制,窄叶和阔叶受B、b控制。两株芦笋杂交,子代中各种性状比例如下图所示:
请据图分析回答:
(1)如果分析芦笋的核基因组,需要至少研究 条染色体;若一株芦笋的性染色体组成是XYY,最可能是亲代中 植株的减数分裂发生异常所致。
(2)运用统计学方法对上述遗传现象进行分析,可判断基因A 、a位于 染色体上,基因B、b位于 染色体上。
(3)亲代基因型为♀ ×♂ 。子代表现型为不抗病阔叶的雌株中,纯合子与杂合子的比例为 。
(4)请从经济效益的角度考虑,应选
植株通过组织培养进行大规模生产
选考部分
第Ⅱ卷选考部分共5题,共35分。其中,第28、29题为物理题,第30、31题为为化学题,考生从两道物理题、两道化学题中各任选一题作答,若第28、29题都作答,则按第28题计分,若第30 、31题都作答,则按第30题计分;第32题为生物题,是必答题。请将答案填写在答题卡选答区域的指定位置上
26.Ⅰ.(16分)为研究促甲状腺激素(TSH)分泌的影响因素,研究者从刚宰杀的大白
鼠体内分离新鲜的下丘脑和脑垂体。然后把这些结构单独或一起培养于含有或不
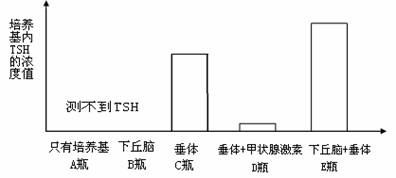 含有甲状腺激素的培养基中,培养后测定培养基内TSH的浓度,结果如下:K^S*5U.C#
含有甲状腺激素的培养基中,培养后测定培养基内TSH的浓度,结果如下:K^S*5U.C#
(1)在上述实验中设置A瓶的目的是____________________________。
(2)根据图中信息可知:
D瓶与A、C瓶比较说明:_________________________________。
E瓶与A、C瓶比较说明:_________________________________。
(3)人类TSH为一种糖蛋白,糖蛋白必须经内质网和高尔基体进一步加工合成。通
过转基因技术,可以使人的TSH基因得以表达的受体细胞是( )
A.大肠杆菌 B.酵母菌 C.T4噬菌体 D.质粒DNA
(4)如果研究者想进一步研究在活体实验条件下,验证甲状腺激素含量对TSH分泌
的影响,应如何设计实验?并预期实验结果。
实验材料:实验大白鼠、甲状腺激素、注射器及其它必需的材料和器具。
实验步骤:
第一步: 挑选挑生长期、大小、性别一致的实验大白鼠各10只随机分成两组,编号A、B;
第二步:A组______________________;B组______________________。
第三步:一段时间后,___________________________________
预期实验结果:___________________________________________
(5)依照培养基培养和活体实验结果,请画出甲状腺、垂体和下丘脑三者与相关激
素的关系图
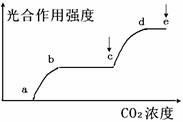 II.(9分)下图表示叶片的光合作用强度与植物周围空气中的CO2浓度的关系,ce段是增大了光照强度后测得的曲线。请回答:
II.(9分)下图表示叶片的光合作用强度与植物周围空气中的CO2浓度的关系,ce段是增大了光照强度后测得的曲线。请回答:
(1)图中e点后降低温度,曲线将 (填上升/下降)。
(2)影响图中曲线ab段和bc段叶片光合作用强度的主
要环境因素分别是 和 。
(3)如在e点后再次增大光照强度,则曲线能否持续
上升? ,
原因 。
25.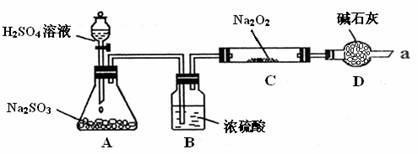 (16分)某同学想通过利用下图所示装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物
(16分)某同学想通过利用下图所示装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物 S*5U.C#
S*5U.C#
实验后测得反应前C管的质量为m1 g,反应后C管的质量为m 2 g,反应后装置D质量增加了n g。请分析:
Ⅰ.装置B的作用 。
装置D的作用 。
Ⅱ.如何检验反应中是否有O2生成
。
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3: 。
(1)若按假设2进行,反应方程式为 。
(2)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:产物是Na2SO4。
该方案是否合理 (填“是”或“否”),理由是 。
(3)若假设1成立,某同学以反应前后C管的质量差( m 2 - m 1 )g为依据推断生成Na2SO3的质量为( m 2 - m 1 )×126/64 g。老师提示推算不合理,请你分析其中的缘由: .
(4)若假设2成立,则参加反应的Na2O2 物质的量为 (列计算式)摩尔。
24.(15分))某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿制取活性ZnO的方案,实现废物综合利用,方案如下图所示
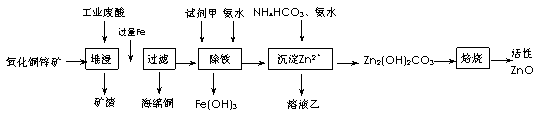
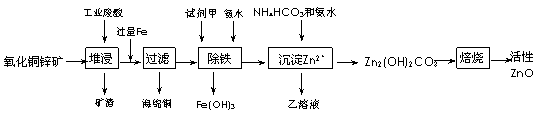
已知:298K时各离子开始沉淀及完全沉淀时的pH如下表所示。
|
离子 |
开始沉淀时的pH |
完全沉淀时的pH |
|
Fe2+ |
6.34 |
9.7 |
|
Fe3+ |
1.48 |
3.2 |
|
Zn2+ |
6.2 |
8.0 |
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS
不溶,这是由于相同温度下:Ksp(CuS) Ksp(ZnS)(选填“>”“<”或“=”)。
(2)你认为在除铁过程中选用下列物质中的 (填序号)作为试剂甲是最合适的。
A.KMnO4 B.O2 C.H2O2 D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在 范围之间。
(4)请写出加甲物质后,加入氨水控制调节溶液的pH下生成Fe(OH)3反应的离子方
程式 。
(5)298K时,残留在溶液中的c (Fe3+)在 __ _。以下。[Fe(OH)3的 = 2.70×10-39]
= 2.70×10-39]
(6)乙的溶液可直接用作氮肥,则乙的化学式是 。
(7)请写出“沉淀Zn2+”步骤中发生反应的化学方程式 。
23.(14分)能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
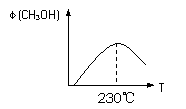
 (1)合成甲醇的反应为:CO(g)+2H2(g)
CH3OH(g);右图表示某次合成实验过程中甲醇的体积分数 φ(CH3OH)与反应温
(1)合成甲醇的反应为:CO(g)+2H2(g)
CH3OH(g);右图表示某次合成实验过程中甲醇的体积分数 φ(CH3OH)与反应温
度的关系曲线,则该反应的
△H (填“>、< 或 = ”下同)0 。
(2)若在230℃时,平衡常数K=1。若其它条件不变,
将温度升高到500℃时,达到平衡时,K 1 。
(3)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到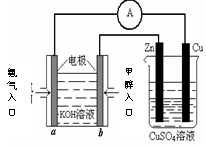 平衡时CO的转化率为90%,此时容器内的压强为开始时的
平衡时CO的转化率为90%,此时容器内的压强为开始时的
倍。
(4)利用甲醇燃料电池设计如右图所示的装置:
则该装置中Cu极为 极;
①写出b极的电极反应式
②当铜片的质量变化为12.8 g时,a极上消耗的 O2
在标准状况下的体积为 L。
(5)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l) == C2H4(g)+3O2(g) ΔH=+1411.0 kJ/mol
2CO2(g)+3H2O(l) == C2H5OH(1)+3O2(g) ΔH=+1366.8 kJ/mol
则由乙烯水化制乙醇反应的热化学方程式为 。
22.(20分)如图所示,第四象限内有互相正交的匀强
电场E与匀强磁场B1, E的大小为0.5×103V/m, B1大小为0.5T;第一象限的某个矩形区域内,有方向垂直纸面向里的匀强磁场B2,磁场的下边界与x轴重合.一质量m=1×10-14kg、电荷量q=1×10-10C
的带正电微粒以某一速度v沿与y轴正方向60°角
从M点沿直线运动,经P点即进入处于第一象限内的磁场B2区域.一段时间后,小球经过y轴上的N点并与y轴正方向成60°角的方向飞出。M点的坐标为(0,-10),N点的坐标为(0,30),不计粒子重力,g取10m/s2
(1)请分析判断匀强电场E的方向并求出微粒的运动速度v;
(2)匀强磁场B2的大小为多大?
(3) B2磁场区域的最小面积为多少?K^S*5U.C#
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com