
题目列表(包括答案和解析)
24.(8分)按要求写出下列化学用语
(1) NaOH的电子式 (2)S原子核外电子排布式
(3)O原子的电子排布图 (4)Cl―离子的结构示意图
23、已知X、Y中含有相同的元素,Z、W中也含有相同的元素,根据反应X+H2O
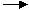 Y+H2 ;
Y+H2 ;
Z+H2O 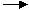 W+O2 (方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为
W+O2 (方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为
A、X>Y、 Z>W B、X<Y、 Z<W
C、X>Y、 Z<<W D、X<Y、Z>W
22、下列各反应中,水作为还原剂的是
A、2H2+O2  2H2O
B、SO3+H2O===H2SO4
2H2O
B、SO3+H2O===H2SO4
C、2F2+2H2O===4HF+O2 D、2Na+2H2O===2NaOH+H2
21、对于反应:2H2S+SO2===3S +2H2O,被氧化的硫原子与被还原的硫原子的质量之比为
A、1:1 B、2:1 C、3:1 D、1:2
20.用价层电子对互斥理论预测SO3和BF3的立体结构分别是:
A.平面三角形;三角锥形 B.三角锥形;平面三角形
C.三角锥形;三角锥形 D.平面三角形;平面三角形
19.下列各组物质熔点由低到高排列的是:
A.H2O 、H2S 、H2Se 、H2Te B.F2 、Cl2 、Br2 、I2
C.Li 、 Na 、 K 、 Rb D.NaCl 、MgCl2 、金刚石 、晶体硅
18.下列性质中,可以较充分说明某晶体是离子晶体的是
A. 具有较高的熔点 B. 固态不导电,水溶液能导电
C. 可溶于水 D. 固态不导电,熔融状态能导电
17.下列各组物质中,化学键类型相同,晶体类型也相同的是:
A. C(金刚石)和CO2 B. NaBr和HBr
C. Cl2和KCl. D. CH4和H2O ?
16.X和Y均为元素周期表前20号元素,X2-和Yˉ离子具有相同的电子层结构。下列正确的是:
A.原子半径 X<Y B. 离子半径X2->Yˉ
C.质子数X>Y D. 氢化物的稳定性H2X >HY
15.下列说法中正确的是:
A.?分子晶体中一定含有分子间作用力,可能有共价键
B.?含有极性键的分子一定是极性分子
C.?只要含有金属阳离子的晶体就一定是离子晶体
D.?金属晶体的熔点一定比分子晶体的高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com