
题目列表(包括答案和解析)
10、其他条件不变的情况下,下列说法不正确的是:
A. 对于反应nA(g)+B (g)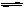 2C(g),平衡后增大压强,A的百分含量减小,则n≥2。
2C(g),平衡后增大压强,A的百分含量减小,则n≥2。
 B.
对于反应2A(g)
B.
对于反应2A(g)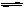 B(g) △H<0,若体系温度不再变化说明反应达到平衡状态。
B(g) △H<0,若体系温度不再变化说明反应达到平衡状态。
9、中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中不正确的是:
A. 用溶解度数据判断煮沸Mg(HCO3)2溶液得到的产物是Mg(OH)2而不是MgCO3 。
B. 用pH数据推测不同强酸弱碱盐在水溶液中水解程度的大小。
C. 用反应热数据的大小判断不同反应的反应速率的快慢。
D. 用平衡常数的大小判断化学反应可能进行的程度。
7、从下列实验 事实所引起的相应结论不正确的是:
事实所引起的相应结论不正确的是:
|
选项 |
实 验 事 实 |
结 论 |
|
A |
其它条件不变, 0.01mol/L的KMnO4酸性溶液分别与0.1mol/L的H2C2O4溶液和0.2mol/L的H2C2O4溶液反应,后者褪色时间短。 |
当其它条件不变时,增大反应物浓度可以使化学反应速率加快 |
|
B |
其它条件不变,分别将等体积、等物质的量浓度的Na2S2O3溶液和H2SO4混合液放在冷水和热水中,放在热水中的混合液先出现浑浊。 |
当其它条件不变时,反应体系的温度越高、化学反应速率越快 |
|
C |
将少量MnO2粉末加入盛有10%双氧水的锥形瓶内,在化学反应前后,MnO2的质量和化学性质都没有发生改变。 |
催化剂虽然可以加快化学反应的速率,但一定不参与化学反应过程 |
|
D |
一定条件下,分别在容积为1L和容积为2L的两个密闭容器中加入等量的氢气和碘蒸气,发生如下反应:H2(g)+I2(g)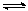 2HI(g),获得等量HI时需要的时间前者少。 2HI(g),获得等量HI时需要的时间前者少。 |
当其它条件不变时,气态反应体系的压强越大、化学反应速率越快 |

 子电池的电池反应为:Li+2Li0.35NiO2
2Li0.85NiO2。下列说法不正确的是:
子电池的电池反应为:Li+2Li0.35NiO2
2Li0.85NiO2。下列说法不正确的是:
A.放电时,负极的电极反应式:Li-e-=Li+
B.放电和充电过程恰好相反,则充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动
6、下列说法正确的是:
 D.实验室通常将固态氯化铁溶解在盐酸中,再稀释到相应浓度来配制FeCl3溶液。
D.实验室通常将固态氯化铁溶解在盐酸中,再稀释到相应浓度来配制FeCl3溶液。
5、对于工业制硫酸中接触室内的反应:2SO2(g)+O2 (g)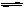 2SO3(g)
△H<0 。达到平衡时,只改变下列一个条件,平衡不发生移动
2SO3(g)
△H<0 。达到平衡时,只改变下列一个条件,平衡不发生移动 的是:
的是:
A. 升高温度 B. 恒温、恒容充入氧气
C. 恒温恒容充入SO3 D. 加入催化剂V2O5
4、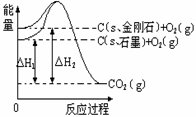 已知25℃、101kPa下,如右题图所示,石墨的燃烧热为393.51kJ/mol,金刚石的燃烧热为395.41kJ/mol 。下列说法或表达正确的是:
已知25℃、101kPa下,如右题图所示,石墨的燃烧热为393.51kJ/mol,金刚石的燃烧热为395.41kJ/mol 。下列说法或表达正确的是:
A. 金刚石比石墨稳定
B. C(s、石墨)=C(s、金刚石) △H=+1.9 kJ/mol
C. △H1<△H2
D. 如果使用催化剂,△H1和△H2都变小
3、 模型法是化学中把微观问题宏观化的最常见方法,对于2HBr(g) H2(g)+Br2(g)
反应。下列四个图中可以表示该反应在一定条件下达到平衡状态的是:
H2(g)+Br2(g)
反应。下列四个图中可以表示该反应在一定条件下达到平衡状态的是:
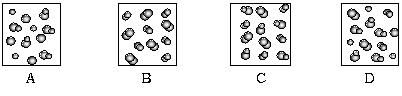
2、下列说法不正确的是:

37.(7分)取3.40g只含羟基、不含其他官能团的液态饱和多元醇,置于5.00 L氧气中,经点燃,醇完全燃烧。反应后气体体积减少0.56 L。将气体经CaO吸收,体积又减少2.80 L(所有体积均在标准状况下测定)。
(1)3.40g醇中C、H、O物质的量分别为:C mol、H mol、O mol;该醇中C、H、O的原子数之比为 。
(2)由以上比值 (填“能”或“不能”)确定该醇的分子式,其原因是 。
(3)如果将该多元醇的任意一个羟基换成一个卤原子,所得到的卤代物都只有一种,试写出该饱和多元醇的结构简式。
36.(20分)以A和乙醇为基础原料合成香料甲的流程图如下:
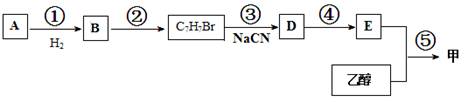
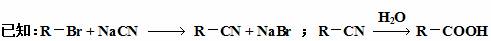
杏仁中含有A,A能发生银镜反应。质谱测定,A的相对分子质量为106。5.3g A完全燃烧时,生成15.4g CO2和2.7g H2O。
(1)A的分子式 ,A发生银镜反应的化学方程式为 。
(2)写出反应②的化学方程式 。
(3)上述反应中属于取代反应的是 。
(4)写出符合下列条件E的同分异构体有 种;
a.能发生银镜反应 b.不含-CH3 c.不能水解
写出其中能使FeCl3溶液显紫色,且苯环上的一溴代物有四种的同分异构体的结构简式 。
(5)写出反应⑤的化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com