
18.(12分)下面是测定硫酸钢晶体中结晶水含量的实验,请按要求填空。
(1)加热前应将晶体放在 中研碎,放在 中进行加热,加热失水后,应放在 中冷却。
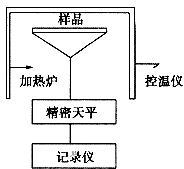
(2)判断是否完全失去结晶水的方法是 (定性和定量)。热重分析法是通过在一定程序控制的温度下,测定物质的质量与温度关系的一种实验技术,该技术使用的关键仪器是热重分析仪,其基本构造如图所示,记录仪画出质量…炉温曲线,又称热重曲线。
近年来有人对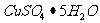 的加热分解作了进一步研究,发现
的加热分解作了进一步研究,发现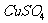 分解为CuO之前还有一黄色物质A产生,A的相对分子质量为239。3mol A与4mol水反应生成lmol蓝色固体B和2mol
分解为CuO之前还有一黄色物质A产生,A的相对分子质量为239。3mol A与4mol水反应生成lmol蓝色固体B和2mol 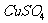 ,B的化学式可表示为
,B的化学式可表示为 。将物质B进行热重分析,其结果如下表所示。
。将物质B进行热重分析,其结果如下表所示。
|
温度 |
25 |
60 |
412 |
690 |
1480 |
|
加热前/mg |
94.1 |
94.1 |
90.4 |
79.7 |
63.6 |
(3)取一定质量的试样进行实验,即使质量不变,当温度升高时,天平显示出的试样质量也有微弱的增加,这种现象称为“表观增重”,其原因是温度升高 。
A.样品体积增大,密度减小
B.气体密度减小,浮力减小
C.地球对样品的吸引力增大
(4)黄色物质A的化学式(写成氧化物的形式)是 。
(5)蓝色固体B在60℃之前质量不变,这一现象说明 。
蓝色固体B在412-690℃之间发生反应的化学方程式为
(6)如果表中的质量数据未经估读,则该精密天平的精度是托盘天平(最小刻度为0.1g)精度的 倍。
17.(10分)利用下图所示的装置,可以验证 和HCl的有关性质。实验前a、b、c活塞均关闭。
和HCl的有关性质。实验前a、b、c活塞均关闭。
(1)通过挤压胶头滴管和控制活塞的开关,若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是
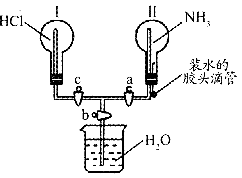
(2)通过挤压胶头滴管和控制活塞的开关,在烧瓶l中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是
16.将l5.6g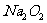 和5.4g Al同时放人一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则
和5.4g Al同时放人一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则
A.反应过程中得到6.72L的气体(标准状况)
B.最终得到的溶液中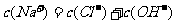
C.最终得到7.8g的沉淀
D。最终得到的溶液中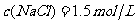
15.下列有关实验的叙述不正确的是
A.不宜用带胶塞的试剂瓶盛放高锰酸钾溶液
B.苯酚不慎沾在手上,立即用浓氢氧化钠溶液洗涤
C.欲取某纯碱样品5. 5g,可用托盘天平称量
D.配制lmol/L NaCl溶液时,用蒸馏水洗涤容量瓶后,直接注入NaCl溶液
14.在密闭容器中,aA(g) bB(g)达到平衡后,保持温度不变,将容器体积增加1倍,当达到新平衡时,8的浓度是原来的60%,下列说法正确的是
bB(g)达到平衡后,保持温度不变,将容器体积增加1倍,当达到新平衡时,8的浓度是原来的60%,下列说法正确的是
A.平衡向正反应方向移动了
B.物质A的转化率减少了
C.物质B的质量分数增加了
D.
13.镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:
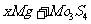
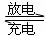
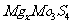 在镁原电池放电时,下列说法错误的是
在镁原电池放电时,下列说法错误的是
A.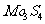 发生氧化反应
发生氧化反应
B.正极反应为: 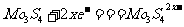
C.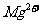 向正极迁移
向正极迁移
D.负极反应为: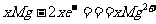
12.下列反应的离子方程式正确的是
A.小苏打溶液跟烧碱反应:
B.向Ca(ClO)2溶液中通入过量二氧化碳:
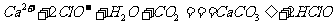
C.氯化铁溶液中加入铁粉: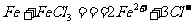
D.过氧化钠和冷水反应: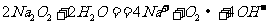
11.下列各组离子中,因发生氧化还原反应而不能大量共存的是
A.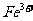 、
、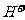 、
、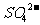 、
、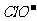
B.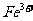 、
、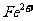 、
、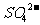 、
、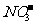
C.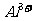 、
、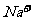 、
、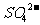 、
、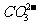
D.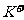 、
、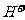 、
、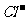 、
、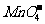
10.下列有关阿伏加德罗常数的叙述正确的是
A.1mol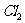 与足量水反应转移电子数约为
与足量水反应转移电子数约为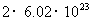 个
个
B.1mol碳酸钠溶于水所得溶液中所含阴离子数大于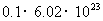 个
个
C.32g氧气与金属钠反应时转移电子数约为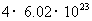 个
个
D.1mol金刚石晶体中约含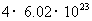 个C-C键
个C-C键
9.短周期元素A、B、C、D的原子序数依次增大,它们的原子最外层电子数之和为l7,其中A、C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述不正确的是
A.B与D可形成离子化合物
B.原子半径:B>C>D
C.由A形成的化合物种类繁多,结构复杂
D.最高价氧化物对应的水化物的酸性:A<C<D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com