
7.下列关于Cl、N、S等非金属元素化合物的说法正确的是 ( )
A.漂白粉的成分是次氯酸钙
B.实验室可用浓硫酸干燥氨气
C.实验室可用NaOH 处理NO2 和HCl 废气
D.用饱和食盐水吸收氯气的尾气,以达环境保护
6.已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是 ( )

A.甲是浓氨水,乙是浓硫酸 B.甲是浓氨水,乙是浓盐酸
C.甲是浓盐酸,乙是浓氨水 D.甲是浓硝酸,乙是浓氨水
5.下面说法,其中正确的是 ( )
A.凡是生成两种或两种以上物质的反应都是分解反应
B.一种元素可能有多种氧化物,但一种化合价只对应一种氧化物
C.有些化学反应不属于化合、分解、置换、复分解反应中的任何一种反应
D.直径介于1nm~10nm之间的微粒称为胶体
4.下列叙述中正确的是 ( )
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18种元素
C.副族元素中没有非金属元素
D.碱金属元素是指ⅠA族的所有元素
3.下列说法正确的是 ( )
A.发酵粉中主要含有氢氧化钠,能使焙制出的糕点疏松多孔
B.含碘食盐中的碘元素遇淀粉溶液变蓝
C.日常生活中常用75%乙醇溶液来杀菌消毒
D.硫酸氢钠属于盐类,是强酸强碱盐,其水溶液显中性
2.氮气是空气中的主要成分,且含量很大,现已有科学家设计出了液氮蒸汽机,即利用液氮的蒸发来驱动机车,从而达到保护环境的目的。其主要依据是 ( )
A.液氮的沸点为-195.8°C,远低于常温 B.氮气与氧气反应放热
C.氮气在空气中燃烧放热 D.氮气在空气中约78%(体积分数)
1.K2O、KOH、K2CO3、KCl、K2SO4可按某种标准划为同一类物质,
①钾的化合物 ②钾盐 ③钾的含氧化合物 ④电解质
⑤能与硝酸反应的物质 ⑥溶于水并形成溶液的物质
下列分类标准正确的是 ( )
A.①④⑥ B.①②③④⑤⑥ C.②④⑤⑥ D.①②④⑤
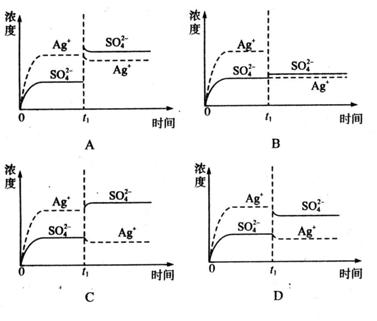
24.已知Ag2SO4的KSP为2.0×10-5,将适量Ag2SO4固体溶于100mL水中至刚好饱和,该过程中Ag+和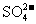 浓度随时间变化关系如下图(饱和Ag2SO4溶液中
浓度随时间变化关系如下图(饱和Ag2SO4溶液中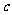 (Ag+)=0.034mol·L-1)。若
(Ag+)=0.034mol·L-1)。若 时刻在上述体系中加入100mL 0.020mol·L-1 Na2SO4溶液,下列示意图中,能正确表示
时刻在上述体系中加入100mL 0.020mol·L-1 Na2SO4溶液,下列示意图中,能正确表示 时刻后Ag+和
时刻后Ag+和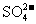 浓度随时间变化关系的是
。
浓度随时间变化关系的是
。
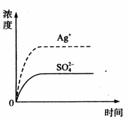
23.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
|
实验编号 |
HA物质的量 浓度(mol·L-1) |
NaOH物质的量 浓度(mol·L-1) |
混合溶液的pH |
|
甲 |
0.2 |
0.2 |
pH=a |
|
乙 |
C1 |
0.2 |
pH=7 |
|
丙 |
0.2 |
0.1 |
pH>7 |
|
丁 |
0.1 |
0.1 |
pH=9 |
请回答:
(1)不考虑其它组的实验结果,单从甲组情况分析,
若a 7(填>、<或=),则HA为强酸;
若a 7(填>、<或=),则HA为弱酸。
(2)在乙组中混合溶液中离子浓度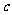 (A-)与
(A-)与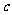 (Na+)的大小关系是
。
(Na+)的大小关系是
。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是 酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是 。
(4)丁组实验所得混合溶液中由水电离出的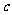
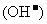 =
mol·L-1。
=
mol·L-1。
22.(1)将等质量的锌粉分别投入10mL 0.1mol•L-1 HCl和10mL 0.1mol•L-1的CH3COOH的溶液中。
①若锌不足量,反应快的是 ;
②若锌过量,产生氢气的量的关系为 。
(2)将等量的锌粉分别投入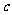 (H+)均为1mol·L-1、体积均为10mL的盐酸和醋酸溶液中。
(H+)均为1mol·L-1、体积均为10mL的盐酸和醋酸溶液中。
①若锌不足量,反应快的是 ;
②若锌过量,产生氢气的量的关系为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com