
4.根据下列三个反应的化学方程式,判断有关物质的还原性强弱顺序
①I2+SO2+2H2O=H2SO4+2HI ②2FeCl2+Cl2=2FeCl3 ③2FeCl3+2HI=2FeCl2+2HCl+I2
A.I->Fe2+>Cl->SO2 B.Cl->Fe2+>SO2>I-
C.Fe2+>I->Cl->SO2 D.SO2>I->Fe2+>Cl-
3.下列条件下,两瓶气体所含分子数一定相等的是
A.同体积、同密度的C2H4和C3H6 B.同温度、同体积的H2和N2
C.同质量、不同密度的N2和CO D.同压强、同体积的N2O和CO2
2.下列变化中加入氧化剂才能发生的是
A.2Cl-→Cl2 B.Fe3+→Fe2+ C.Cu2+→Cu D.MnO4-→MnO2
1.下列说法正确的是
A.摩尔是国际单位制七个基本物理量之一 B.Cl2的摩尔质量是71 g/mol
C.标准状况下,22.4LH2O的物质的量为1mol D.1molH2的质量是1g
25.(共8分)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题:
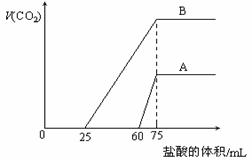
(1)原NaOH溶液的物质的量浓度为 。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是什么?其物质的量之比为多少?
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为 mL。
24.(共9分)下列图1中B是一种常见的无色无味的液体。C是一种有磁性的化合物,E是一种无色无味的有毒气体。根据下列图1、图2,回答下列问题:
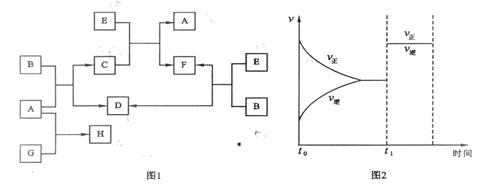
(1)E和N2是等电子体(原子数相同、电子数均相同、结构相似),请写出可能E的电子式: 。
(2)若G是一种淡黄色固体单质,在通常情况下16 g G和足量的A反应放出的热量为Q kJ(Q > 0),写出这个反应的热化学方程式: 。
(3)若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式: ;请说明H的水溶液止血的原理
。将过量F通入NaOH得到的溶液再与H溶液反应的离子方程式为 。
(4)在101kPa和150℃时,可逆反应E(g) +
B(g) F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) 。
F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) 。
A.升高温度 B.增大压强 C.加入催化剂
D.将B、E的浓度均增加1倍
23.(共10分)化学式为C11H12O4的芳香族化合物A、B互为同分异构体,A和D都能发生银镜反应,E的一溴取代物只有两种, A经①、②两步反应得C、D和E。B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如图所示。
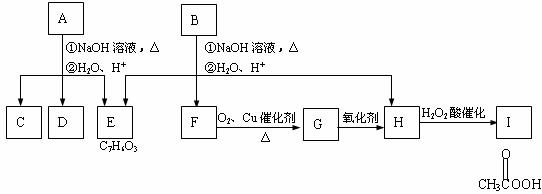
(1)A有2种可能结构,写出其结构简式 。
(2)在B、C、D、F、G、I化合物中,互为同系物的是 。
(3)写出D与F在加热和浓H2SO4催化作用下发生反应的化学方程式 ,指出反应类型 。
(4)除银镜反应外至少选用其它两种实验方法证明D具有还原性,请按要求填写下表:
|
|
所选试剂 |
观察到的实验现象 |
|
方法1 |
|
|
|
方法2 |
|
|
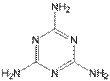
22.(共8分)近期“问题奶粉”引起了人们的极大关注。 其问题主要是奶粉中掺杂了三聚氰胺,三聚氰胺性状为纯白色晶体,无味,密度1.573克/厘米3 (16℃)。常压下熔点为354℃(分解),快速加热升华,升华温度为300℃;微溶于冷水,易溶于热水、醚、苯和四氯化碳,可溶于甲醇、乙酸、热乙二醇等。
(1)三聚氰胺的结构简式如下图所示的环状物,则三聚氰胺的分子式为_________该物质的含氮量为 ,三聚氰胺为三个氰胺分子加聚而成,已知氰胺分子中除H原子外,C、N 原子的最外层均达8个电子的结构,则氰胺的电子式为_______________, 三聚氰胺和相对分子质量相近的硝基苯比较 (无色或微黄色具苦杏仁味的油状液体。相对分子质量为123.11;熔点5.7℃。沸点210.9℃)。三聚氰胺的熔点特殊的高,其原因是______________________________。
(2)下列关于三聚氰胺的说法中,正确的有________________(填序号,多选扣分);
A. 三聚氰胺是一种含氮量高的白色结晶,无味,所以掺入奶粉后不易被发现
B. 三聚氰胺分子中所有原子一定在同一个平面上
C. 三聚氰胺易溶于冷水,属于分子晶体
D. 三聚氰胺呈弱碱性,可以与酸反应
E. 采用三聚氰胺制造的食具一般都会标明“不可放进微波炉使用”
(3)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%。不法分子通过在低蛋白含量的奶粉中加入三聚氰胺来“提高”奶粉中的蛋白质含量,导致许多婴幼儿肾结石。假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的假奶粉中掺入了________g的三聚氰胺就可使奶粉“达标”(小数点后保留1位有效数字)。
21.(共6分)如下图所示,A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液见图。
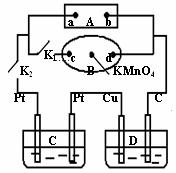
(1)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向c端移动,则电源b端为 极,通电一段时间后,观察到滤纸d端的电极反应式是 ;
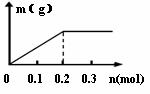
(2)已知C装置中溶液为Cu(NO3)2和X(NO3)3,且均为0.1mol,打开K1,关闭K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如下图所示。则Cu2+、X3+、H+氧化能力由大到小的顺序是 ;D装置中溶液是H2SO4,则电极C端从开始至一段时间后的实验现象是:_______ ___。
20.(5分)已知: NO3-+4H++3e-→NO+2H2O 。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中有一种(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:___________________________________。
(2)反应中硝酸体现了________________ 、________________ 性质。
(3)若1mol甲与某浓硝酸反应时,被还原硝酸的物质的量增加,原因是:
____________________________ _____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com