
14.用惰性电极电解500mL一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1molCu(OH)2后能恰好恢复到电解前的浓度和pH。则原硫酸铜溶液的浓度为( )
A.0.2mol/L B.>0.2mol/L C.<0.2mol/L D.无法确定
13.在金属焊接和切割过程,常能闻到一股鱼腥臭味。经检测,那是电弧产生的臭氧的气味。臭氧具有很强的氧化性,可使湿润的KI一淀粉试纸变蓝色,有关反应的化学方程式为:O3+2KO+H2O 2KOH+I2+O2,对此反应,下列说法正确的是 ( )
A.在此反应中O3是氧化剂,O2是还原产物
B.反应中1mol O2参加反应,转移的电子为6mol
C.由此反应可知,氧化性强弱关系为:O3>I2>O2
D.被还原的氧原子与被氧化的I-的个数比为1:2
12.在一定条件下,下列粒子的还原性顺序为:C1-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是 ( )
A.2Fe3++SO2+2H2O 2Fe2++SO42-+4H+
B.I2+SO2+2H2O 4H++SO42-+2I-
C.2Fe3++2I- 2Fe2++I2
D.2Br-+4H++SO42- SO2+Br2+2H2O
11.下列热化学方程式中,能正确表示物质的燃烧热的热化学方程式的是 ( )
A.CO(g)+1/2O2(g)=CO2(g);△H=-283.0kJ/mol
B.C(s)+1/2O2(g)=CO(g);△H=-110.5kJ/mol
C.H2(g)+1/2O2(g)=H2O(g);△H=-241.8kJ/mol
D.2C8H18(g)+25O2(g)=16CO2(g)+18H2O(1);△H=-11036kJ/mol
9.用铂作电极电解下列溶液,一段时间内,阴极产生的气体体积是阳极产生气体体积两倍的是 ( )
A.NaOH B.CuC12 C.HC1 D.CuSO4
|
4P(白磷,s)+5O2(g) 2P2O5(s);△H -a kJ/mol
4P(红磷,s)+5O2(g) 2P2O5(s);△H -b kJ/mol
若a、b均大于零,则a和b的关系为 ( )
A.a<b B.a=b C.a>b D.无法确定
8.根据下列事实,判断离子的氧化性顺序为 ( )
①A2+B2+=A2++B
②D+2H2O=D(OH)2+H2↑,
③以B、E为电极与E的盐溶液组成原电池,两个电极反应分别为:E2++2e-=E和B-2e-=B2+
A.E2+>B2+>A2+>D2+ B.D2+> E2+> A2+> B2+
C.D2+> B2+> A2+> E2+ D.A2+> B2+> D2+> E2+
7.金属加工后的废切削液中含2%-5%的NaNO2,它是一种环境污染物。人们用NH4C1溶液来处理此废屑削液,使NaNO2转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4C1→NaC1+NH4NO2
第二步:NH4NO2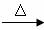 N2↑+2H2O
N2↑+2H2O
下列对第二步反应的叙述中正确的是 ( )
①NH4NO2只是氧化剂 ②NH4NO2只是还原剂
③NH4NO2发生了分解反应 ④只有氮元素的化合价发生了变化
⑤NH4NO2既是氧化剂又是还原剂
A.①③ B.①④ C.②③④ D.③④⑤
6.下列离子在溶液中因发生氧化还原反应而不能大量共存的是 ( )
A.H2O+、NO3-、Fe2+、Na+ B.Ag+、NO3-、C1-、K+
C.K+、Ba2+、OH-、SO42- D.Cu2+、NH4+、Br-、OH-
5.在硫酸的工业制法中,下列生产操作与说明生产操作的原因二者都正确的是 ( )
A.矿石燃烧前需要粉碎,因为大块矿石不能燃烧
B.从沸腾炉出来的炉气需净化,因为炉气中二氧化硫会与杂质反应
C.SO2被氧化为SO3时需使用催化剂,这样可提高SO 2的转化率
D.SO3用98.3%的浓H2SO4吸收 ,能提高吸收效率的防止形成酸雾
4.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源标准的是 ( )
①天然气 ②煤 ③核能 ④石油
⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.②⑤⑥⑦⑧ D.③④⑤⑥⑦
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com