
15£®ÏÂÁÐ˵·¨ÖÐÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®´ÎÍâ²ãµç×ÓÊýÊÇ2»ò8»ò18µÄÔ×ÓÒ»¶¨ÊÇÖ÷×åÔªËØ
B£®HClÆøÌåÈÜÓÚË®¹²¼Û¼ü±»ÆÆ»µ
C£®ÖÊÁ¿Êý¿ÉÒÔ±íʾÔ×ÓÏà¶ÔÔ×ÓÖÊÁ¿µÄ½üËÆÖµ
D£®ºËÍâµç×ÓÅŲ¼ÏàͬµÄ΢Á££¬Ò»¶¨¾ßÓÐÏàͬµÄ»¯Ñ§ÐÔÖÊ
14£®·ÖÀàÊÇ»¯Ñ§Ñо¿Öг£Óõķ½·¨¡£ÏÂÁзÖÀà·½·¨ÖУ¬²»ÕýÈ·µÄÊÇ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®¸ù¾ÝÔªËØÔ×Ó×îÍâ²ãµç×ÓÊýµÄ¶àÉÙ½«ÔªËØ·ÖΪ½ðÊôºÍ·Ç½ðÊô
B£®ÒÀ¾ÝÓÐÎÞµç×ÓתÒÆ£¬½«»¯Ñ§·´Ó¦·ÖΪÑõ»¯»¹Ô·´Ó¦ºÍ·ÇÑõ»¯»¹Ô·´Ó¦
C£®¸ù¾Ýµç½âÖÊÔÚÈÛÈÚ״̬ÏÂÄÜ·ñÍêÈ«µçÀ뽫µç½âÖÊ·ÖΪǿµç½âÖʺÍÈõµç½âÖÊ
D£®ÒÀ¾Ý×é³ÉÔªËصÄÖÖÀ࣬½«´¿¾»Îï·ÖΪµ¥Öʺͻ¯ºÏÎï
13£®ÏÂÁÐÀë×Ó·½³ÌʽÕýÈ·µÄÊÇ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®Óô×Ëá³ýȥˮ¹¸£ºCaCO3 + 2H+==Ca2+ + H2O + CO2¡ü
B£®Ca(HCO3)2Óë¹ýÁ¿Ca(OH)2ÈÜÒº·´Ó¦£º
Ca2++2HCO3£+2OH£ £½CaCO3¡ý+CO32£+2H2O
C£®ÓÃ̼ËáÄÆÈÜÒºÎüÊÕÉÙÁ¿¶þÑõ»¯Áò£º2CO32-+SO2+H2O ==2HCO3-+SO32-
D£®ÓÃÏ¡HNO3ÈܽâFeS¹ÌÌ壺FeS+2H+=Fe2++H2S¡ü
12£®ÄÑÈÜÎïÇ⻯ÑÇÍ(CuH)¿ÉÓÃCuSO4ÈÜÒººÍ¡°ÁíÒ»ÖÖ·´Ó¦ÎÔÚ40¡æ~50¡æʱ·´Ó¦Éú³É¡£CuH²»Îȶ¨£¬Ò׷ֽ⣻CuHÔÚÂÈÆøÖÐÄÜȼÉÕ£»³£ÎÂϸúÑÎËá·´Ó¦ÄܲúÉúÆøÌ壬ÒÔÏÂÓйØËüµÄÍƶÏÖв»ÕýÈ·µÄÊÇ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®¡°ÁíÒ»ÖÖ·´Ó¦Îһ¶¨¾ßÓÐÑõ»¯ÐÔ¡¡¡¡¡¡ B£®CuH¼È¿É×öÑõ»¯¼ÁÒ²¿É×ö»¹Ô¼Á
C£®CuH+Cl2 CuCl+HCl¡ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®CuH+HCl==CuCl¡ý+H2¡ü
CuCl+HCl¡ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®CuH+HCl==CuCl¡ý+H2¡ü
11£®Éè°¢·ü¼ÓµÂÂÞ³£ÊýΪNA¡£ÔòÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®³£Î³£Ñ¹Ï£¬18.0 gÖØË®(D2O)ÖÐËùº¬µÄµç×ÓÊýΪ10 NA
B£®1cm3ÌúËùº¬µÄÌúÔ×ÓÊýÊǦѡ¤NA/56(¦ÑÊÇÌúµÄÃܶȣ¬µ¥Î»Îªg¡¤cm£3)
C£®2.24LCO2Óë×ãÁ¿µÄNa2O2·´Ó¦£¬Na2O2תÒƵĵç×Ó×ÜÊýÒ»¶¨Îª0.1NA
D£®³£ÎÂÏ£¬2.7gÂÁƬͶÈë×ãÁ¿µÄŨÁòËáÖУ¬ÂÁʧȥµÄµç×ÓÊýΪ0.3NA
9£®1999ÄêÔø±¨µ¼ºÏ³ÉºÍ·ÖÀëÁ˺¬¸ßÄÜÁ¿µÄÕýÀë×ÓN5+µÄ»¯ºÏÎïN5AsF6£¬ÏÂÁÐÐðÊö´íÎóµÄÊÇ
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®N5+¹²ÓÐ34¸öºËÍâµç×Ó¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®N5+ÖеªµªÔ×Ó¼äÒÔ¹²Óõç×Ó¶Ô½áºÏ
C£®»¯ºÏÎïN5AsF6ÖÐAs»¯ºÏ¼ÛΪ+1 ¡¡¡¡¡¡ D£®»¯ºÏÎïN5AsF6ÖÐF»¯ºÏ¼ÛΪ-1
|
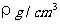 £¬NAΪ°¢·ü¼ÓµÂÂÞ³£Êý£¬ÏàÁÚµÄÁ½¸öCs+µÄºË¼ä¾àΪa cm£¬ÔòCsClµÄʽÁ¿¿ÉÒÔ±íʾΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
£¬NAΪ°¢·ü¼ÓµÂÂÞ³£Êý£¬ÏàÁÚµÄÁ½¸öCs+µÄºË¼ä¾àΪa cm£¬ÔòCsClµÄʽÁ¿¿ÉÒÔ±íʾΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
¡¡¡¡ A£® 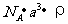 ¡¡¡¡¡¡ B£®
¡¡¡¡¡¡ B£®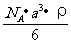 ¡¡C£®
¡¡C£® 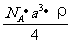 ¡¡¡¡¡¡¡¡¡¡ ¡¡D£®
¡¡¡¡¡¡¡¡¡¡ ¡¡D£®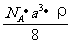
8£®ÔÚÖ¸¶¨»·¾³ÖУ¬ÏÂÁи÷×éÀë×ÓÒ»¶¨¿ÉÒÔ´óÁ¿¹²´æµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®Ê¹pHÊÔÖ½³ÊºìÉ«µÄÈÜÒºÖУºFe2+¡¢NO3-¡¢SO42-¡¢Na+
B£®µÎ¼ÓÎÞÉ«·Ó̪ÊÔÒººóÈÔÎÞÉ«µÄÈÜÒºÖУºCO32£¡¢K+¡¢ClO£¡¢AlO2£
C£®ÔÚc(H+)/c(OH£)= 1¡Á1013µÄÈÜÒºÖУºNH4+¡¢Ca2+¡¢C1£¡¢K+
D£®¼ÓÈëÂÁ·Ûºó²úÉú´óÁ¿ÇâÆøµÄÈÜÒºÖУºNH4+¡¢Na+¡¢NO3£¡¢SO42£
7£®ÔÚäåË®ÖмÓÈë»òͨÈëÏÂÁÐÎïÖÊ£º
¢Ùþ·Û ¢ÚSO2 ¢ÛH2S ¢Ü»îÐÔÌ¿ ¢ÝAgNO3ÈÜÒº ¢ÞNaHCO3ÈÜÒº ¢ßNH3 ¢à KI ÄÜʹÈÜÒºÍÊÉ«µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡ (¡¡)
A£®È«²¿ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£® ¢Ü¢à ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£®³ý¢àÍâ¡¡ ¡¡¡¡¡¡¡¡ D£® ¢Ú¢Û¢Ü¢Ý
6£®ÏÂÁÐʵÑé·½°¸ÄܴﵽĿµÄµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®³ýÈ¥Fe·ÛÖлìÓеÄI2£º¼ÓÈÈʹI2Éý»ª
B£®³ýÈ¥NaCl¹ÌÌåÖлìÓеÄMgCl2£º¼ÓÈëKOHÈÜÒººó¹ýÂË£¬ÂËÒºÕô·¢ ½á¾§
C£®³ýȥ̼ËáÄÆÖлìÓеÄ̼ËáÇâÄÆ£º¼ÓÈë¹ýÁ¿µÄÇâÑõ»¯ÄÆÈÜÒº£¬Õô·¢½á¾§
D£®³ýÈ¥ÇâÑõ»¯Ã¾ÖлìÓеÄÇâÑõ»¯¸Æ£º·ÅÈëË®ÖнÁ°è³É½¬×´ºó£¬¼ÓÈë×ãÁ¿ÂÈ»¯Ã¾ÈÜÒº£¬³ä·Ö½Á°è£¬¹ýÂË£¬³ÁµíÓÃÕôÁóˮϴµÓ
5£®ÏÂͼÖÐÿÌõÕÛÏß±íʾÖÜÆÚ±í¢ôA-¢÷AÖеÄijһ×åÔªËØÇ⻯ÎïµÄ·Ðµã±ä»¯(ÍâѹΪ1atm)£¬ÆäÖСø´ú±íµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
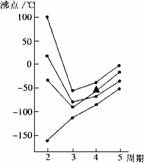
A£®AsH3¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡B£®HBr¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£®H2Se¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡D£®GeH4
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com