
24.[B](14分)
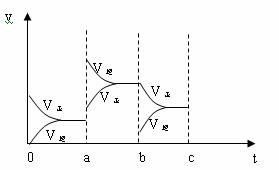
(1)下图左表示在密闭容器中反应:2SO2+O2 2SO3 ΔH<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是
;b c过程中改变的条件可能 ;
2SO3 ΔH<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是
;b c过程中改变的条件可能 ;
(2)如右图所示,将6 mol
X和3 mol
Y混合气体置于体积可变的等压容器中,在一定温度下发生如下反应:2X(g)+Y(g) 2Z(g)。反应达到平衡状态A时,测得气体总物质的量为6.6 mol。若X、Y、Z的起始物质的量分别用a、b、c表示,回答下列问题:
2Z(g)。反应达到平衡状态A时,测得气体总物质的量为6.6 mol。若X、Y、Z的起始物质的量分别用a、b、c表示,回答下列问题:
① 达平衡状态A时,Y的转化率为____________,在达到平衡状态
A的容器中通人少量Y,体系中X的体积分数_____________(填“增大”或“减小”或“不变”)。
② 若起始时a=3.2 mol,且达到平衡后各气体的体积分数与平衡状态A相同,则起始时b、c的取值分别为b___________________;c____________________。
③ 若要使反应开始时向逆反应方向进行,且达到平衡后各气体的物质的量与平衡状态A相同,则起始时c的取值范围是__________________________。
24.[A](14分)反应3Fe(S)+4H2O(g) Fe3O4(s)+4H2(g)在一可变的容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g)在一可变的容积的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是 (填增大、不变、减小,以下相同)
②将容器的体积缩小一半,其正反应速率 ,逆反应速率 。
③保持体积不变,充入N2使体系压强增大,其正反应速率 ,逆反应速率 。
④保持压强不变,充入N2使容器的体积增大,其正反应速率 ,逆反应速率 。
23.(3分)计算下列各题:
(1) 用pH=2的盐酸中和pH=12的NaOH溶液,所用盐酸V(酸)和氢氧化钠溶液V(碱)的体积比是V(酸)﹕V(碱)= ;
(2) 用pH=3的盐酸中和pH=12的NaOH溶液,所用盐酸V(酸)和氢氧化钠溶液V(碱)的体积比是V(酸)﹕V(碱)= ;
(3) 用pH=a的盐酸中和pH=b的NaOH溶液, 所用盐酸V(酸)和氢氧化钠溶液V(碱)的体积比是V(酸)﹕V(碱)= 。
22.(7分)
(1)对比同体积、同浓度的盐酸和醋酸,c(H+)前者 后者,与碱完全中和时,消耗NaOH的物质的量是前者 后者,与足量的Zn反应产生H2的速率是前者 后者。(填“>”、“<”或“=”)
(2)25℃时,在 0.5 L 0.2 mol·L-1的HA溶液中,有0.01 mol的HA电离成离子。求该温度下HA的电离常数 。
(3)将纯水加热至较高温度, 水的离子积变 ,pH变 ,呈 性。
21.(8分)恒温下,在容积为2 L的恒容密闭容器A中通入1 mol N2与1mol H2的混合气体,发生如下反应:N2 (g) + 3 H2(g)  2NH3(g),△H<0,一段时间后,达到平衡,若平衡时氨气的物质的量为0.4mol。
2NH3(g),△H<0,一段时间后,达到平衡,若平衡时氨气的物质的量为0.4mol。
(1)此温度时该反应的K值为 。
(2) 若在此温度下,向另一容积为1 L的恒容容器B中按物质的量分别为2 mol 、1 mol 、1 mol充入N2、H2、NH3,此时,该反应是否处于平衡状态 (填“是”或“否”),此时,反应向 方向进行。
(3)其他条件不变,若降低A容器的温度,该反应K值 (填“增大”、“减小”或“不变”)。
20.(8分)现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1) 该反应的逆反应为 热反应,且m+n p (填“>”“=”“<”)。
(2) 减压时,A的质量分数 。(填“增大”“减小”或“不变”,下同)
(3) 若加入B(体积不变),则A的转化率_________。
(4) 若升高温度,则平衡时B、C的浓度之比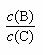 将
。
将
。
(5) 若加入催化剂,平衡时气体混合物的总物质的量 。
(6) 若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色 (填“变深”“变浅”或“不变”)。
19.(6分)某温度下SO2的转化反应的平衡常数K =532.4. 2SO2+O2  2SO3
2SO3
下面三个混合体系中各物质的浓度如下表:
|
体系 |
c(SO2) mol/L |
c(O2) mol/L |
c(SO3) mol/L |
反应方向 |
|
(1) |
0.0600 |
0.400 |
2.000 |
|
|
(2) |
0.0960 |
0.300 |
0.500 |
|
|
(3) |
0.0862 |
0.263 |
1.020 |
|
试判断各体系中反应进行的方向:
体系(1)
体系(2)
体系(3) 。
18.下列说法正确的是
A.HCl溶液中无OH-
B.NaCl溶液中既无OH_也无H+
C.NaOH溶液中无H+
D.常温下,任何物质的水溶液中都有H+和OH-,且KW=c(H+)·c(OH-)=10-14
第Ⅱ卷(非选择题共46分)
17.向醋酸溶液中加入NaHSO4固体,则醋酸的电离程度
A.增大 B.减小 C.不变 D.无法确定
16.下列电离方程式正确的是
A.Al2(SO4)3 2Al3++3SO42- B.CH3COOH
2Al3++3SO42- B.CH3COOH  H++CH3COO-
H++CH3COO-
C.NH3·H2O==NH4+ + OH- D.Ca(OH)2 Ca2++2OH-
Ca2++2OH-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com