
15.有镁铝合粉末10.2g,将它溶于500mL 4mol/L的盐酸里,若要使沉淀质量达到最大值,则需加入2mol/L氢氧化钠溶液的体积为 ( )
A.1000mL B.500mL C.100mL D.1500mL
14.对于反应2A2(g)+B(S) 2C(g),能增大正反应速率的措施是 ( )
2C(g),能增大正反应速率的措施是 ( )
A.加入少量B物质 B.增大容器容积
C.恒容时充入Ar气体 D.恒容时加入适量的C物质
13.将1.12g铁粉加入25mL 20mol·L-1的氯化铁溶液中,充分反应后,其结果是 ( )
①铁有剩余,溶液呈浅绿色,Cl-浓度基本不变
②往溶液中滴入无色KSCN溶液,显红色
③Fe2+和Fe3+的物质的量之比为6:1
④氧化产物与还原产物的物质的量之比为2:5
A.①② B.②③ C.③④ D.①④
12.下列离子方程式中,属于水解反应的是 ( )
A.HCOOH+H2O HCOO- + H3O+
HCOO- + H3O+
B.CO2+H2O HCO3- + H+
HCO3- + H+
C.CO32- + H2O HCO3- + OH-
HCO3- + OH-
D.HS- + H2O S2- + H3O+
S2- + H3O+
11.100mL 6mol/L的H2SO4溶液与过量的Zn粉反应,在一定温度下,为了减缓反应进行的速率,但由不影响生成H2的总量,可以向反应物中加入适量的 ( )
A.Na2CO3晶体 B.CH3COONa晶体
C.K2SO4晶体 D.KNO3溶液
10.在一定温度下,反应A2(g)+B2(g)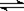 2AB(g)达到平衡的标志是 ( )
2AB(g)达到平衡的标志是 ( )
A.单位时间生成nmolA2同时生成n mol AB
B.容器内总压强不随时间变化
C.单位时间生成2n mol AB同时生成n mol B2
D.单位时间生成n molA2同时生成n molB2
9.若溶液中由水电离产生的c(OH-)=1×10-14 mol·L-1,满足此条件的溶液中一定能大量共存的离子组是: ( )
A.Al3+ Na+ NO3- Cl- B.K+ Na+ Cl- NO3-
C.K+ Na+ Cl- HCO3- D.K+ Fe2+ SO42- NO3-
8.向浅绿色的Fe(NO3)2溶液中逐滴加入稀盐酸,溶液的颜色变化应该是 ( )
A.变黄色 B.变为深绿色 C.没有变化 D.颜色变浅
7.下列操作错误的是 ( )
A.滴定管用水清洗后,再用所盛试液润洗
B.用25mL酸式滴定管量取12.00mL稀盐酸
C.把KMnO4溶液注入酸式滴定管中
D.操作中眼睛注视滴定管内液面的变化
6.等体积的下列溶液,阴离子的总浓度最大的是 ( )
A.10mL 0.1mol/L的Ba(OH)2溶液 B.30mL 0.2mol/L的CH3COONa溶液
C.20mL 0.2mol/L的K2S溶液 D.40mL 0.2mol/L的(NH4)2SO4溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com