
9.下列说法正确的是 ( )
A.1L O2的质量一定比1L Cl2的质量小
B.1.8g H2O所含电子数为0.1NA
C.等质量的NO2和N2O4所含原子数一定相等
D.等体积、等物质的量浓度的强酸溶液中所含的H+离子数一定相等
29.(17分)某有机物X(C12H13O6Br)遇到FeCl3溶液显紫色,其部分结构简式如下:
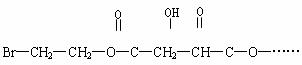
已知:X在足量的氢氧化钠水溶液中加热,可得到A、B、C三种有机物:
①C中苯环上只有一种氢原子
②室温下A经盐酸酸化可得到苹果酸E,E的结构简式为 HOOC-CH2-CH-COOH
请回答:
(1)E中含有的官能团是 ;
(2)C经酸化可得到有机物G,G 的结构简式为 ;G可以发生的反应类型有 (填序号) ①加成反应;②消去反应;③氧化反应;④取代反应。
(3)B的结构简式为 ;
(4)E的一种同分异构体F有如下特点:1molF可以和3mol金属钠发生反应,放出33.6LH2(标况下),1molF可以和足量NaHCO3溶液反应,生成1molCO2,1molF还可以发生银镜反应,生成2molAg。则F的结构简式可能是(只写一种)
(5)在一定条件下两分子E可生成六元环酯,写出此反应的化学方程式
28.(16分)某校化学课外活动小组利用下图装置制备氯化铝固体,并用该固体配制氯化铝溶液。装置中a为长玻璃导管,b为玻璃活塞。实验中可供选用的试剂有:①二氧化锰固体;②铝粉;③氯化钠固体;④浓硫酸;⑤浓盐酸;⑥蒸馏水;⑦碱石灰。资料表明:氯化铝受热至180℃时即升华,在潮湿的空气中易水解。
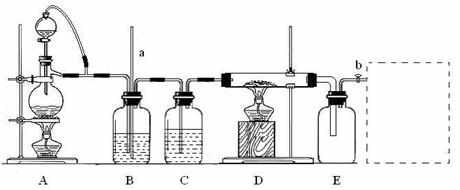
回答下列问题:
(1)检查该装置气密性的方法是____________。(2)A中气体制备的离子方程式是______。
(3)实验中B装置的作用是_____________。(4)D、E间导管短且粗,原因是________。
(5)用实验制得的氯化铝固体配制溶液的方法是_______________________。
(6)请将E后的虚线框中装置补充完善______(画在横线上)。该装置中应盛放的试剂是______(从题中可供试剂中选择,填序号)。作用是_____________________。
27.(11分)某无色溶液中可能有Na+、K+、SO32-、HS-、HCO3-、Cl-、AlO2-、Br-、Ba2+、Cu2+ 等离子中的若干种,依次进行下列实验,现象如下:
① 用PH试纸检验,溶液的PH值>7;
② 向溶液中滴加氯水,滴加过程中一直无气体、沉淀产生,再加入CCl4振荡,静置,CCl4层显橙色,后用分液漏斗分液;
③ 向分液后所得的水溶液中加入Ba(NO3)2和HNO3混合溶液,除有白色沉淀生成外无其它变化,然后过滤;
④ 向滤液中加入AgNO3和HNO3混合溶液,有白色沉淀产生。
请回答下列问题:
(1)原溶液中肯定存在的离子有_______;
(2)肯定不存在的离子是_____________;
(3)步骤②中发生的反应的离子方程式是: 。
26.(16分)A、B、C、D为原子序数依次增大的四种短周期元素,A、D同主族,B、C同周期。它们中的两种元素可形成多种原子个数比为1﹕1的化合物,甲、乙、丙、丁为其中的四种,它们的元素组成如下表:
|
化合物 |
甲 |
乙 |
丙 |
丁 |
|
元素种类 |
A、B |
A、C |
A、D |
C、D |
通常情况下,甲为气体,密度比空气略小;乙为液体;丙和丁为固体且均为离子化合物。请填写下列空白:
(1)D元素的原子结构示意图为 ,乙的电子式为 ,丁中阴离子与阳离子的个数比为 ;
(2)已知在标准状况下,5.6L的甲完全燃烧放出的热量为325 KJ,试写出表示甲的燃烧热的热化学方程式 ;
(3)研究表明,乙是一种二元弱酸,请写出乙在水中的电离方程式 ;
(4)已知丙的晶体结构与NaCl相似,则该晶体中与D离子距离最近的D离子有 个;
(5)写出由丁制备C元素形成的单质的化学方程式(任写一个)并标出电子转移 ;
13. CuS与一定浓度的HNO3反应,生成CuSO4、NO、NO2和H2O,当生成等物质的量的NO和NO2时,实际参加反应的CuS与HNO3的物质的量之比为
A.1:5 B.1:4 C.1:2 D.2:9
第Ⅱ卷(非选择题 174分)
12.如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是
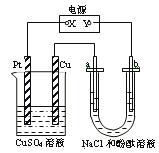
A.x是正极,y是负极,CuSO4溶液的pH逐渐减小
B.x是正极,y是负极,CuSO4溶液的pH保持不变
C.x是负极,y是正极,CuSO4溶液的pH 逐渐减小
D.x是负极,y是正极,CuSO4溶液的pH保持不变
11.对于平衡体系mA(g)+nB(g) pC(g)+qD(g);△H<0。下列结论中不正确的是
pC(g)+qD(g);△H<0。下列结论中不正确的是
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B.若平衡时,A、B 的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
C.若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol
D.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
10.某溶液中有Cl-、SO42-、OH-三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依次检验出来,下列实验操作顺序正确的是
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.③②④②① B.④②①②③ C.①②③②④ D.④②③②①
9.下列有关实验的说法不正确的是
A.淀粉胶体中混有氯化钠杂质,可用半透膜做渗析实验提纯
B.用已被蒸馏水润湿的PH试纸测定未知液的PH时,一定会有误差
C.不用其它试剂即可鉴别稀盐酸和碳酸钠两种无色溶液
D.仅用溴水即可鉴别己烯、苯和四氯化碳
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com