
7ЃЎФГжїзхдЊЫиRЕФзюИпе§МлгызюЕЭИКЛЏКЯМлЕФДњЪ§КЭЮЊ4ЃЌгЩДЫПЩвдХаЖЯЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎRвЛЖЈЪЧЕкЫФжмЦкдЊЫиЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁ BЃЎRвЛЖЈЪЧIVAзхдЊЫи
ЁЁЁЁЁЁ CЃЎRЕФЦјЬЌЧтЛЏЮяБШЭЌжмЦкЦфЫћдЊЫиЦјЬЌЧтЛЏЮяЮШЖЈ
ЁЁЁЁЁЁ DЃЎRЦјЬЌЧтЛЏЮяЛЏбЇЪНЮЊH2R
6ЃЎФГдЊЫидСЫЕФКЫЕчКЩЪ§ЪЧЕчзгВуЪ§ЕФ5БЖЃЌЦфжЪзгЪ§ЪЧзюЭтВуЕчзгЪ§ЕФ3БЖЃЌИУдЊЫиЕФКЫЕчКЩЪ§ЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎ11ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ15ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ17ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ34
5ЃЎЯТСаЙигкNaКЭNa+ЕФа№ЪіжаЃЌДэЮѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЫќУЧЯрВювЛИіЕчзгВуЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЫќУЧЕФЛЏбЇаджЪЯрЫЦ
ЁЁЁЁЁЁ CЃЎФЦдзгЃЌФЦРызгОљЮЊЭЌвЛдЊЫиЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎзЦЩеЪБЃЌЫќУЧЕФбцЩЋЗДгІЖМГЪЛЦЩЋ
4ЃЎЮяжЪбѕЛЏадЁЂЛЙдадЕФЧПШѕЃЌВЛНігыЮяжЪЕФНсЙЙгаЙиЃЌЛЙгыЮяжЪЕФХЈЖШКЭЗДгІЮТЖШЕШгаЙиЁЃЯТСаИїзщЮяжЪЃКЂйCuгыHNO3ШмвКЁЁ ЂкCuгыFeCl3ШмвКЁЁ ЂлZnгыH2SO4ШмвКЁЁ ЂмFeгыHClШмвКгЩгкХЈЖШВЛЭЌЖјФмЗЂЩњВЛЭЌбѕЛЏЛЙдЗДгІЕФЪЧЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЂйЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂлЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂйЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂйЂлЂм
3ЃЎЗжРрЪЧбЇЯАКЭбаОПЛЏбЇЕФвЛжжГЃгУЕФПЦбЇЗНЗЈЁЃЯТСаЗжРрКЯРэЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ ЂйИљОнЫсЗжзгжаКЌгаHдзгИіЪ§НЋЫсЗжЮЊвЛдЊЫсЁЂЖўдЊЫсЕШ
ЁЁЁЁЁЁ ЂкИљОнЗДгІжаЪЧЗёгаЕчзгЕФзЊвЦНЋЛЏбЇЗДгІЗжЮЊбѕЛЏЛЙдЗДгІКЭЗЧбѕЛЏЛЙдЗДгІ
ЁЁЁЁЁЁ ЂлИљОнЕчНтжЪдкШлШкзДЬЌЯТФмЗёЭъШЋЕчРыНЋЕчНтжЪЗжЮЊЧПЕчНтжЪКЭШѕЕчНтжЪ
ЁЁЁЁЁЁ ЂмИљОндЊЫидзгзюЭтВуЕчзгЪ§ЕФЖрЩйНЋдЊЫиЗжЮЊН№ЪєКЭЗЧН№Ъє
ЁЁЁЁЁЁ ЂнИљОнЗДгІЕФШШаЇгІНЋЛЏбЇЗДгІЗжЮЊЗХШШЗДгІКЭЮќШШЗДгІ
ЁЁЁЁЁЁ AЃЎЂкЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂкЂнЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂйЂкЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂкЂлЂмЂн
2ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎашМгШШВХФмНјааЕФЗДгІвЛЖЈЪЧЮќШШЗДгІ
ЁЁЁЁЁЁ BЃЎУКЕФИЩСѓЁЂЪЏгЭЕФЗжСѓЖМЪєгкЛЏбЇБфЛЏ
ЁЁЁЁЁЁ CЃЎFe(OH)3НКЬхКЭMgCl2ШмвКЙВЭЌОпБИЕФаджЪжЎвЛЪЧЗжЩЂжЪЮЂСЃПЩЭЈЙ§ТЫжН
ЁЁЁЁЁЁ DЃЎКЌгаН№ЪєдЊЫиЕФРызгвЛЖЈЖМЪЧбєРызгЃЛжЛКЌгаЗЧН№ЪєдЊЫиЕФРызгвЛЖЈЪЧвѕРызг
1ЃЎЯТСаа№Ъіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎбѕЛЏМСдкЗДгІжаЪЇШЅЕчзгЃЌЛЙдМСдкЗДгІжаЗЂЩњЛЙдЗДгІ
ЁЁЁЁЁЁ BЃЎФГдЊЫидкЛЏбЇЗДгІжагЩЛЏКЯЬЌБфЮЊгЮРыЬЌЃЌдђИУдЊЫиМШПЩФмБЛбѕЛЏвВПЩФмБЛЛЙд
ЁЁЁЁЁЁ CЃЎгаЕЅжЪВЮМгЕФЗДгІвЛЖЈЪЧбѕЛЏЛЙдЗДгІ
ЁЁЁЁЁЁ DЃЎЬМЫсЧтФЦПЩгУгкжЮСЦЮИЫсЙ§ЖрЃЌЕтбЮжаЕФЕтПЩвджБНггУЕэЗлМьбщ
25ЃЎ(10Зж)ШчЭМЫљЪОЃЌPЮЊвЛПЩздгЩЛЌЖЏЕФЛюШћЃЌЙиБеKЃЌЗжБ№ЯђШнЦїAЁЂBжаИїГфШы2mol XЁЂ2molYЃЌЦ№ЪМЪБЃЌVA=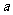 LЃЌVB=0.8
LЃЌVB=0.8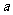 L(СЌЭЈЙмЕФЬхЛ§КіТдВЛМЦ)ЃЌдкЯрЭЌЮТЖШКЭДпЛЏМСДцдкЕФЬѕМўЯТЃЌСНШнЦїжаИїздОљЗЂЩњЯТЪіЗДгІЃК
L(СЌЭЈЙмЕФЬхЛ§КіТдВЛМЦ)ЃЌдкЯрЭЌЮТЖШКЭДпЛЏМСДцдкЕФЬѕМўЯТЃЌСНШнЦїжаИїздОљЗЂЩњЯТЪіЗДгІЃК
3X(g)+3Y(g) 2Z(g)+2W(g)ЃЌДяЕНЦНКтЪБЃЌVB=0ЃЎ6
2Z(g)+2W(g)ЃЌДяЕНЦНКтЪБЃЌVB=0ЃЎ6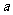 LЁЃ
LЁЃ
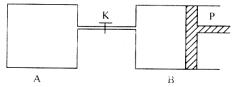
(1)BжаXЕФзЊЛЏТЪЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)AЁЂBжаXЕФзЊЛЏТЪЕФЙиЯЕЪЧAЁЁЁЁ B(ЬюЁА>ЁБЁА=ЁБЛђЁА<ЁБ)ЃЌЦфРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ЦНКтЪБAЁЂBжаЛьКѓЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЕФЙиЯЕЪЧЃКMA ЁЁЁЁЁЁMB(ЬюЁА>ЁБЁА=ЁБЛђЁА<ЁБ)
(4)ДђПЊKЃЌвЛЖЮЪБМфКѓЗДгІдйДЮДяЕНЦНКтЃЌШчЙћвЊМЦЫуГіДЫЪБBШнЦїжаЛьКЯЦјЬхЕФУмЖШЁЃдђжСЩйЛЙашвЊжЊЕРвдЯТЪ§ОнзщКЯжаЕФ ЁЁЁЁЁЁЁЁзщ(ЬюбЁЯюзжФИ)ЁЃ(ЩшMXЁЂMYЁЂMZЁЂMWЗжБ№БэЪОXЁЂYЁЂZЁЂWЕФФІЖћжЪСП)
AЃЎMzКЭMwЁЁЁЁ ЁЁ BЃЎMXКЭMYЁЁЁЁ ЁЁ CЃЎMxКЭMzЁЁЁЁ ЁЁ DЃЎMYКЭMW
аДГіЦфУмЖШЕФвЛжжБэДяЪНЃКЁЁЁЁЁЁЁЁ
gЁЄL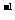 ЁЃ
ЁЃ
24ЃЎ(8Зж)бЧЯѕЫсбЮЙуЗКДцдкгкздШЛЛЗОГжаЃЌШчЪпВЫЁЂШтРрЁЂЖЙРрЕШЖМПЩвдВтГівЛЖЈСПЕФбЧЯѕЫсбЮЃЌвЛАуЧщПіЯТЃЌЕБШЫЬхвЛДЮадЩуШЁЕУ300-500 mgбЧЯѕЫсФЦЪБЃЌОЭЛсв§Ц№жаЖОЁЃФГбаОПадбЇЯАаЁзщгУЕтСПЗЈВтЖЈХнВЫжабЧЯѕЫсбЮЕФКЌСПЃЌЗДгІЗНГЬЪНШчЯТЃКЁЁЁЁ 2NaNO2+2H2SO4+2KI==2NO+I2+K2SO4+Na2SO4+2H2OЃЌ2Na2S2O3+I2==Na2S4O6+2NaIЁЃШЁl kgХнВЫеЅжЃЌНЋеЅГіЕФвКЬхЪеМЏКѓЃЌМгШыЬсШЁМСКЭЧтбѕЛЏФЦЃЌЪЙЕУЕНЕФХнВЫжжаЕФбЧЯѕЫсбЮЖМГЩЮЊбЧЯѕЫсФЦЃЌдкЙ§ТЫКѓЕФТЫвКжаМгШыЧтбѕЛЏТСШщвКЃЌвдГ§ШЅЩЋЫиЃЌдйДЮЙ§ТЫКѓЕУЕНТЫвКЃЌНЋИУТЫвКЯЁЪЭжС1LЃЌШЁ25.00 mLВЫжгыЙ§СПЕФЯЁСђЫсКЭЕтЛЏМиШмвКЕФЛьКЯвКЗДгІЃЌдйбЁгУКЯЪЪЕФжИЪОМСЃЌгУНЯЯЁЕФСђДњСђЫсФЦШмвКНјааЕЮЖЈЃЌЙВЯћКФ0.050 molЁЄL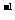 Na2S2O3ШмвК20.00 mLЁЃЧыЛиД№ЯТСаЮЪЬтЃК
Na2S2O3ШмвК20.00 mLЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЁЁЁЁ (1)ИУЪЕбщжаПЩбЁгУЕФжИЪОМСЪЧ ЁЁЁЁЁЁЁЁЁЃ
ЁЁЁЁ (2)ЭЈЙ§МЦЫуХаЖЯШєФГШЫвЛДЮЪГШы0.125 kgетжжХнВЫЃЌЪЧЗёЛсв§Ц№жаЖО?
ЁЁЁЁ (3)гаОбщЕФГјЪІдкзіХнВЫЪБЭљЭљМгШыЪЪСПЕФГШжЃЌвдМѕЧсбЧЯѕЫсбЮЕФЮЃКІЃЌжївЊЪЧвђЮЊГШжжаКЌгаЗсИЛЕФЮЌЩњЫиCЃЌЫЕУїЮЌЩњЫиCОпга ЁЁЁЁЁЁЁЁадЁЃ
23ЃЎ(10Зж)ЛЏКЯЮяAЪЧЪЏгЭЛЏЙЄЕФвЛжжживЊдСЯЃЌгУAКЭЫЎУКЦјЮЊдСЯОЭМЫљЪОЭООЖКЯГЩЛЏКЯЮяD(ЗжзгЪНЮЊC3H6O3)ЁЃ
ЁЁЁЁ 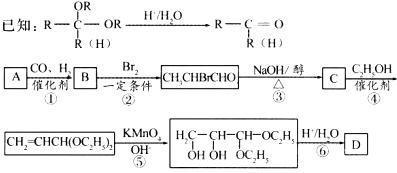
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)аДГіЯТСаЮяжЪЕФНсЙЙМђЪНЃКAЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛBЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЃЛCЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛDЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)жИГіЗДгІЂкЕФЗДгІРраЭЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)аДГіЗДгІЂлЕФЛЏбЇЗНГЬЪНЃКЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(4)ЗДгІЂмЕФФПЕФЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(5)ЛЏКЯЮяDЁфЪЧDЕФвЛжжЭЌЗжвьЙЙЬхЃЌЫќзюдчЗЂЯжгкЫсХЃФЬжаЃЌЪЧШЫЬхФкЬЧРрДњаЛЕФжаМфВњЮяЁЃDЁфдкХЈСђЫсДцдкЕФЬѕМўЯТМгШШЃЌМШПЩвдЩњГЩФмЪЙфхЫЎЭЪЩЋЕФЛЏКЯЮяE(C3H4O2)ЃЌгжПЩвдЩњГЩСљдзгЛЗзДЛЏКЯЮяF(C6H8O4)ЁЃЧыЗжБ№аДГіDЁфЩњГЩEКЭFЕФЛЏбЇЗНГЬЪНЃК
DЁфЁњEЃКЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
DЁфЁњFЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com