
13.据联合国世界卫生组织调查,当今缺铁性贫血是世界上最流行的营养性问题。我国 缺铁性贫血发生率达到15%至20%,为此2004年10月9日卫生部启动和推广铁强化酱油计划,以预防缺铁性贫血。所谓铁强化酱油即在普通酱油中加入无铁腥味、极易被人体吸收的添加剂--EDTAFeNa(化学名:乙二胺四乙酸铁钠,通常带三个结晶水,分子式为:C10H12FeN2NaO8·3H2O),其中EDTAFe是一种络合铁,EDTAFe-Na的结构式为:
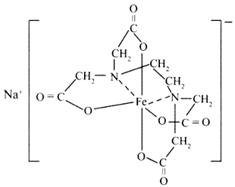
EDTA的结构简式为:(HOOCCH2)2NCH2CH2N(CH2COOH)2,下列说法正确的是
A.EDTAFeNa中铁为+2价 B.EDTAFeNa中铁为+3价
C.EDTA属于有机物 D.人体血液中血红蛋白中铁为+3价
12.X、Y两种元素均为短周期元素,X元素的原子所具有的电子层数为其最外层电子数的二分之一。下列有关判断中,正确的是
A.X元素在周期表中的位置只能是第二周期第ⅣA族
B.若X的常见简单阴离子X 能跟Y的单质发生氧化还原反应,则说明Y的非金属性比X的强
能跟Y的单质发生氧化还原反应,则说明Y的非金属性比X的强
C.若Y的非金属性比X的强,则与同一种还原剂反应时,一个Y原子得到的电子数一定比一个X原子得到的电子数少
D.若X能形成XO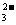 、XO
、XO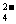 和X2O
和X2O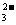 ,Y能形成YO
,Y能形成YO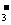 和XO
和XO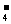 ,则X、Y一定在同一周期
,则X、Y一定在同一周期
11.下列实验中,仪器的下端必须插入液面下的是
①制备氢气的简易装置中的长颈漏斗 ③制备氯气装置中的分液漏斗
③制备Fe(OH)2操作中的胶头滴管 ④将氯化氢气体溶于水时的导管
⑤用乙醇制取乙烯时的温度计 ⑥分馏石油时的温度计
A.①③④⑤ B.②④⑥ C.①③⑤ D.全部
10.下列反应的离子方程式正确的是
A.铜片插入氯化铁溶液中 Cu+2Fe3+==Cu2++2Fe2+
B.电解饱和食盐水 2Cl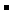 +2H+
+2H+ H2↑+Cl2↑
H2↑+Cl2↑
C.向溴化亚铁溶液中通人过量的氯气 2Fe2++Cl2==2Fe3++2Cl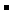
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加足量Ba(OH)2溶液 NH4++Al3++2SO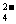 +2Ba2++5OH
+2Ba2++5OH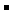 ==AlO
==AlO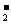 +2BaSO4↓+NH3·H2O+2H2O
+2BaSO4↓+NH3·H2O+2H2O
9.下列可用氢键来解释的是
A.浓的氢氟酸溶液中存在HF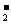 和H2F
和H2F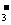
B.SiH4沸点比CH4高
C.水和乙醇分别与金属钠反应,前者比后者剧烈
D.H2O比H2S稳定,前者1000℃以上才分解,后者300℃分解
8.下列各组离子在所给的条件下能够大量共存的是
A.在Ph=0的溶液中:Fe2+、Mg2+、SO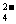 、NO
、NO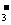
B.由水电离出的c(H+)=1×10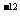 mol/L的溶液中:HCO
mol/L的溶液中:HCO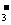 、K+、Na+、S2一
、K+、Na+、S2一
C.在AlCl3溶液中:SO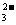 、Na+、CO
、Na+、CO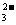 、AlO
、AlO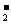
D.在滴加酚酞试液后呈红色的溶液中:I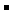 、AlO
、AlO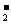 、Na+、S
、Na+、S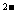
7.一定温度下,氢氧化镁饱和溶液中存在如下关系:c(Mg2+)·[c(OH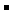 )]2=KSP,其中KSP为常数,称为该温度下Mg(OH)2的溶度积常数。试推断氢氧化镁在下列物质中的溶解度由大到小的顺序是
)]2=KSP,其中KSP为常数,称为该温度下Mg(OH)2的溶度积常数。试推断氢氧化镁在下列物质中的溶解度由大到小的顺序是
①0.1mol·L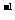 AlCl3溶液 ②0.1mol·L
AlCl3溶液 ②0.1mol·L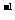 NH4C1溶液
NH4C1溶液
③0.1mol·L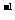 KCl溶液 ④0.1mol·L
KCl溶液 ④0.1mol·L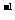 KAlO2溶液
KAlO2溶液
A.①④③② B.①②③④ C.③①④② D.④①③②
6.2005年10月12日我国成功发射了第二艘载人航天飞船--“神舟六号”,实现了双人多天太空旅行,这标志着中国人的太空时代又向前迈进了一大步。发射“神六”时用肼 (N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。
已知:N2(g)+2O2(g)==2NO2(g);△H=+67.7kJ/mol
N2H4(g)+O2(g)==N2(g)+2H2O(g);△H=-534kJ/tool
下列关于肼和NO2反应的热化学方程式中,正确的是
A.2N2H4(g)+2NO2(g)==3N2(g)+4H2O(1);AH=-1135.7kJ/mol
B.2N2H4(g)+2NO2(g)==3N2(g)+4H2O(g);△H=-1000.3kJ/mol
C.N2H4(g)+NO2(g)==3/2N2(g)+2H2O(1);△H=-1135.7kJ/mol
D.2N2H4(g)+2NO2(g)==3N2(g)+4H2O(g);△H=-1135.7kJ/mol
5.关于图中各装置图的叙述错误的是
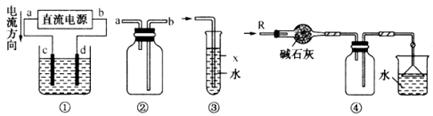
A.装置①中,c为阳极,d为阴极
B.装置②可用于收集H2、NH3、Cl2、HCl、NO2
C.装置③中X为苯,可用于吸收氨气或氯化氢
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
4.下列说法正确的是
A.不用其他试剂无法鉴别下列四种溶液:Na2CO3、Al2(SO4)3、NaCl、NaHSO4,
B.可以用分液漏斗分离下列三组液态混合物:硝基苯和水、油酸和水、乙酸乙酯和乙醇
C.实验室保存少量液溴和白磷常用水封
D.浓碱溶液沾到了皮肤上要立即用盐酸冲洗
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com