
1ĢŪ2007ÄęÅĩąīķûŧŊŅ§―ąĘÚÓčĩÂđúŧŊŅ§žŌGerhard ErtlĢŽŌÔąíÕÃËûķÔđĖĖåąíÃæŧŊŅ§ŅÐūŋđýģĖÖÐĩÄÖØīó·ĒÏÖĄĢĘđCOĄĒNOxĩČÔÚēŽąíÃæ·ĒÉúŧŊŅ§·īÓĶŨŠąäģÉÎÞķūÆøĖåĢŽŌÔžõÉŲÆûģĩÎēÆøÖÐÓÐķūÆøĖåĩÄÅÅ·ÅĢŽÕýĘĮīËÏîŅÐūŋĩÄÖØŌŠÓĶÓÃÖŪŌŧĄĢÏÂÁÐÓÐđØËĩ·ĻēŧÕýČ·ĩÄĘĮĄĄ (ĄĄĄĄ )

AĢŪCOÔÚēŽąíÃæąŧŅõŧŊÉúģÉCO2ĢŽēŽÆðīßŧŊŨũÓÃ
BĢŪÆûģĩÎēÆøÖÐNOxÔÚēŽąíÃæ·ĒÉú·īÓĶĩÄēúÎïĘĮN2
CĢŪCOÔÚēŽąíÃæŋÉÄÜšÍO2ĄĒNOx·īÓĶ
DĢŪNOxĄĒCOĄĒCO2ūųÄÜÓëČËĖåÖÐĩÄŅŠšėĩ°°Ũ―ášÏ
20ĄĒ(8·Ö)ĘĩŅéĘŌĀïģĢÓÃÅĻŅÎËáÓëķþŅõŧŊÃĖ·īÓĶĀīÖÆČĄÉŲÁŋĩÄÂČÆøĢŽ·īÓĶĩÄŧŊŅ§·―ģĖĘ―ÎŠĢš
MnO2+4HCl(ÅĻ) MnCl2+
Cl2Ąü+2H2OĄĢČôēúÉúĩÄÂČÆøÔÚąęŋöÏÂĩÄĖåŧýΊ11.2LĢŽĘÔžÆËãĢš
MnCl2+
Cl2Ąü+2H2OĄĢČôēúÉúĩÄÂČÆøÔÚąęŋöÏÂĩÄĖåŧýΊ11.2LĢŽĘÔžÆËãĢš
ĒŲēΞӷīÓĶĩÄMnO2ĩÄÖĘÁŋĘĮķāÉŲĢŋ
ĒÚ·īÓĶÖÐąŧŅõŧŊĩÄHClĩÄÎïÖĘĩÄÁŋĘĮķāÉŲĢŋ
19ĄĒ(6·Ö)ĘĩŅéĘŌÓÃÃÜķČΊ1.84g.cm-3ĢŽČÜÖĘĩÄÖĘÁŋ·ÖĘýΊ98%ĩÄÁōËáĢŽÅäÖÆ250mLÎïÖĘĩÄÁŋÅĻķČΊ0.46mol/LĩÄÁōËáĄĢ
(1)ÏÖÓÐÏÂÁОļÖÖđæļņĩÄÁŋÍēĢŽÁŋČĄÖĘÁŋ·ÖĘýΊ98%ĩÄÁōËáÓĶŅĄÓÃĄĄĄĄĄĄ (ĖîÐōšÅ)
ĒŲ10mLÁŋÍēĄĄ ĒÚ50 mLÁŋÍēĄĄ ĒÛ100mLÁŋÍēĄĄ
(2)ÍęģÉļÃĘĩŅéÐčŌŠĩÄŌĮÆũģýÁŋÍēĄĒÉÕąĄĒēĢÁ§°ôÍâĢŽŧđÐčŌŠĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĄĢ
(3)ÏÂÁÐēŲŨũĘđËųÅäČÜŌšĩÄÎïÖĘĩÄÁŋÅĻķČÆŦļßĩÄĘĮĄĄĄĄĄĄĄĄĄĄ
AĢŪÍųČÝÁŋÆŋÖÐŨŠŌÆČÜŌšĘąĢŽÓÐÉŲÁŋŌšĖå―ĶģöĄĢ
BĢŪÎīÏīĩÓÏĄĘÍÅĻH2SO4ĩÄÐĄÉÕąĄĢ
CĢŪķĻČÝĘąļĐĘÓŋĖķČÏߥĢ
DĢŪÏīūŧČÝÁŋÆŋÎīļÉÔïžīÓÃĀīÅäÖÆČÜŌš
EĢŪķĻČÝšóČûÉÏÆŋČû·īļīŌĄÔČĢŽūēÖÚóĢŽŌšÃæēŧĩ―ŋĖķČÏßĢŽÔŲžÓËŪÖÁŋĖķČÏߥĢ
18ĄĒ(6·Ö)ÄģÎÞÉŦÍļÃũČÜŌšÖÐŋÉÄÜīóÁŋīæÔÚAg+ĄĒMg2+ĄĒFe3+ÖÐĩÄžļÖÖĀëŨÓĄĢ
(1)ēŧŨöČΚÎĘĩŅéūÍŋÉŌÔŋÏķĻÔČÜŌšÖÐēŧīæÔÚĩÄĀëŨÓĘĮĄĄĄĄĄĄ ĄĢ
(2)ČĄÉŲÁŋÔČÜŌšžÓČëđýÁŋÏĄŅÎËáĢŽÓаŨÉŦģÁĩíÉúģÉĢŽÔŲžÓČëđýÁŋÏĄÏõËáĢŽ°ŨÉŦģÁĩíēŧÏûʧĢŽËĩÃũÔČÜŌšÖÐŋÏķĻÓÐĩÄĀëŨÓĄĄĄĄĄĄ ĢŽĄĄ ÓÐđØĩÄĀëŨÓ·īÓĶĘ―ÎŠĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĄĢ
(3)ČĄ(2)ĩÄÂËŌšžÓČëđýÁŋNaOHČÜŌšĢŽģöÏÖ°ŨÉŦģÁĩíĢŽËĩÃũÔČÜŌšÖÐŋÏķĻīæÔÚĩÄĀëŨÓÓÐĄĄĄĄĄĄĄĄ ĄĢ
(4)ÔČÜŌšÖÐŋÉÄÜīóÁŋīæÔÚĩÄŌõĀëŨÓĘĮÏÂÁÐA-DÖÐĩÄ(ĖîÐōšÅ)ĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĄĢ
AĢŪClĢ ĄĄĄĄĄĄĄĄĄĄĄĄĄĄBĢŪNO3ĢĄĄĄĄĄĄĄĄ CĢŪCO32ĢĄĄĄĄĄĄĄĄĄĄ DĢŪOHĢ
17ĄĒ(6·Ö)ÏÂÁÐļũŨéÎïÖĘĩÄ·ÖĀëŧōĖáīŋĢŽÓĶŅĄÓÃÏÂĘö·―·ĻĩÄÄÄŌŧÖÖĢŋ(ĖîÐōšÅ)
AĢŪ·ÖŌšĄĄ BĢŪđýÂË ĄĄCĢŪÝÍČĄĄĄ D ĢŪÕôÁóĄĄ E ĢŪÕô·Ē―áū§ĄĄ FĢŪžÓČČ·Ö―â
(1)ģýČĨCa(OH)2ČÜŌšÖÐÐüļĄĩÄCaCO3ĄĄĄĄĄĄĄĄ Ģŧ(2)īÓĩâËŪÖÐĖáČĄĩ⥥ĄĄĄĄĄĄĄĄĄĄĄĄ Ģŧ
(3)ÓÃŨÔĀīËŪÖÆČĄÕôÁóËŪĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĢŧĄĄ (4)·ÖĀëÖēÎïÓÍšÍËŪĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ Ģŧ
(5)ģýČĨNaClÖÐËųšŽĩÄÉŲÁŋKNO3ĄĄĄĄ ĢŧĄĄ (6)ģýČĨCaOÖÐÉŲÁŋĩÄCaCO3ĄĄĄĄĄĄĄĄĄĄĄĄĄĄ Ģŧ
16ĄĒ(1)(6·Ö)ÏÂÁзīÓĶÖÐĘĮĀëŨÓ·īÓĶĩÄÐīģöĀëŨÓ·―ģĖĘ―ĢŽ·ņÔōÐīŧŊŅ§·īÓĶ·―ģĖĘ―ĢŧĘĮŅõŧŊŧđÔ·īÓĶĩÄĢŽÓÃËŦÏßĮÅąęģöĩįŨÓŨŠŌÆĩÄ·―ÏōšÍĘýÄŋ
ĒŲŅÎËáÓëĖžËáļÆĩÄ·īÓĶ__________________________________
ĒÚÍžÓČëÏõËáŌøČÜŌšÖÐ_____________________________________
(2)(8·Ö)2molO3šÍ3molO2ĩÄÖĘÁŋĄĄĄĄ(ĖîÏāĩČĄĒēŧÏāĩČŧōÎÞ·ĻÅÐķÏ)Ģŧ·ÖŨÓĘýÖŪąČΊĄĄĄĄĄĄ ĢŧšŽÓÐŅõÔŨÓĩÄĘýÄŋÖŪąČΊĄĄĄĄ ĢŧÔÚÏāÍŽĖõžþÏÂÆøĖåĩÄĖåŧýąČΊĄĄĄĄĄĄ ĄĢ
15ĄĒļųūÝÏÂÁзīÓĶĢšĒŲ2H2S+O2 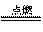 2S+2H2OĄĄ ĒÚ4NaI+O2+2H2OĢ―4NaOH+2I2ĄĄ ĒÛNa2S+I2Ģ―2NaI+SĄý.·īÓĶÖÐŅõŧŊžÁĩÄŅõŧŊÐÔÓÉĮŋĩ―ČõĩÄÅÅÁÐËģÐōÕýČ·ĩÄĘĮ(ĄĄ )
2S+2H2OĄĄ ĒÚ4NaI+O2+2H2OĢ―4NaOH+2I2ĄĄ ĒÛNa2S+I2Ģ―2NaI+SĄý.·īÓĶÖÐŅõŧŊžÁĩÄŅõŧŊÐÔÓÉĮŋĩ―ČõĩÄÅÅÁÐËģÐōÕýČ·ĩÄĘĮ(ĄĄ )
AĢŪSĢūI2ĢūO2ĄĄĄĄĄĄĄĄĄĄ ĄĄĄĄĄĄĄĄĄĄĄĄ BĢŪO2 ĢūSĢūI2 ĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ CĢŪO2 ĢūI2ĢūSĄĄĄĄ ĄĄĄĄĄĄ DĢŪI2ĢūO2 ĢūS
ĩÚĒōūí(·ĮŅĄÔņĖ⥥ đē40·Ö)
14ĄĒÉč°Ē·üžÓĩÂÂÞģĢĘýΊNAĢŽÏÂÁÐËĩ·ĻēŧÕýČ·ĩÄĘĮ(ĄĄ )
AĢŪ71gCl2ËųšŽĩÄÔŨÓĘýΊNAĄĄ
BĢŪ18gËŪÖÐËųšŽĩįŨÓĘýΊ10NA
CĢŪ46gNO2šÍ46gN2O4šŽÓÐĩÄÔŨÓĘýūųΊ3NA
DĢŪÔÚ1L2mol/LĩÄÏõËáÃūČÜŌšÖКŽÓÐĩÄÏõËáļųĀëŨÓĘýΊ4NA
13ĄĒČįÏÂÍžĢŽÔÚĘĒÓÐĩâËŪĩÄČýÖ§ĘÔđÜÖÐ·ÖąðžÓČëą―(ÃÜķČąČËŪÐĄĢŽēŧČÜÓÚËŪ)ĄĒËÄÂČŧŊĖžšÍūÆūŦĢŽÕņĩīšóūēÖÃĢŽģöÏÖÏÂÁÐÏÖÏóĢŽÕýČ·ĩÄ―áÂÛĘĮĄĄ (ĄĄ )
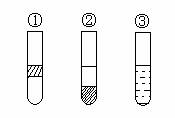
AĢŪĒŲžÓČëĩÄĘĮCCl4,ĒÚžÓą―ĢŽĒÛžÓūÆūŦ
BĢŪĒŲžÓČëĩÄĘĮūÆūŦ ĒÚ žÓCCl4,ĒÛžÓą―
CĢŪĒŲžÓČëĩÄĘĮą― ĒÚžÓCCl4 ĒÛžÓūÆūŦ
DĢŪĒŲžÓČëĩÄĘĮą― ĒÚ žÓūÆūŦ ĒÛžÓCCl4
12.ĄĒ1mol/LÁōËáĩÄšŽŌåĘĮĄĄ (ĄĄ )
AĢŪ1 LËŪÖКŽÓÐ1 mol ÁōËᥥĄĄĄĄĄĄĄĄĄĄĄĄ BĢŪ1 LČÜŌšÖКŽÓÐ1 mol H+
CĢŪ―Ŧ98ŋËÁōËáČÜÓÚ1LËŪÖÐËųÐÎģÉĩÄČÜŌšĄĄ ĄĄ DĢŪÖļ1LÁōËáČÜŌšÖКŽÓÐ98ŋËH2SO4
đúžĘŅ§ÐĢÓÅŅĄ - Á·Ï°ēáÁÐąí - ĘÔĖâÁÐąí
šþąąĘĄŧĨÁŠÍøÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻÆ―ĖĻ | ÍøÉÏÓКĶÐÅÏĒūŲąĻŨĻĮø | ĩįÐÅÕĐÆūŲąĻŨĻĮø | ÉæĀúĘ·ÐéÎÞÖũŌåÓКĶÐÅÏĒūŲąĻŨĻĮø | ÉæÆóĮÖČĻūŲąĻŨĻĮø
ÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻĩįŧ°Ģš027-86699610 ūŲąĻÓĘÏäĢš58377363@163.com