
20.下列离子方程式中正确的是 ( )
A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O
C.苯酚钠溶液中通入少量CO2: -O-+CO2+H2O→
-O-+CO2+H2O→ -OH+HCO3-
-OH+HCO3-
D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
第Ⅱ卷(非选择题,共50分)
19.下列实验操作中,先后顺序正确的是 ( )
A.稀释浓硫酸时,先在烧杯中加入一定体积的浓硫酸,后注入蒸馏水
B.为测定硫酸铜晶体的结晶水含量,称样时,先称取一定量的晶体,后放入坩埚
C.为检验酸性溶液中的Cl-和SO42-,先加硝酸银溶液,滤去沉淀后再加入硝酸钡溶液
D.在制取干燥纯净的氯气时,先使氯气通过饱和食盐水,后通过浓硫酸
18.配制一定溶质质量分数的NaOH溶液时,造成所配制溶液的溶质质量分数偏高的原因可能是 ( )
A.所用NaOH已潮解
B.用带游码的托盘天平称量NaOH固体质量时,误将砝码放在左盘,被称量物放在右盘
C.托盘天平的左右托盘上各放一张纸,调整天平至平衡后,将NaOH固体放在纸上称量
D.用量筒量取水时,俯视水面刻度线来读取体积
17.20℃时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1,则下列说法中不正确的是 ( )
A.25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1
B.此溶液中KCl的质量分数为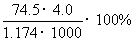
C.20℃时,密度小于1.174g·cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g·cm-3
16.某周期的IA族元素的原子序数为x,和它同周期的ⅢA族元素的原子序数可能是( )
①x+2 ②x+19 ③x+12 ④x+18 ⑤x+26 ⑥x+11
A.只有②④⑥ B.只有①③⑤ C.只有①② D.全部
15.下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
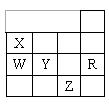
A.常压下五种元素的单质中Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物沸点比X的氢化物的沸点高
D.Y元素的非金属性比W元素的非金属性强
14.将NaCl和NaBr的混和物mg溶于足量的水配成500mL的溶液A,再向其中通入足量的氯气,充分反应后蒸发至干,得干燥晶体(m-2)g,则A溶液中Na+、Br-、Cl-的物质的量浓度之比不可能为 ( )
A.3︰2︰1 B.3︰1︰2 C.4︰3︰1 D.3︰1︰4
13.在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温、同压下相同体积的氧气时,三个反应中转移的电子数之比为 ( )
A.1︰1︰1 B.2︰2︰1 C.2︰3︰1 D.4︰3︰2
12.把NaHCO3和Na2CO3·10H2O混和物6.56g溶于水制成100mL溶液,其中C(Na+)=0.5mol/L。如果把6.56g这种混和物加热至恒重会失重多少克 ( )
A.2.65g B.3.56g C.3.91g D.4.65g
11.在V升Al2(SO4)3溶液中加入过量的氨水,过滤得沉淀,然后在高温下灼烧沉淀,最后得到白色固体mg,则原溶液中的SO42-的物质的量浓度(mol·L-1)为 ( )
A.m/27V B.2m/27V C.m/18V D.m/34V
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com