
28.(5)某同学做1L 0.1mol/L的澄清石灰水中慢慢通入足量标况下的二氧化碳气体实验。下面是他整理的部分实验报告。
(1)该实验过程中的化学方程式为: 。
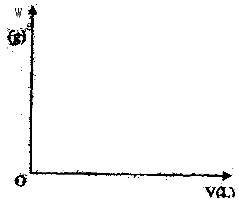
(2)该实验过程中产生沉淀的质量W(g)随通入标况下二氧化碳的体积V(L)而变化,可用图像直观地有达。请画出这一关系图像(请标明交点、折点数据)。
27.(6分)实验室要做验证氢氧化铝的两性实验。
(1)在实验前需配制100mL 2.0mol/L的NaOH溶液,请回答下列问题:
①下列仪器中,在上述配制实验中不使用的有 (填字母)
A、烧杯 B、200mL容量瓶 C、胶头滴管 D、玻璃棒 E、100mL容量瓶
②以上正确的操作顺序是 (填字母)。
A、冷却 B、称量 C、洗涤 D、定容 E、溶解 F、摇匀 G、转移
(2)实验时首先将NaOH溶液滴加到装有AlCl3溶液的试管中先看到有白色沉淀产生,并逐渐增多;再看到沉淀溶解并逐渐消失。请回答:
①产生白色沉淀的离子方程式 。
②白色沉淀消失的离子方程式 。
(3)在做完(2)中的溶液滴加的HCl溶液,开始几滴加入未见任何现象,再滴加则产生白色沉淀并逐渐增多,继续滴加白色沉淀溶解并逐渐消失。请回答:
①开始几滴为何无现象 。
②再滴加HCl溶液产生白色沉淀的离子方程式 。
26.(8分)为了验证木炭与浓H2SO4反应生成的混合气体中含有CO2和SO2两种气体,选用下图所示仪器(内含物质)组装成实验装置(每种仪器最多用两次):
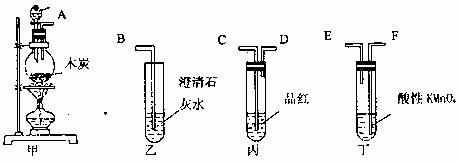
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母): 接C,D接 , 接C,D接 ;
(2)第一次接丙装置的作用是:
;
(3)第二次接丙装置的作用是:
;
(4)丁中酸性KMnO4溶液的作用是 ;
(5)写出甲中反应的化学方程式
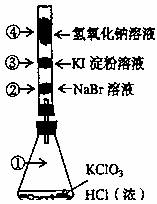
25.(4分)已知常温下氯酸钾与浓酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是 。
|
|
① |
② |
③ |
④ |
|
A |
黄绿色 |
橙色 |
蓝色 |
白色 |
|
B |
无色 |
橙色 |
紫色 |
白色 |
|
C |
黄绿色 |
橙色 |
蓝色 |
无色 |
|
D |
黄绿色 |
无色 |
紫色 |
白色 |
24.(4分)如何除去杂质,提纯下列各物质
|
混合物成分 |
提纯所用试剂的化学式 |
|
(1)FeCl2溶液中含少量FeCl3杂质 |
|
|
(2)FeCl3溶液中含少量FeCl2杂质 |
|
|
(3)FeSO4溶液中含少量CuSO4杂质 |
|
|
(2)NaHCO3溶液中含少量Na2CO3杂质 |
|
23.(7分)A是中学化学常见元素的单质,B、C、D、E是含A元素的常见化合物,它们之间可按下图转化(反应条件未标出)。
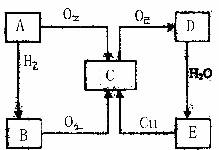
(1)A必定为 (填金属或非金属)。
(2)若A常温下为淡黄色固体,则试管壁上沾有A,应用 洗涤。浓的E溶液在常温下为粘稠的液体,且E具有强吸水性、强氧化性、强脱水性。则:E表现吸水性时,可做干燥剂,下列物质可用E干燥的是 (填字母序号)
A.氨气 B.硫化氢 C.氢气 D.二氧化硫
浓E溶液与铜反应时,E除了表现强氧化性外,还表现了 性。
(3)若A常温下为气体,则D物质的颜色为 ,写出B→C的化学反应方程式: 。
22.(3分)酸雨主要是燃烧含硫燃料时释放出SO2所造成的。现取一份雨水样品,每隔一定的时间测定其pH值,测定结果见附表:
附表:雨水样品pH值随时间的变化值
|
测试时间(/h) |
0 |
1 |
2 |
4 |
8 |
|
雨水样品pH值 |
4.73 |
4.62 |
4.56 |
4.55 |
4.55 |
试说明雨水样品pH值减小的原因
21.(6分)科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行探入的研究。下列各组物质中有一种物质与其它物质不属于同一类,请将其挑出来。
|
物质组 |
不属于同类的物质 |
|
(1)Mg、O2、I2、NO |
|
|
(2)NaOH、Na2CO3、CH4、CaO |
|
|
(3)HClO、H2SO4、NH3H2O、H2SiO3 |
|
|
(4)CO、SO2、CO2、SO3 |
|
|
(5)Ca(HCO3)2、Na2CO3、AgNO3、BaSO4 |
|
|
(6)水、液氯、氨水、水银 |
|
20.减少酸雨产生的途径可采用的措施是 ( )
①减少煤燃料的使用 ②把工厂烟囱造高
③煤燃料脱硫 ④在已酸化的土壤中加石灰
⑤开发新能源 ⑥对能被酸雨腐蚀的设施进行防腐处理
A.①②③④ B.①⑤ C.①③⑤ D.①②③④⑤⑥
19.关于氧化还原反应的下列是说法中正确的是 ( )
A.在氧化还原反应中,某元素由化合态变为单质,此元素一定被还原
B.在氧化还原反应中,可通过比较失去电子数的多少确定还原剂的强弱
C.在氧化还原反应中,非金属单质一定是氧化剂,金属单质一定是还原剂
D.化合物分解的产物中有单质生成,则该分解反应一定属于氧化还原反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com