
1.环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的。下列环境问题与所对应的物质不相关的是 ( )
A.温室效应--二氧化碳 B.光化学污染--二氧化氮
C.酸雨--二氧化碳 D.臭氧层破坏--氟氯烃
24.(17分)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y Z+W
Z+W
(1)Y的电子式是 _。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是 。
(3)用图示装置制备NO并验证其还原性。有下列主要操作:
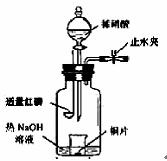
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①步骤c后还缺少的一步主要操作是 。
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是 。
③步骤c滴入稀硝酸后烧杯中的现象是 。反应的离子方程式是 。
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
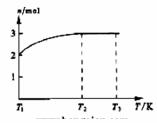
①温度在T1-T2之间,反应的化学方程式是 。
②温度在T2-T3之间,气体的平均相对分子质量是(保留1位小数) 。
23.(15分)在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是 ;X与碳元素形成的化合物的电子式是 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是 ;D与E能形成一种非极性分子,该分子的结构式为 ;D所在族元素的氢化物中,沸点最低的是 。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是 。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,写出其氢化物能用于刻蚀玻璃时主要反应方程式为 。
22.(14分)实验室制备少量硫酸亚铁晶体的实验步骤如下:
取废铁屑放入碳酸钠溶液中加热,用蒸馏水把铁屑冲洗干净,取过量洁净的铁屑,加入20%-30%的稀硫酸溶液,在50℃-80℃水浴中加热仍有少量铁屑。将该溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置,冷却时间后收集产品。
(1)废铁屑放入碳酸钠溶液中加热目的 。
(2)硫酸溶液过稀会导致 。
(3)采用水浴加热的原因是 。温室控制到50℃-80℃原因 。
(4)反应时铁屑过量的目的是(用离子方程式表示) 。
(5)溶液趁热时过滤的原因是 。
(6)静置冷却一段时间后,在试管中观察到的现象是 。
21.(14分)某无色溶液,其中有可能存在离子如下:Na+、Ba2+、Al3+、A1O2-、S2-、SO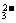 、SO
、SO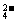 。现取该溶液进行有关实验,实验结果如下图所示。
。现取该溶液进行有关实验,实验结果如下图所示。

请回答下列问题:
(1)沉淀甲是 ;
(2)沉淀乙是 由溶液甲生成沉淀乙的离子方程式为:
;
(3)沉淀丙是 ;
(4)写出生成甲的离子方程式
(5)综合上述信息,可以肯定存在的离子 。
20.某固定体积的密闭容器中存在化学平衡:aA(g) bB(g)+cC(g),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是 ( )
A.若a=b+c时,B的物质的量分数变大
B.若a=b+c时,B的物质的量分数不变
C.若a>b+c时,A的转化率不变
D.若a<b+c时,A的转化率变小
第Ⅱ卷(非选择题,共60分)
19.把Ca(OH)2放入一定量的蒸馏水中,一定温度下达到平衡:Ca
(OH)2(s) Ca2++2OH-,当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是 ( )
A.溶液中Ca2+数不变 B.c(Ca2+)增大
C.溶液pH不变 D.溶液pH增大
18.有一种混合气体,它可能由CO、CO2、SO2、HC1中的一种或多种气体组成,该气体依次通过下列物质的现象如下:通过澄清石灰水无白色沉淀析出;通过品红溶液,溶液红色褪去;通过炽热的CuO,固体变为红色;通过澄清石灰水,出现白色沉淀,该混合气体组成的各种说法中,正确的是 ( )
A.肯定不含有CO2
B.只含有CO和 SO2
C.含有SO2、CO和CO2,可能含HC1
D.含HC1、SO2和CO,可能含CO2
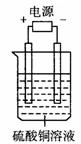
17.如图电解池中装有硫酸铜溶液,选用不同的、材料的电极进行电解。下列说法正确的是
( )
|
序号 |
电极材料 |
通电后的变化 |
|
|
阴极 |
阳极 |
||
|
A |
石墨 |
石墨 |
阴极质量增加,溶液的pH增大 |
|
B |
铜 |
铜 |
阳极质量减小,阴极质量增加 |
|
C |
铁 |
铁 |
两极的质量不发生变化 |
|
D |
铂 |
铁 |
阴极质量增加,溶液的pH不变 |
16.在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气。当制得同温、同压下相同体积的氧气时,三个反应中转移的电子数之比为 ( )
A.1:1:1 B.2:2:1 C.2:3:1 D.4:3:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com