
7.已知25℃时,AgI饱和溶液中c (Ag+)为1.22×10-8 mol/L,AgCl的饱和溶液中c (Ag+)为1.25×10-5 mol/L。若在5 mL含有KCl和KI各为0.01 mol/L的溶液中,加入8 mL0.01 mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
A.c(K+)>c(NO3-) >c(Cl-) >c(Ag+)>c(I-)
B.c(K+)>c(NO3-) >c(Ag+) >c(Cl-)>c(I-)
C.c(NO3-)>c(K+)>c(Ag+) >c(Cl-)>c(I-)
D.c(K+)>c(NO3-) >c(Ag+) = c(Cl-) + c(I-)
6.向盛有50mL 1.00mol·L-1HC1溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列叙述中不正确的是
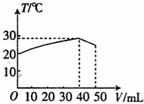
A.该实验表明化学能可以转化为热能
B.NaOH溶液的浓度大于1.00mol·L-1
C.V=50mL时,混合液的pH>7
D.该实验表明有水生成的反应都是放热反应
5.下列实验设计能够成功的是 ( )
A.检验亚硫酸钠试样是否变质:试样
 白色沉淀
白色沉淀 沉淀不溶解
沉淀不溶解
B.除去乙酸乙酯中混有的乙酸:混合液
 溶液分层
溶液分层 得上层液体
得上层液体
C.证明酸性条件下H2O2氧化性比I2强:NaI溶液
溶液变蓝色
D.鉴定盐A的成分是FeBr2:
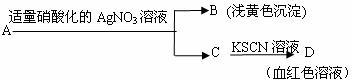
4.设NA表示阿伏加德罗常数的值,下列有关说法正确的是
A.常温常压下,1mol氦气含有2NA个原子
B.标准状况下,0.5NA个CCl4所占的体积约为11.2L
C.78g Na2O2 固体含有的阴离子数为NA
D.用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,阴极析出6.4g金属
3.化学反应N2+3H2=2NH3的能量变化如下图所示,该反应的热化学方程式是
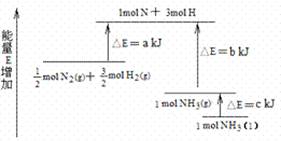
A.N2(g)+3H2(g)=2NH3(g);⊿H=2(b-a)kJ·mol-1
B.N2(g)+3H2(g)=2NH3(l);⊿H=2(a-b-c)kJ·mol-1
C.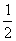 N2(g)+
N2(g)+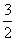 H2(g)=NH3(l);⊿H=(b+c-a)kJ·mol-1
H2(g)=NH3(l);⊿H=(b+c-a)kJ·mol-1
D.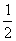 N2(g)+
N2(g)+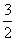 H2(g)=NH3(g);⊿H=(a+b)kJ·mol-1
H2(g)=NH3(g);⊿H=(a+b)kJ·mol-1
2.新华社2007年3 月21日电,全国科学技术名词审定委员会21日公布:111号元素(符号为Rg)的中文名称为“ 钅仑 ”。下列说法正确的是:
A.111号元素是第6周期、第ⅠA族的金属元素 B.111号元素属于过渡元素
C.111号元素为非金属元素 D.111号元素质量数为111
1.焰火“脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。下列说法中正确的是
A.非金属单质燃烧时火焰均为无色 B.所有金属及其化合物灼烧时火焰均有颜色
C.焰色反应均应透过蓝色钴玻璃观察 D.NaC1与Na2CO3灼烧时火焰颜色相同
23.(10分)数据分析能力是新课程中对学生提出的一项要求。下表是用沉淀法测定KHCO3和Na2CO3混合物的组成的相关数据。实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的Ba(OH)2溶液,每次实验均充分反应。实验记录见下表:
|
实验 次数 |
称取样品 的质量/g |
所加Ba(OH)2 溶液的体积/L |
测得生成 沉淀质量/g |
|
1 |
0.518 |
0.5 |
0.985 |
|
2 |
1.036 |
0.5 |
|
|
3 |
1.554 |
0.5 |
2,955 |
|
4 |
2.072 |
0.5 |
3.940 |
|
5 |
2.590 |
0.5 |
3.940 |
|
6 |
3.108 |
0.5 |
3.940 |
分析上表数据回答下列问题:
(1)第2次实验中产生沉淀质量是多少克,请将结果填在表格相应空格中;
(2)样品中KHCO3和Na2CO3的物质的量之比是 ;
(3)室温下,取上述Ba(OH)2溶液50mL,加入0.05moL/L的盐酸,反应后所得溶液的pH=2,求出所加盐酸的体积(溶液混合时不考虑体积变化,写出计算过程)。
22.(12分)某同学用废干电池内的黑色固体(可能含有MnO2、NH4Cl、ZnCl2等物。所示实验:
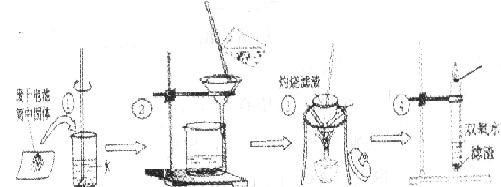
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、泥三角、三角架、 ;
(2)操作④的试管加入③中所得滤渣,试管中迅速产生能使带火星的木条复燃的气体,自此推测滤渣中含有MnO2,写出试管中发生反应的化学方程式: ; MnO2的作用是
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的黑色物质为
(4)已知氯化锌与稀氨水反应先生成Zn(OH)2白色沉淀,Zn(OH)2可以溶于稀氨水生成可溶性的Zn(NH3)4(OH)2:该同学设计如下实验探究②中所得滤液中的溶质
[探究1]滤液中含有氯化铵
[实验过程]
[实验现象]有刺激性气味气体逸出
写出该离子方程式
[探究2]滤液中含有氯化锌
[实验过程] [实验现象]
由上述现象得出结论:滤液中含有氯化锌和氯化铵。
21.(11分)有机物A的结构简式为: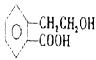 它可通过不同化学反应分别制得B、C、D和E四种物质。
它可通过不同化学反应分别制得B、C、D和E四种物质。
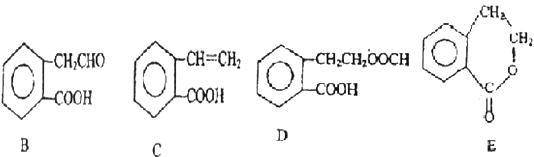
请回答下列问题:
(1)指出反应的类型:A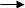 C:
。
C:
。
(2)在A-E五种物质中,互为同分异构体的是 (填代号)。
(3)写出由A生成B的化学方程式 。
(4)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是 (填代号)。
(5)C能形成高聚物,写出C生成其高聚物的化学方程式 。
(6)写出D与Na0H溶液共热反应的化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com