
13.(8分:每空1分)下表是元素周期表的一部分。
族
 周期 周期 |
ⅠA |
ⅡB |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
一 |
① |
|
|||||
|
二 |
② |
|
|
③ |
④ |
⑤ |
⑥ |
|
三 |
⑦ |
⑧ |
|
|
|
⑨ |
⑩ |
|
四 |
⑾ |
|
⑿ |
|
|
|
⒀ |
(1)表中元素______的非金属性最强;元素______的金属性最强; (填写元素符号);
(2)表中元素③⑨组成的物质,分子内含有________键(填极性或非极性,下同),其分子为_______分子;
(3)表中元素⑥⑩⒀氢化物的稳定性顺序为_____>_____>_____(填写化学式,下同);
(4)用电子式表示表中⑧⑩两元素形成化合物的过程
__________________________________________________________。
12.在pH=13的无色溶液中,可以大量共存的一组离子是: ( )
A.NH4+、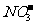 、K+、
、K+、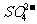 B.
B.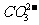 、
、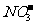 、
、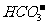 、Na+
、Na+
C.Na+、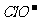 、
、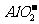 、
、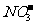 D.
D.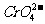 、K+、Na+、
、K+、Na+、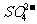
|
本卷包括必考和选考题两部分,第13~16题为必考题,每个试题考生都必修做答。第17~25题为选做题,考生根据要求做答。
11.25℃、101KPa时,1g甲醇完全燃烧生成CO2和H2O,同时放出22.68KJ热量。下列表示该反应的热化学方程式中正确的是 ( )
A.2CH4O(l)+ 3O2(g)==2CO2(g)+4H2O(l) △H=-22.68KJ/mol
B.2CH4O(l)+ 3O2(g)==2CO2(g)+4H2O(l) △H=+1451.6KJ/mol
C.CH4O(l)+ 3/2 O2(g)==CO2(g)+2H2O(l) △H=-725.8KJ/mol
D.CH4O(l)+ 3/2 O2(g)==CO2(g)+2H2O(g) △H=-725.8KJ/mol
10.A、B、C、D、E均为短周期元素。A、B、C位于同一周期相邻位置,它们分别与D形成的分子中都有10个电子,且A和C的原子序数之比为3︰4。E原子半径是短周期元素原子半径最大的。则下列叙述正确的是 ( )
A.A和C能形成共价化合物
B.由B、D原子构成的分子的结构是正四面体
C.E和C只能形成E2C 一种化合物
D.由A、B、C、D四种元素形成的化合物一定不属于无机盐
9.设NA为阿伏加德罗常数,下列说法正确的是: ( )
A.标准状况下,5.6L四氯化碳含有的分子数为0.25NA
B.标准状况下,14g氮气含有的核外电子数为5NA
C.标准状况下,22.4L任意比的氢气和氯气的混合气体中含有的分子总数均为NA
D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA
8.下列离子方程式中,表达正确的是 ( )
A.向 NaHS 溶液中通入适量氯气:HS―+Cl2 =S↓+H++2Cl―
B.向Fe(OH)3悬浊液中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
C.将 10 mL 0.1 mol•L-l HCl溶液与20 mL 0.05 mol•L-l Na3PO4 溶液混合
3H++2 PO43―= H2PO4―+HPO42―
D.向 Mg(HCO3)2溶液中加入过量NaOH 溶液
Mg2++2HCO3―+2OH―=MgCO3↓+CO32―+2H2O
7.巴豆酸的结构简式为CH3CH=CHCOOH ,现有①水;②溴的四氯化碳溶液;③乙醇;④纯碱溶液;⑤酸性KMnO4溶液,在一定条件下,能与巴豆酸反应的物质组合是( )
A.只有②④⑤ B.只有②③⑤ C.只有②③④⑤ D.①②③④⑤
6.现有三种常见治疗胃病药品的标签:

① ② ③
药品中所含的物质均能中和胃里过量的盐酸,下列关于三种药片中和胃酸的能力比较,正确的是: ( )
A.①=②=③ B.①>②>③ C.③>②>① D.②>③>①
5.据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学方程式为: 5KClO3 + 6P=3P2O5 + 5KCl ,则下列有关叙述错误的是 ( )
A.上述反应是氧化还原反应
B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中
的水分,生成磷酸小液滴(雾)
C.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替
D.上述反应中消耗3molP时,转移电子的物质的量为15mol
4.下列实验不能达到预期目的是 ( )
A.用饱和碳酸钠溶液除去乙酸乙酯中混有的乙酸
B.向某溶液中滴入稀盐酸与氯化钡的混合溶液,检验该溶液中是否含有SO42-
C.将颗粒大小相同的钠与钾分别与水反应,比较钠、钾金属活泼性的强弱
D.将Mg(OH)2和Al(OH)3分别与过量NaOH溶液反应,比较其碱性的强弱
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com