
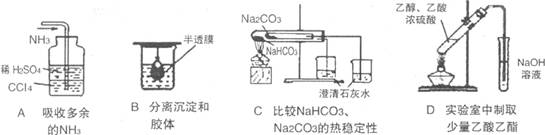
5.用下列实验装置完成对应的实验,能达到实验目的的是
4.下列有关化学史的叙述错误的是
A.我国春秋晚期能炼铁,战国晚期能炼钢
B.法国科学家道尔顿提出了近代原子学说
C.意大利科学家阿佛加德罗提出了分子的概念
D.俄国化学家门捷列大发现了元素周期律
3.海水淡化可采用膜分离技术。如下图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其它各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化分析不正确的是
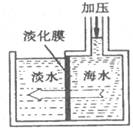
A.钠离子浓度增大 B.溶液质量不变
C.溶剂质量减少 D.溶质质量分数增加
2.下列说法不正确的是
A.某地工厂较多,经常处于红棕色烟雾中,估计空气污染物中可能含有Fe2O3粉尘
B.不法分子往奶粉中添加的三聚氰胺(化学式为C3H6N6)属于有机化合物
C.最好喝纯净水,因为纯净水不含任何化学物质
D.运动员大量运动出了很多汗,最好喝含有氯化钠的水,这样可以补充必需的盐分
1.承担神舟飞船发射任务的长征二号F运载火箭,使用四氧化二氮和偏二甲肼作为推进剂,当引燃后产生大量高温气体从火箭尾部喷出。高温气体成分有CO2、H2O、N2、NO等,这些气体均为无色,但在卫星发射现场看到火箭喷射出大量红烟,产生红烟的原因是
A.高温下N2遇空气生成NO2 B.NO与H2O反应生成NO2
C.CO2与NO反应生成NO2 D.NO遇空气生成NO2
20.(8分)白色粉末A由Na2SO3、Na2SO4 和NaCl等物质中的二种或三种混合而成,取一定量A样品,投入100 mL 2.2 mol·L-1 盐酸中,充分反应后过滤,最终得到100 mL含H+ 的物质的量浓度为1 mol·L-1 的滤液。若将此滤液蒸干,只得到8.19g纯净物B。
(1)B的化学式 ;
(2)则所取的A样品中含有的各物质的物质的量分别为 ;该样品与投入的盐酸反应后生成气体的体积为(标准状况) 。
19.(11分)下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、C是气体单质,B为金属;气体E极易溶于水、液态常做致冷剂。D为黑色固体,H的固体受热分解生成两种气体E和y,y的组成元素均为短周期元素。
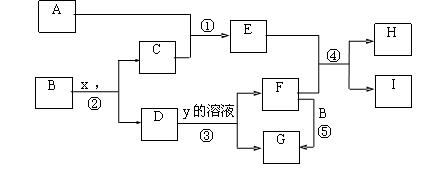
(1)写出:G的化学式 ,y的电子式 ;
(2)反应②的化学方程式为 ,反应④的离子方程式为 ;
(3)鉴定H中阳离子的实验方法和现象 。
18.(11分)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
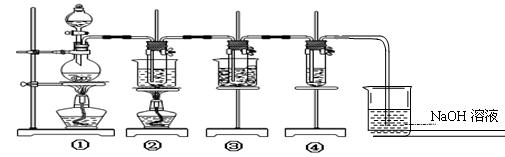
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;请填写下列空白:
(1)制取氯气时,通过分液漏斗向盛有二氧化锰固体的烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装 (填写化学试剂和装置名称);
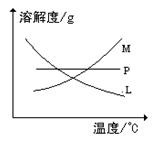
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是: , ③的试管中反应的化学方程式为 ,反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是_______(填写编号字母);从②的试管中分离出该晶体的方法是_________ (填写实验操作名称);
(3)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
|
实验现象 |
原因 |
|
溶液最初从紫色逐渐变为_____色 |
|
|
随后溶液逐渐变为无色 |
|
17.(11分)某化学研究小组测定某FeCl3 样品(含少量FeCl2 杂质)中铁元素的质量分数,在实验室中按以下步骤进行实验:
① 称取a g样品,置于烧杯中;
② 加适量盐酸和适量蒸馏水使样品溶解,准确配制成250mL溶液;
③ 准确量取25.00 mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;
④ 加入过量氨水,充分搅拌,使沉淀完全;
⑤ 过滤,洗涤沉淀;
⑥ 将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,冷却至室温后,称量;
⑦……。

请根据上面叙述,回答:
(1)上图仪器中,实验步骤①②③中必须用到的仪器是E和 (填仪器序号);
(2)检验沉淀是否洗净,应向洗涤液中加入几滴 (填写序号);
①KSCN溶液 ②NaOH溶液 ③AgNO3 溶液 ④酚酞试液
(3)第⑥步的操作中,将沉淀物加热,冷却至室温,称量其质量为m1g,再次加热并冷却至室温称量其质量为m2 g,若m1与m2 差值较大,其原因可能是 ;
(4)若坩埚质量是W1 g,最终坩埚和固体的总质量是W2 g,则样品中铁元素的质量分数为 。
16.(11分)A、B、C、D、E属于短周期主族元素。其中A元素的原子是短周期中原子半径最大的原子,B是最小的原子;C元素原子的最外层电子数为m,次外层电子数为n;D元素原子的L层电子数为m+n,M层电子数为m-n;E元素原子的最外层电子数等于其电子层数,且在周期表中与D元素相邻; A、B、C三种元素可组成化合物X,C、E可组成化合物Y。
(1)写出下列元素的元素符号:A ,D ;
(2)A~E所形成的简单离子中,与Mg2+具有相同电子层结构的是 (用离子符号表示);
(3)化合物Y与X的水溶液反应的离子方程式为 ;
(4)A和C可在一定条件下相互作用可生成一种用于航天员在太空舱中的供氧剂,写出该反应的化学方程式: ;C、D组成的化合物Z的化学式为 ,Z在信息技术上的一种重要用途是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com