
11.下列有关说法不正确的是 ( )
A.焙制糕点所用的发酵粉只是由碳酸氢钠组成
B.我国政府为了消除碘缺乏病,在食盐中加入了一定量的碘酸钾
C.医疗上用质量分数为3%或更小的稀双氧水作为消毒杀菌剂
D.二氧化硫可以用作食物和干果的防腐剂
l2.用NA表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.0.6 g CaCO3与Mg3N2的混合物中所含质子数为0 .6NA
B.64g的铜发生氧化还原反应,一定失去2NA个电子
C.32 g S8(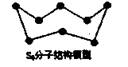 )单质中含有的S-S键个数为NA
)单质中含有的S-S键个数为NA
D.28.6g Na2CO3·10H2O在晶体中或在溶液中,含有的CO32-离子均小于0.1NA
10.在浓盐酸中HNO2与SnCl2反应的离子方程式为:
3SnCl2+12C1-+2 HNO2+6H+=N2+3SnClxy-+4H2O关于该反应的说法中正确的组合是( )
①氧化剂是HNO2; ②还原性:Cl->N2;
③每生成2.8gN2,还原剂失去的电子为0.6mol;
④x为4,y为2; ⑤SnClxy-是氧化产物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
9.向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示,则下列分析与判断不正确的是(不计CO2的溶解) ( )
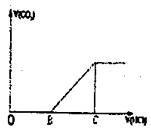
A.若OB=0,则形成溶液M所发生的离子反应方程式为:OH-+ CO2=HCO3-
B.若OB=BC,则溶液M为Na2CO3溶液
C.若OB>BC,则溶液M中大量存在的阴离子为CO32-和HCO3-
D.若3OB=BC,则溶液M中C(NaHCH3)=2c(Na2CO3)
8.下列离子方程式书写正确的是: ( )
A.溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5+Br+OH-
 CH2↑+Br-+H2O
CH2↑+Br-+H2O
B.等物质的量浓度、等体积的Ca(HCO3)2溶液与NaOH溶液相混合:
Ca2+2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.向Fe(NO 3)2和KI稀的混合溶液中滴几滴盐酸:
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
D.在H2O2中加入酸性KMnO4溶液:2MnO4一+5 H2O2+6H+=2Mn2++5 O2↑+8H2O
7.A、B、C、D、E为原子序数依次递增的同一短周期主族元素,下列说法一定正确的是(m、n均为正整数) ( )
A.若A、B的最高价氧化物水化物均为碱,则A(OH)n的碱性一定比B(OH)n+1的碱性强
B.若D、E的气态氢化物均溶于水,则E的氢化物的沸点一定比D的氢化物的沸点高
C.若C的最低化合价为一3,则E的最高正化合价为+6
D.若B的最高正化合价为+4,则五种元素的单质所形成的晶体都是分子晶体
6.关于某溶液所含离子的检验方法和结论都正确的是 ( )
A.加入NaOH溶液,先有白色沉淀生成,而后沉淀消失,则原溶液一定有Al3+
B.加入AgNO3溶液有白色沉淀生成,加稀盐酸沉淀不消失,则原溶液中一定有Cl-
C.加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中不一定有CO32-或SO32-
D.加入NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液中一定含有NH4+
28.现取等物质的量混合的氧气、氮气和二氧化碳气体amol,压强为pPa,在固定容积的密闭容器中进行实验。
(1)若加入过量硫,加热条件下充分反应后,恢复到原温度,则压强是原来的 倍。
(2)若加入一定量的磷,加热条件下,充分反应生成P2O5后,恢复到原温度,压强是原来的3/4,则加入磷的质量为 。
(3)若加入b mol碳,高温条件下充分反应后,恢复到原温度,试计算反应后气体压强是原来的倍数。(写出计算过程)
27.(12分)已知A-L所代表的物质(或溶液中的溶质)都是中学化学课本里学过的物质。通常状况下,A、B是淡黄色固体,B是金黄色固体,俗称“愚人金”,D是单质气体,E是无色无味气体,K是不溶于水的酸。反应①一③是化学工业生产某重要产品的三步反应,反应④是工业生产普通玻璃的反应之一。一定条件下,各物质间的相互转化关系如图所示(反应时加入或生成的水均没标出)
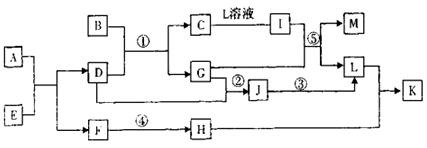
请回答:
(1)写出下列物质的化学式:B ;D的同素异形体
(2)写出A的电子式 ;E的电子式
(3)指出反应①、②、③是吸热反应,还是放热反应
① ② ③
(4)完成下列反应方程式:
反应⑤的离子方程式:
反应④的化学议程式为 。
(5)15.6克A与适量E完全反应,转移的电子的物质的量为
26.(7分)某无色溶液可能含有下列钠盐中的几种:(A)氯化钠(B)硫化钠(C)亚硫酸钠(D)硫代硫酸钠(E)硫酸钠(F)碳酸钠。向此溶液中加入适量稀硫酸,有浅黄色的沉淀析出,同时有气体产生。此气体有臭鸡蛋气味,可使澄清的石灰水变浑浊,不能使品红试液褪色。根据上述实验现象回答下列问题。
(1)不能使品红试液褪色,说明该气体中不含_________(填分子式)。(2分)
(2)此无色溶液中至少存在哪几种钠盐?请写出全部可能的情况(填写相应的字母)。
第一种情况是______________,第二种情况是________________________,
第三种情况是______________,第四种情况是________________________。
(对1空给2分,对两空给5分,每错1空,倒扣3分,不出现负分)
2.形成稳定结构的倾向
下表是一些气态基态原子失去核外不同电子所需的能量(kJ·mol-1):
|
|
锂 |
X |
Y |
|
失去第一电电子 |
519 |
502 |
580 |
|
失去第二电电子 |
7296 |
4570 |
1820 |
|
失去第三电电子 |
11799 |
6920 |
2750 |
|
失去第四电电子 |
|
9550 |
11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_______________________________。
②表中X可能为以上13种元素中的 (填写字母)元素。用元素符号表示X和j形成化合物的化学式_ ________ 。
③Y是周期表中_________ 族元素。
④以上13种元素中,_________ (填写字母)元素原子失去核外第一个电子需要的能量最多。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com