
9£Æœ¬ÕºŒ™ µ—È “÷∆«‚∆¯µƒºÚ“◊◊∞÷√°£»Ù‘⁄º”œ°¡ÚÀ· ±£¨∑¢œ÷–ø¡£”Îœ°¡ÚÀ·√ª”–Ω”¥•∂¯œ°¡ÚÀ·”÷≤ªπª¡À£¨Œ™ π∏√∑¥”¶À≥¿˚Ω¯––£¨‘Úø…“‘¥”≥§æ±¬©∂∑÷–º”»Îµƒ ‘º¡ «°°°°°°°°°° (°°°° )
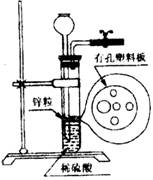
°°°°°° ¢Ÿ ≥—ŒÀÆ°°°° °°°°°°°°°° ¢⁄KNO3»Ð“∫°°°° °°°° ¢€ ¡øœ°¡ÚÀ·Õ≠»Ð“∫°°°°
¢ÐNa2CO3»Ð“∫°°°°°°°° ¢ðCCl4°° °°°°°°°°°°°°°°°° ¢Þ≈®∞±ÀÆ
A£Æ¢Ÿ¢€¢ð°° °°°°°°°°°°°° B£Æ¢⁄¢Þ°° °°°°°°°°°°°°°° C£Æ¢€¢ð°°°° °°°°°°°°°°°° D£Æ¢Ÿ¢⁄¢Ð
8£Æœ¬¡–¿Î◊”∑Ω≥Ã Ω’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°° (°°°° )
A£Æ”√–°À’¥Ú÷Œ¡∆Œ∏À·π˝∂ý£∫HCO3£≠+H+==CO2°¸+H2O
°°°° B£ÆœÚ¬»ªØ¬¡»Ð“∫÷–º”»Îπ˝¡ø∞±ÀÆ£∫Al3++3OH£≠==Al(OH)3°˝
°°°° C£Æ¬»∆¯Õ®»ÎÀÆ÷–£∫Cl2+H2O==2H++Cl£≠+ClO£≠
°°°° D£ÆœÚ ت“ÀÆ÷–º”»Îπ˝¡øNaHCO3»Ð“∫£∫Ca2++OH£≠+HCO3£≠==CaCO3°˝+H2O
7£Æ…ËNAŒ™∞¢∑¸º”µ¬¬Þ≥£ ˝£¨œ¬¡–Àµ∑®’˝»∑µƒ «°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°° (°°°° )
A£Æ±Í◊º◊¥øˆœ¬£¨11.2LH2O∫¨”–0.5NA∏ˆH2O∑÷◊”
B£Æ14g““œ©∫Õ±˚œ©µƒªÏ∫œŒÔ÷–◊Б≠◊” ˝Œ™3NA∏ˆ
C£Æ0.1L3mol°§L£≠1µƒNH4NO3»Ð“∫÷–∫¨”–µƒNH4+ ˝ƒøŒ™0.3NA
D£Æ7.1 g¬»∆¯”ÎÀÆÕÍ»´∑¥”¶◊™“∆µÁ◊” ˝ƒøŒ™0.2NA
6£Æœ¬¡–ŒÔ÷ ≤ªƒÐÕ®π˝ªØ∫œ∑¥”¶÷±Ω”÷∆µ√µƒ «°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°° (°°°° )
A£ÆFeCl2°°°° °°°°°°°°°° B£ÆNaHSO3°°°°°°°°°°°°°° C£ÆCu(OH)2°°°° °° D£ÆFe(OH)3
5£Æƒ≥∫œ◊˜—ßœ∞–°◊ÈÃ÷¬€±ÊŒˆ“‘œ¬Àµ∑®
¢Ÿ¥÷—Œ∫ÕÀ·”Í∂º «ªÏ∫œŒÔ£ª°°°°°°°°°°°°°°°°°°°° ¢⁄’”∆¯∫ÕÀÆ’Ù∆¯∂º «ø…‘Ÿ…˙ƒÐ‘¥£ª
¢€±˘∫Õ∏…±˘º» «¥ø檌Ԕ÷ «ªØ∫œŒÔ£ª°°°°°° ¢Ð≤ª–‚∏÷∫Õƒø«∞¡˜Õ®µƒ”≤±“∂º «∫œΩ£ª
¢ð—ŒÀ·∫Õ ≥¥◊º» «ªØ∫œŒÔ”÷ «À·£ª°°°°°°°°°° ¢Þ¥øºÓ∫Õ Ï Øª“∂º «ºÓ°£
…œ ˆÀµ∑®’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°° (°°°° )
A£Æ¢Ÿ¢⁄¢€¢Ð°° °°°°°° B£Æ¢Ÿ¢⁄¢ð¢Þ°°°° °°°° C£Æ¢Ÿ¢€¢Ð°°°° °°°°°°°° D£Æ¢€¢ð¢Þ
4£Æ±Í◊º◊¥øˆœ¬£¨‘⁄“ªªÓ»˚ Ωµƒ√б’»ð∆˜÷–£¨≥‰»Î2.24LµƒNO£¨‘Ÿ–°–ƒ≥‰»Î1.12NO2∑¥”¶Õͱœ£¨»‘ª÷∏¥÷¡±Í◊º◊¥øˆ£¨‘Úœ¬¡–∏˜œÓ– ˆ÷–≤ª’˝»∑µƒ « °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°° A£Æ∆¯Ã±‰Œ™∫Ï◊ÿ…´
°°°° B£Æ∆¯ÃÂê˝”¶–°”⁄2.24L
°°°° C£Æ∏√∆¯Ã‘⁄±Í◊º◊¥øˆœ¬µƒ√Ð∂»Œ™2.05g°§L-1
°°°° D£Æ∏√∆¯Ã‘⁄±Í◊º◊¥øˆœ¬µƒ√Ð∂»¥Û”⁄2.05g°§L-1
3£Æƒ≥¿Î◊”R2+µƒ◊ÓÕ‚≤„”–2∏ˆµÁ◊”£¨«“”–5∏ˆµÁ◊”≤„£¨µ±πÃÃÂRCl2»Ð”⁄ÀÆ≈‰≥…»Ð“∫ ±£¨–˺”»Î…Ÿ¡øµ•÷ R∫Õ—ŒÀ·°£”…¥ÀÕ∆∂œœ¬¡–– ˆ’˝»∑µƒ « °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°° °°°° A£ÆRŒ™IIA◊‘™Àÿ
°° °°°° B£ÆRµƒ◊Ó∏þº€—ıªØŒÔµƒÀÆªØŒÔ ««øºÓ
°° °°°° C£ÆR2+µƒœıÀ·—ŒµƒÀƻГ∫≥ À·–‘
°°°°°° D£ÆRCl4æþ”–«ø—ıªØ–‘£¨»ð“◊±ªªπ‘≠
2£ÆΩ®≤ƒ÷–µƒ∑≈…‰–‘ŒÔ÷ À•±‰ª·…˙≥…æþ”–∑≈…‰–‘µƒÎ±∆¯£¨Œ“√«Œ¸»Îα∆¯∫Ûª·”–∫¶”⁄Ω°øµ£¨Î±‘™Àÿµƒ‘≠◊”–Ú ˝ «86£¨œý∂‘‘≠◊”÷ ¡ø «222£¨ø∆—ߺ“ªπ∑¢œ÷ƒ≥–©∑≈…‰–‘øÛŒÔ∑÷Ω‚∑≈≥ˆµƒ°∞Ôπ…‰∆¯°± «”…÷ ◊” ˝86£¨÷ ¡ø ˝219µƒ“ª÷÷Ôπ‘≠◊”◊È≥…°£œ¬¡–”–πÿᵃÀµ∑®’˝»∑µƒ «°° (°°°° )°°°°°°°°°°°°°°°°°°°°°°
A£Æα∆¯‘⁄±Í◊º◊¥øˆœ¬µƒ√Ð∂»‘º «9.91g£ØL
B£Æα∆¯ªØ—ß–‘÷ ΩœªÓ∆√£¨“Ú¥À∂‘»ÀÔ–∫¶
C£Æα‘≠◊”∫ÀÕ‚”–∆þ∏ˆµÁ◊”≤„£¨◊ÓÕ‚≤„”–8∏ˆµÁ◊”
D£Æ°∞Ôπ…‰∆¯°± «Î±µƒÕ¨Àÿ“Ï–ŒÃÂ
1£Æ‘⁄œ¬¡–±»Ωœ÷–£¨’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£Æ л»Œ»∂®–‘£∫HI£æHBr£æHCl£æHF °°°° B£Æ∑÷◊”÷–µƒº¸Ω«£∫CH4 = H2O£ºCO2
°°°° C£ÆŒ¢¡£∞Îæ∂£∫ F£≠£º Na+£º Mg2+°° °°°°°°°°°°°°°° D£Æµ•÷ µƒ»€µ„£∫ Li£æNa£æK£æRb
24£Æ(5∑÷)‘⁄250mLƒ≥ªÏ∫œ»Ð“∫÷–£¨HNO3∫ÕH2SO4ŒÔ÷ µƒ¡ø≈®∂»∑÷±Œ™0.2mol°§L-1∫Õ0.1mol°§L-1°£œÚ∏√ªÏ∫œ»Ð“∫÷–º”»Î1.92gÕ≠∑€£¨º”»»≥‰∑÷∑¥”¶°£
°° (1)–¥≥ˆ∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°°°°°° °£
°° (2)º∆À„À˘µ√»Ð“∫÷–Cu2+µƒŒÔ÷ µƒ¡ø≈®∂»°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com