
28£®(16·Ö)A¡¢B¡¢C¡¢DËÄÖÖ·¼Ïă×廯ºÏÎïµÄ½á¹¹¼̣ʽÈçÏÂËùʾ£º
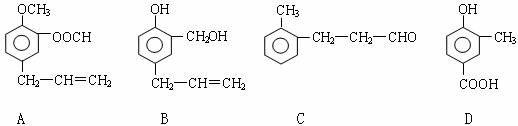
Çë»Ø´đÏÂÁĐÎỀ⣺
(1)Đ´³öAÖĐÎ̃Ñơ¹ÙÄÜÍŵÄĂû³Æ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»DÖĐº¬Ñơ¹ÙÄÜÍŵĽṹ¼̣ʽΪ¡¡¡¡ ¡¡¡¡¡¡¡£
(2)ÓĂA¡¢B¡¢C¡¢D̀î¿Ơ£ºÄÜ·¢Éú̉ø¾µ·´Ó¦µÄÓĐ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»¼ÈÄÜÓëFeCl3ÈÜ̉º·¢ÉúÏÔÉ«·´Ó¦ÓÖÄÜÓëNa2CO3ÈÜ̉º·´Ó¦·Å³öÆø̀åµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)°´ÏÂͼC¾̉»²½·´Ó¦¿ÉÉú³ÉE£¬EÊÇBµÄͬ·Ö̉́¹¹̀壬
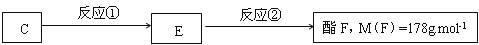
Ộ·´Ó¦¢ÙµÄ·´Ó¦ÀàĐÍΪ¡¡ ¡¡¡¡¡¡¡¡£»Đ´³ö·´Ó¦¢ÚµÄ»¯Ñ§·½³̀ʽ£º¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡£
(4)G¡¢HºÍD»¥ÎªÍ¬·Ö̉́¹¹̀壬ËüĂǾßÓĐÈçÏẦØµă£º
¢Ù GºÍH¶¼ÊDZ½µÄ¶₫Ԫȡ´úÎƠâÁ½¸öÈ¡´ú»ù·Ö±đΪôÇ»ùºÍº¬ÓĐ£COO£½á¹¹µÄ»ùÍÅ£»
¢Ú GºÍH±½»·ÉϵÄ̉»ÂÈ´úÎïÓĐÁ½ÖÖ²»Í¬½á¹¹£»
¢Û G¿É̉Ô·¢Éú̉ø¾µ·´Ó¦£¬H·Ö×ÓÖб½»·²»ÓëÈ¡´ú»ù̀¼Ô×ÓÖ±½ÓÏàÁ¬ ¡£
Đ´³öGºÍHµÄ½á¹¹¼̣ʽ£ºG£º¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡£»H£º¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡£
27£®(13·Ö)A-I·Ö±đ±íʾÖĐѧ»¯Ñ§ÖĐ³£¼ûµÄ̉»ÖÖÎïÖÊ£¬ËüĂÇÖ®¼äÏ໥¹ØϵÈçÏÂͼËùʾ(²¿·Ö·´Ó¦Îï¡¢Éú³ÉÎïĂ»ÓĐÁĐ³ö)£¬Ç̉̉ÑÖªGΪÖ÷×åÔªËصĹ̀̀¬Ñơ»¯ÎA¡¢B¡¢C¡¢D¡¢E¡¢FÁùÖÖÎïÖÊÖĐ¾ùº¬Í¬̉»ÖÖÔªËØ¡£
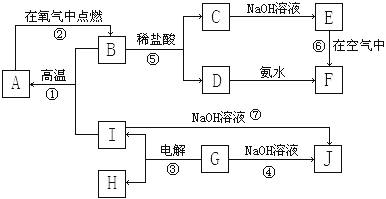
Çë̀îĐ´ÏÂÁĐ¿Ơ°×£º
(1)I¡¢G¡¢JÈưÖÖÎïÖÊÖĐËùº¬Í¬̉»ÖÖÔªËØÔÚÖÜÆÚ±íÖĐλÖõÚ_______ÖÜÆÚ¡¢µÚ_______×å £»
(2)Đ´³ö·´Ó¦¢̃µÄ»¯Ñ§·½³̀ʽ___________¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ _________£»
(3)Đ´³ö·´Ó¦¢ÜµÄÀë×Ó·½³̀ʽ_____________¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ _______£»
(4)Èô28g Aµ¥ÖÊÔÚ×ăÁ¿µÄÑơÆøÖĐ×ÆÉƠ£¬·´Ó¦·Å³öµÄÈÈÁ¿ÎªQ kJ(Q > 0)£¬Đ´³öƠâ¸ö·´Ó¦µÄÈÈ»¯Ñ§·½³̀ʽ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(5)·´Ó¦¢ßÖĐÈôÓĐ18g I²ÎÓë·´Ó¦£¬Ộת̉Ƶç×ÓÊưΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ NA¡£
26£®(15·Ö)
(1)ºÏ³É°±¹¤̉µ¶Ô»¯Ñ§¹¤̉µºÍ¹ú·À¹¤̉µ¾ßÓĐÖØ̉ª̉ẩå¡£¹¤̉µºÏ³É°±µÄÔÀíÊÇ£º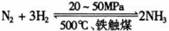 ¡÷H <0£¬Éú²úÁ÷³̀ÈçÏÂͼËùʾ¡£
¡÷H <0£¬Éú²úÁ÷³̀ÈçÏÂͼËùʾ¡£
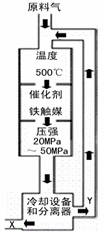
¢ÙXµÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡ £»
¢ÚÉÏͼÖĐ̀ơ¼₫Ñ¡¶¨µÄÖ÷̉ªỘ̉ÊÇ(Ñ¡̀î×ÖĸĐ̣ºÅ) ¡¡¡¡¡¡¡¡£»
A£®Éư¸ßζȡ¢Ôö´óѹǿ¾ùÓĐÀûÓÚ̀á¸ß°±µÄת»¯ÂÊ
B£®̀ú´¥Ă½ÔÚ¸ĂζÈʱ»îĐÔ´ó
C£®¹¤̉µÉú²úÊܶ¯Á¦¡¢²ÄÁÏ¡¢É豸µÈ̀ơ¼₫µÄÏ̃ÖÆ
¢ÛÈôÉư¸ßζȣ¬´ïĐÂƽºâʱ£¬Æ½ºâ³£Êư½«__________(̀îÔö´ó»̣¼ơĐ¡»̣²»±ä)¡£
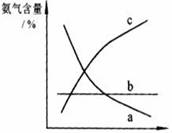
¢Ü¸Ä±ä·´Ó¦̀ơ¼₫£¬»áʹƽºâ·¢Éú̉ƶ¯¡£ÏÂͼ±íʾËæ̀ơ¼₫¸Ä±ä£¬°±ÆøµÄ°Ù·Öº¬Á¿µÄ±ä»¯Ç÷ÊÆ¡£µ±ºá×ø±êΪѹǿʱ£¬±ä»¯Ç÷ÊÆƠưÈ·µÄÊÇ(Ñ¡̀î×ÖĸĐ̣ºÅ) ¡¡¡¡¡¡¡¡£¬µ±ºá×ø±êΪζÈʱ£¬±ä»¯Ç÷ÊÆƠưÈ·µÄÊÇ(Ñ¡̀î×ÖĸĐ̣ºÅ)¡¡¡¡¡¡¡¡ £»
(2)³£ÎÂÏ°±Æø¼«̉×ÈÜÓÚË®£¬ÆäË®ÈÜ̉º¿É̉Ôµ¼µç¡£
¢ƯÓĂ·½³̀ʽ±íʾ°±ÆøÈÜÓÚË®Ç̉ÏÔÈơ¼îĐԵĹư³̀£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡£»
¢̃°±Ë®ÖĐË®µçÀë³öµÄc(OH£) ¡¡¡¡¡¡¡¡¡¡10£7 mol¡¤L-1(̀îĐ´¡°£¾¡±¡¢¡°£¼¡±»̣¡°£½¡±)£»
¢ß½«Ïàͬ̀å»ư¡¢ÏàͬÎïÖʵÄÁ¿Å¨¶ÈµÄ°±Ë®ºÍÑÎËá»́ºÏºó£¬ÈÜ̉ºÖĐÀë×ÓŨ¶ÈÓÉ´óµ½Đ¡̉À´ÎΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
13£®ÔÚº¬ÓĐNaI¡¢FeBr2ºÍNa2SO3¸÷1 molµÄÈÜ̉ºÖĐͨÈë×ăÁ¿µÄCl2£¬½«ÈÜ̉ºÔÚ¿ƠÆøÖĐ¼ÓÈÈƠô¸É²¢³ä·Ö×ÆÉƠ£¬×îÖƠµĂµ½Ê£ÓàµÄ¹̀̀åÎïÖÊÊÇ(¡¡¡¡¡¡¡¡¡¡¡¡¡¡ )
A£®NaCl¡¢FeCl3¡¢Na2SO4 ¡¡¡¡¡¡¡¡¡¡¡¡B£®NaCl¡¢FeBr3¡¢Na2SO4
C£®NaI¡¢FeCl3¡¢Na2SO3¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡D£®NaCl¡¢Fe2O3¡¢Na2SO4
µÚII¾í ·ÇÑ¡Ôñ̀â(¹²174·Ö)
12£®¦Á-đ°Î²ÍªÏăÁϵķÖ×ӽṹÈçÏÂͼ£¬ÏÂÁĐ˵·¨²»ƠưÈ·µÄÊÇ (¡¡¡¡ )
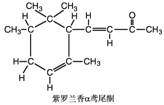
A£®¦Á-đ°Î²Íª¿ÉÓëijÖÖ·Ó»¥ÎªÍ¬·Ö̉́¹¹̀å
B£®1mol¦Á-đ°Î²Íª×î¶à¿ÉÓë3molH2¼Ó³É
C£®¦Á-đ°Î²ÍªÄÜ·¢Éú̉ø¾µ·´Ó¦
D£®¦Á-đ°Î²Íª¾¼ÓÇâ¡úÏûÈ¥¡ú¼ÓÇâÈư²½·´Ó¦¿Éת±äΪ£º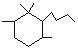
11£®Ă¾¼°Æ仯ºÏÎï̉»°ăÎ̃¶¾(»̣µÍ¶¾)¡¢Î̃ÎÛȾ£¬Ă¾µç³Ø·Åµçʱµçѹ¸ßÇ̉ƽÎÈ£¬̣̉¶øÔ½À´Ô½³ÉΪÈËĂÇÑĐÖÆẦÉ«µç³ØËù¹Ø×¢µÄÖØµă¡£ÓĐ̉»ÖÖĂ¾¶₫´Îµç³ØµÄ·´Ó¦Îª£º
xMg+Mo3S4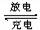 MgxMo3S4
£»ÏÂÁĐ˵·¨ÖĐ´íÎóµÄÊÇ(¡¡¡¡¡¡ )
MgxMo3S4
£»ÏÂÁĐ˵·¨ÖĐ´íÎóµÄÊÇ(¡¡¡¡¡¡ )
A£®·ÅµçʱMg2+ Ị̈Ơư¼«Ç¨̉Æ¡¡¡¡¡¡ B£®·ÅµçʱƠư¼«µÄµç¼«·´Ó¦Îª Mo3S4 + 2xe- == Mo3S42x-
C£®·Åµçʱ Mo3S4 ·¢ÉúÑơ»¯·´Ó¦¡¡ D£®³äµçʱ̉ơ¼«µÄµç¼«·´Ó¦Îª x Mg2+ + 2xe- == xMg
10£®Ôڼס¢̉̉Á½ÉƠ±ÈÜ̉ºÖĐ£¬·Ö±đº¬ÓĐ´óÁ¿µÄCu2+¡¢K+¡¢H+¡¢Cl-¡¢CO32-¡¢OH-µÈ6ÖÖÀë×ÓÖеÄ3ÖÖ£¬̉ÑÖª¼×ÉƠ±µÄÈÜ̉º³ÊÀ¶É«£¬Ộ̉̉ÉƠ±µÄÈÜ̉ºÖĐ´óÁ¿´æÔÚµÄÀë×ÓÊÇ(¡¡ )
A£®Cu2+¡¢H+¡¢Cl- ¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®CO32-¡¢OH-¡¢Cl-¡¡
C£®K+¡¢H+¡¢Cl-¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®K+¡¢OH-¡¢CO32-
9£®ÏÂÁĐʵÑé²Ù×÷»̣¶ÔʵÑéÊÂʵµÄĐđÊö²»ƠưÈ·µÄÊÇ(¡¡¡¡ )
A£®ÓĂÏơËá̉øÈÜ̉ºÇø·Ö¶₫Ñơ»¯µªºÍäåƠôÆø
B£®¾Æ¾«µÆÅöµ¹È÷³ö¾Æ¾«×Å»đ£¬Ñ¸ËÙÓĂʪĨ²¼Æ˸Ç
C£®Î¶ȼÆˤ»µµ¼ÖÂË®̉øÉ¢Âäµ½µØĂæÉÏ£¬Ó¦Á¢¼´ÓĂË®³åÏ´Ë®̉ø
D£®¼́ÑéÂÈ´ú̀₫ÖеÄÂÈÔªËØʱ£¬¿ÉÏȼÓÇâÑơ»¯ÄÆÈÜ̉º£¬ÔÙ¼ÓÈëÏơËáÈÜ̉º£¬×îºó¼ÓÈëÏơËá̉øÈÜ̉ºÀ´½øĐĐ¼́Ñé
8£®ÏÂÁĐĐđÊöÖĐ´íÎóµÄÊÇ(¡¡¡¡ )
A£®±ê×¼×´¿öÏ£¬1LHClºÍ1LH2OµÄÎïÖʵÄÁ¿Ïàͬ
B£®±ê×¼×´¿öÏ£¬1gH2ºÍ14gN2µÄ̀å»ưÏàͬ£»
C£®ÔÚͬÎÂͬ̀å»ưʱ£¬Æø̀åÎïÖʵÄÎïÖʵÄÁ¿Ô½´ó£¬ỘѹǿԽ´ó
D£®Í¬ÎÂͬѹÏ£¬Æø̀åµÄĂܶÈÓëÆø̀åµÄÏà¶Ô·Ö×ÓÖÊÁ¿³ÉƠư±È¡£
7£®2007Äê8ÔÂ4ÈƠ5ʱ26·Ö(±±¾©Ê±¼ä17ʱ26·Ö)£¬ĂÀ¹ú¡°·ï»Ë¡±ºÅ»đĐÇ׎̀½²âÆ÷˳ÀûÉư¿Ơ£¬¿ªÊ¼·ÉÍù»đĐÇÖ®ÂĂ¡£¡°·ï»Ë¡±ºÅÉÏרĂÅ·ÅÁË̉»ƠÅĐäƠä¹âÅ̀£¬ÀïĂæ¼Ç¼ÁËƠâĂû¿Æѧ¼̉¡¢ƠÜѧ¼̉¡¢¿Æ»ĂĐ¡Ëµ¼̉µÈ¶Ô»đĐǵġ°ĂÎÏ롱¡£ƠâƠŹâÅ̀ÓÉʯӢ²£Á§ÖƳɣ¬ÄÜÔÚ»đĐÇÉÏ´ư500ÄꡣʯӢ²£Á§ÊÇÓĂ½Ï´¿¾»µÄ¶₫Ñơ»¯¹èÖƳɵġ£ÏÂÁĐ¹ØÓÚ¶₫Ñơ»¯¹èºÍʯӢ²£Á§µÄÓĐ¹Ø˵·¨²»ƠưÈ·µÄÊÇ(¡¡¡¡ )
A£®¶₫Ñơ»¯¹è¾§̀åÊÇÔ×Ó¾§̀å
B£®Ê¯Ó¢²£Á§ÖĐº¬ÓĐ¹èËáÑΡ¢¶₫Ñơ»¯¹è£¬ÄÍÈκÎËá¼î¸¯Ê´
C£®Ê¯Ó¢²£Á§ÖƳɵĹ⵼ÏËάÊÇ̉»ÖÖĐÂĐÍÎ̃»ú·Ç½đÊô²ÄÁÏ
D£®Ê¯Ó¢²£Á§ÓĐ½Ï¸ßµÄÈÛµă
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com