
23.(17分)某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
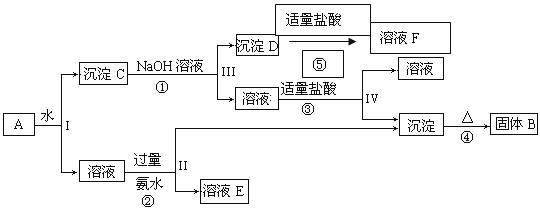
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式
固体B ;沉淀D ;
溶液E 。
(3)写出①、④两个反应的化学方程式
① ;④ 。
(4)写出②、③两个反应的离子方程式
② ;③ 。
(5)设计实验检验溶液F中所含溶质:
(6)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3 Fe2O3
22.(10分)
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______________________________________。
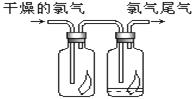
(2)为防止氯气尾气污染空气,可用 溶液吸收多余的氯气,原理是(用化学方程式表示)_________________________________。
(3)工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_______(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_______(用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
21.(16分)写出下列反应化学方程式或离子方程式
(1)过氧化钠可用在呼吸面具里作为氧气的来源,其反应的化学方程式为
____________________________________ ;
(2)氢氧化铝可用作治疗胃酸过多的药剂,其原理用离子方程式表示为
________________________________ ;
(3)氢氧化亚铁被氧气氧化的化学方程式____________________________;
|
;
;
。
(5)实验室制氨气的化学方程式: ;
(6)铜与浓硝酸反应的离子方程式: ;
20.在一定条件下,将钠与氧气反应的生成物1.5g溶于水,所得溶液恰好能被80mL浓度为0.5mol/L的HCl溶液中和,则生成物的成分是 ( )
A.Na2O B.Na2O2 C.Na2O和Na2O2 D.Na2O2和NaO2
第Ⅱ卷 非选择题(共60分)
19.在一定体积的18mol·L-1的浓硫酸中加入过量铜片并加热,被还原的硫酸的物质的量为0.9mol,则浓硫酸的实际体积为 ( )
A.等于50 mL B.大于50 mL
C.等于100 mL D.大于100 mL
18.a g铁粉与含有H2SO4的CuSO4溶液完全反应后,得到a g铜,则参与反应的CuSO4与H2SO4的物质的量之比为 ( )
A.1 :7 B.7 :1 C.7 :8 D.8 :7
17.在铜与稀硝酸的反应中,如果有1mol的硝酸被还原,则被氧化的铜的物质的量( )
A.3 mol B.3/2 mol C.3/8 mol D.8/3 mol
16.在氧化还原反应:2H2S + SO2 = 3S + 2H2O中,被氧化与被还原的硫原子数比是( )
A.1:1 B.1:2 C.3:2 D.2:1
15.下列叙述不正确的是 ( )
A.为防止氯化亚铁溶液变质,在氯化亚铁溶液中加铁粉。
B.二氧化硫和二氧化氮都能形成酸雨,酸雨的pH=5.6。
C.用铁片区分浓硫酸和稀硫酸。
D.用湿润的蓝色的石蕊试纸检验氨气。
14.下列物质在一定条件下能与铜反应的有 ( )
①Cl2 ②浓H2SO4 ③FeCl3 ④AgNO3 ⑤FeCl2
A.①③⑤ B.①③④ C.①②③④ D.①②③④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com