
12ЃЎРћгУЗДгІ2NO(g)+2CO(g) 2CO2(g)+N2(g);ЁїH=Ѓ746.8kJЁЄmol-1ЃЌПЩОЛЛЏЦћГЕЮВЦјЃЌШчЙћвЊЭЌЪБЬсИпИУЗДгІЕФЫйТЪКЭNOЕФзЊЛЏТЪЃЌВЩШЁЕФДыЪЉЪЧ(ЁЁЁЁ )
2CO2(g)+N2(g);ЁїH=Ѓ746.8kJЁЄmol-1ЃЌПЩОЛЛЏЦћГЕЮВЦјЃЌШчЙћвЊЭЌЪБЬсИпИУЗДгІЕФЫйТЪКЭNOЕФзЊЛЏТЪЃЌВЩШЁЕФДыЪЉЪЧ(ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎНЕЕЭЮТЖШЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎдіДѓбЙЧПЭЌЪБМгДпЛЏМС
ЁЁЁЁЁЁ CЃЎЩ§ИпЮТЖШЭЌЪБГфШыN2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎМАЪБНЋCO2КЭN2ДгЗДгІЬхЯЕжавЦзп
11ЃЎЯТСаЗДгІЕФРызгЗНГЬЪНЪщаДе§ШЗЕФЪЧЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЬМЫсЧтИЦШмвКгыЯЁЯѕЫсЗДгІЃКHCO-3+H+===CO2Ёќ+H2O
ЁЁЁЁЁЁ BЃЎЫЎВЃСЇжаЭЈШыЙ§СПЕФЖўбѕЛЏЬМЦјЬхЃКSiO2-3+CO2+H2O==H2SiO3+CO2-3
ЁЁЁЁЁЁ CЃЎХЈЩеМюШмвКжаМгШыТСЦЌЃКAl+OH-+H2O===AlO-2+H2Ёќ
ЁЁЁЁЁЁ DЃЎСђЫсЧтФЦШмвКгызуСПЧтбѕЛЏБЕШмвКЛьКЯЃК2H++SO2-4+Ba2++OH-===BaSO4Ё§+2H2O
10ЃЎЖЬжмЦкдЊЫиЕФРызгЁЃW2+ЁЂbX+ЁЂcY2-ЁЂdZ-ОпгаЯрЭЌЕФЕчзгВуНсЙЙЃЌЯТСаЭЦЖЯе§ШЗЕФЪЧ(ЁЁ ЁЁ)
ЁЁЁЁЁЁ AЃЎдзгАыОЖЃКW>X>Z>YЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎШШЮШЖЈадЃКH2Y>HZ
ЁЁЁЁЁЁ CЃЎРызгАыОЖЃКW2+>Y2-ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎМюадЃКXOH>W(OH)2
9ЃЎФГЮТЖШЯТЃЌЯђШнЛ§ЮЊ2LЕФУмБеЗДгІЦїжаГфШы0.10mol SO3ЃЌЕБЗДгІЦїжаЕФЦјЬхбЙЧПВЛдйБфЛЏЪБВтЕУSO3ЕФзЊЛЏТЪЮЊ20%ЃЌдђИУЮТЖШЯТЗДгІ2SO2(g)+O2(g) 2SO3(g)ЕФЦНКтГЃЪ§ЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
2SO3(g)ЕФЦНКтГЃЪ§ЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎ3.2ЁС103mol-1ЁЄLЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ1.6ЁС103mol-1ЁЄL
ЁЁЁЁЁЁ CЃЎ8.0ЁС102mol-1ЁЄL ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ4.0ЁС102mol-1ЁЄL
8ЃЎЯТСаЗжРыЛђЬсДПЗНЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ ЁЁ)
ЁЁЁЁЁЁ ЂйгУОЦОЋнЭШЁЕтЫЎжаЕФЕт
ЁЁЁЁЁЁ ЂкгУNa2CO3ШмвКГ§ШЅCaCO3ЙЬЬхжаЕФЩйСПCaSO4
ЁЁЁЁЁЁ ЂлгУNaOHШмвКГ§ШЅKClШмвКжаЕФЩйСПMgCl2
ЁЁЁЁЁЁ ЂмгыаТжЦЕФЩњЪЏЛвЛьКЯКѓеєСѓПЩГ§ШЅввДМжаЕФЩйСПЫЎ
ЁЁЁЁЁЁ AЃЎЂйЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂкЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂлЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂкЂм
7ЃЎЩшNAБэЪОАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎБъзМзДПіЯТЃЌ2.24LБНжаКЌгаЕФЗжзгЪ§ЮЊ0.1NA
ЁЁЁЁЁЁ BЃЎ0.1molЁЄL-1СђЫсЭШмвКжаКЌЭРызгЪ§ЮЊ0.1NA
ЁЁЁЁЁЁ CЃЎ0.1mol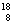 OдзгжаКЌжазгЪ§ЮЊNA
OдзгжаКЌжазгЪ§ЮЊNA
ЁЁЁЁЁЁ DЃЎ4.6gNO2ЦјЬхжаКЌгаЕФдзгЪ§ЮЊ0.1NA
6ЃЎЯТСаЗДгІЕФФмСПБфЛЏгыЦфЫћШ§ЯюВЛЯрЭЌЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎТСЗлгыбѕЛЏЬњЕФЗДгІЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎТШЛЏяЇгыЯћЪЏЛвЕФЗДгІ
ЁЁЁЁЁЁ CЃЎаПЦЌгыЯЁСђЫсЗДгІЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎФЦгыРфЫЎЗДгІ
5ЃЎЯТСаа№Ъіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎгУБъзМЧтбѕЛЏФЦШмвКЕЮЖЈКЌМзЛљГШЕФбЮЫсЃЌжеЕуЪБШмвКгЩГШЩЋБфГЩЛЦЩЋ
ЁЁЁЁЁЁ BЃЎНЋSO2ЭЈШыBaCl2ШмвКжаВњЩњАзЩЋГСЕэЃЌдйЕЮМгЯЁЯѕЫсГСЕэВЛЯћЪЇ
ЁЁЁЁЁЁ CЃЎНЋЕтбЮМгШыЕэЗлШмвКжаЃЌГфЗжНСАшКѓШмвКГЪРЖЩЋ
ЁЁЁЁЁЁ DЃЎЯђЦЯЬбЬЧШмвКжаМгШыаТжЦЧтбѕЛЏЭЃЌМгШШжСЗаЬкЃЌОВжУКѓЩЯВуШмвКЯдКьЩЋ
4ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎввЯЉКЭОлввЯЉЖМФмЪЙфхЕФЫФТШЛЏЬМШмвКЭЪЩЋ
ЁЁЁЁЁЁ BЃЎЕэЗлКЭЯЫЮЌЫиЖМПЩвдзїЮЊЙЄвЕЩЯЩњВњЦЯЬбЬЧЕФдСЯ
ЁЁЁЁЁЁ CЃЎгЭжЌЕФЫЎНтЗДгІЖМЪЧдэЛЏЗДгІ
ЁЁЁЁЁЁ DЃЎесЬЧЪЧИпЗжзгЛЏКЯЮяЃЌЦфЫЎНтВњЮяФмЗЂЩњвјОЕЗДгІ
3ЃЎЯТСаЙигкЭЕчМЋЕФа№Ъіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЭаПдЕчГижаЭЪЧИКМЋ
ЁЁЁЁЁЁ BЃЎдкЬњжЦЦЗЩЯЕчЖЦЭЪБЃЌгУЭзївѕМЋ
ЁЁЁЁЁЁ CЃЎЕчНтБЅКЭЪГбЮЫЎжЦЩеМюЪБЃЌгУЭзїбєМЋ
ЁЁЁЁЁЁ DЃЎЕчНтЗЈОЋСЖЭЪБЃЌДжЭСЌНгЕчдДЕФе§МЋ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com