
9.下列文字表述与反应方程式对应且正确的是:
A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓
B.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑
C.利用腐蚀法制作印刷线路板:Fe3+ + Cu == Fe2+ + Cu2+
D.实验室用液溴和苯在催化剂作用下制溴苯: 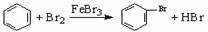
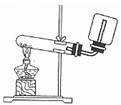
8.下列装置或操作能达到实验目的的是
.... 
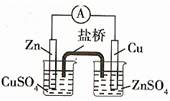
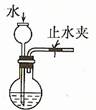
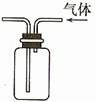
① ② ③ ④
.... A.①实验室制取并收集NH3
.... B.②构成铜锌原电池
.... C.③检查装置气密性
.... D.④利用排空气法收集CO2
7.化学与科技、社会、生产密切结合,下列有关说法错误的是
A.“乙醇汽油”的广泛使用能有效减少有害气体的排放
B.“无磷洗涤剂”的推广使用,能有效减少水体富营养化的发生
C.“无氟冰箱”取代“含氟冰箱”,对人类的保护伞--臭氧层起到保护作用
D.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
29.I.(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个化学方程式并配平。
________+________→________+________+________+H2O
(2)反应中1mol氧化剂得到________mol电子。
Ⅱ.某研究性学习小组拟用氧化铜和铜的混合物与硫酸和硝酸的混合液反应来制取CuSO4·5H2O,混酸中硝酸的还原产物只有NO,反应过程中不产生SO2,反应后溶液中不含Cu(NO3)2,反应后固体全部溶解,两种酸均恰好完全反应。设固体混合物质量为240克,其中氧化铜的质量分数为x,回答下列问题:
(3)所得硫酸铜晶体的质量y的表达式为_______(用x表示)
(4)若x=0.6,则混酸中硝酸与硫酸的物质的量之比为___。
28.用水杨酸和乙酸酐合成阿司匹林的过程如下:
在150ml的干燥锥形瓶中加入2 g水杨酸、5ml乙酸酐和5滴浓硫酸,振荡。待其溶解后置于85--90℃水浴中加热10分钟。取出,冷却至室温,用玻璃棒摩擦瓶壁后,即有晶体析出。向瓶中加入50毫升水,将锥形瓶置于冰水中,继续冷却使结晶完全。
减压过滤,用滤液淋洗锥形瓶,直至所有固体被收集在漏斗中。用少量蒸馏水洗涤晶体两次。然后将晶体转移至表面皿上,在空气中风干。
请回答下列问题
(1)写出制取阿司匹林的方程式__________.
(2)用玻璃棒摩擦瓶壁的目的是________________
(3)下图所示为减压过滤装置,回答有关问题。
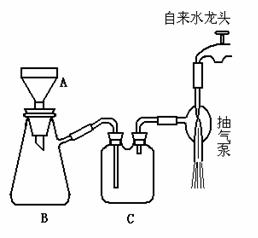
①写出图中A、B、C三种仪器的名称,A_____;B ______;C________。
②该装置图有几处错误,请指出错误。_________;_________( 写出两处即可)
(4)简述用水洗涤沉淀的操作过程_________________________.
(5)若产品中混有少量聚水杨酸,设计实验除去该杂质。
_______________________________________________________________.
27.烯烃通过臭氧氧化并经锌和水处理得到醛或酮。例如:
CH3CH2CH=C (CH3)2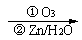 CH3CH2CH=O + O=C(CH3)2
CH3CH2CH=O + O=C(CH3)2
I.已知丙醛的燃烧热为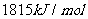 ,丙酮的燃烧热为
,丙酮的燃烧热为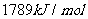 ,试写出丙醛燃烧的热化学方程式 。
,试写出丙醛燃烧的热化学方程式 。
II.上述反应可用来推断烯烃的结构。一种链状单烯烃A通过臭氧氧化并经锌和水处理得到B和C。化合物B含碳69.8%,含氢11.6%,B无银镜反应,催化加氢生成D。D在浓硫酸存在下加热,不能得到使溴水褪色的物质但可以得到唯一产物E。反应图示如下:
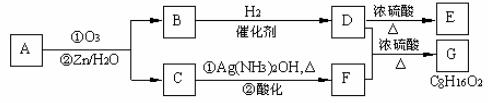
回答下列问题:
(1)B的相对分子质量是_____________
;F+D G的反应类型为_________D中含有官能团的名称______________ 。
G的反应类型为_________D中含有官能团的名称______________ 。
(2)写出C与银氨溶液反应的化学方程式(不需酸化):____________。
(3)A的结构简式为_____________ 。E的结构简式为__________.
(4)化合物A的某种同分异构体通过臭氧化并经锌和水处理只得到一种产物,符合该条件的异构体的结构简式有_______种。
26.已知某些非金属单质与强碱溶液会发生反应,如:
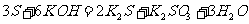
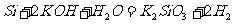
合金A由4种单质组成,经过一系列反应分别进入了沉淀或气体中.
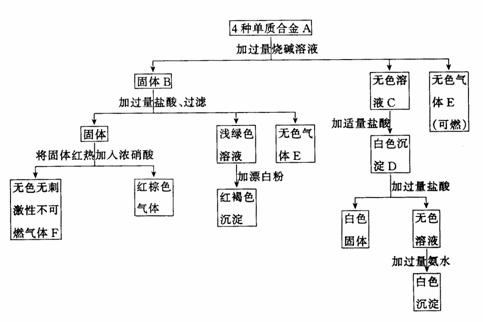
试回答:
(1)合金A由哪4种元素的单质组成?______、_____、____、______.
(2)写出固体B、溶液C、沉淀D有关组成的化学式:
B_________、C_________、D_________
(3)写出无色溶液C中某成分加入过量盐酸生成无色溶液的离子方程式:
__________________________________________
(4)气体F的电子式是___________.
(5)浅绿色溶液加入漂白粉生成红褐色沉淀的离子方程式______________________.
13.LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和锂,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是 ( )
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和锂,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是 ( )
A.可加入硫酸以提高电解质的导电性
B.放电时电池内部Li+向负极移动.
C.充电过程中,电池正极材料的质量减少
D.放电时电池负极反应为:FePO4+Li++e - =LiFePO4
第Ⅱ卷
12.碘钨灯比白炽灯使用寿命长。灯管内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应: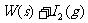
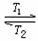
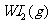
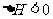 (温度T1<T2
(温度T1<T2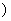 。下列说法正确的是 ( )
。下列说法正确的是 ( )
A.灯管工作时,扩散到灯丝附近高温区的WI2(g)会分解出W重新沉积到灯丝上
B.灯丝附近温度越高,WI2(g)的转化率越低
C.该反应的平衡常数表达式是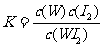
D.不能利用该反应原理提纯钨
11.镁、铝、铁三种金属组成的混合物与足量的稀硫酸反应,生成2.8L H2(标准状况),则三种金属的物质的量之和不可能是 ( )
A.0.12mol B.0.09 C.0.10mol D.0.08mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com