
8Ł®±ę׼״żöĎÂŁ¬ÄłÍ¬Ń§Ďň100mL H2S±ĄşÍČÜŇşÖĐͨČëSO2Ł¬ËůµĂČÜŇşpH±ä»ŻČçÍĽËůĘľˇŁĎÂÁĐ·ÖÎöÖĐŁ¬ŐýČ·µÄĘǡˇˇˇˇˇˇˇˇˇ ˇˇ (ˇˇ)
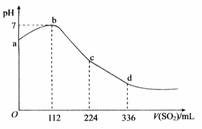
ˇˇˇˇˇˇ AŁ®bµă¶ÔÓ¦µÄČÜŇşµĽµçĐÔ×îÇż
ˇˇˇˇˇˇ BŁ®ŃÇÁňËáĘDZČÇâÁňËá¸üČőµÄËá
ˇˇˇˇˇˇ CŁ®ÔH2SČÜŇşµÄÎďÖʵÄÁżĹ¨¶ČÎŞ0.05molˇ¤LŁ1
ˇˇˇˇˇˇ DŁ®ab¶Î·´Ó¦ĘÇŁşSO2+2H2S====3Sˇý+2H2O
7Ł®ĎÂÁĐʵŃé˛Ů×÷ÍęČ«ŐýČ·µÄĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (ˇˇ)
ˇˇˇˇˇˇ AŁ®ĹäÖĆ100mL 0.1molˇ¤LŁ1µÄNaClČÜҺʱŁ¬ĎČÁżČˇ10mL 1molˇ¤LŁ1µÄNaClČÜŇşµąČëČÝÁżĆżÖĐŁ¬ÔŮĽÓˮϡĘÍÖÁżĚ¶ČĎß
ˇˇˇˇˇˇ BŁ®ĹäÖĆÂČ»ŻĚúČÜҺʱŁ¬˝«Ň»¶¨ÁżÂČ»ŻĚúČÜ˝âÔÚÉŮÁżĹ¨ŃÎËáÖĐŁ¬ÔŮÓĂˮϡĘÍ
ˇˇˇˇˇˇ CŁ®ÖƱ¸ŇŇËáŇŇőĄĘ±Ł¬˝«ŇŇ´ĽşÍŇŇËáŇŔ´ÎĽÓČ뵽ŨÁňËáÖĐ
ˇˇˇˇˇˇ DŁ®ŇŇ´ĽÓë˝đĘôÄƵķ´Ó¦Ł¬ÔÚʢÓĐÉŮÁżŇŇ´ĽČÜŇşµÄĘÔąÜÖĐŁ¬ĽÓČëһСżéĐÂÇеġ˘ÓĂÂËÖ˝˛Á¸É±íĂćĂşÓ͵ĽđĘôÄĆ
6Ł®ĎÖ´úÎŢ»ú»ŻŃ§¶ÔÁňŇ»µŞ»ŻşĎÎďµÄŃĐľżĘÇ×îÎŞ»îÔľµÄÁěÓň֮һˇŁĆäÖĐČçÍĽĘÇŇŃľşĎłÉµÄ×îÖřĂűµÄÁňŁµŞ»ŻşĎÎďµÄ·Ö×ӽṹˇŁĎÂÁĐ˵·¨ŐýČ·µÄĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (ˇˇ)
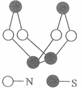
ˇˇˇˇˇˇ AŁ®¸ĂÎďÖʵķÖ×ÓʽΪSN
ˇˇˇˇˇˇ BŁ®¸ĂÎďÖʵķÖ×ÓÖĐĽČÓĐĽ«ĐÔĽüÓÖÓĐ·ÇĽ«ĐÔĽü
ˇˇˇˇˇˇ CŁ®¸ĂÎďÖĘľßÓкܸߵÄČۡ˘·Đµă
ˇˇˇˇˇˇ DŁ®¸ĂÎďÖĘÓ뻯şĎÎďS2N2»ĄÎŞÍ¬ËŘŇěĐÎĚĺ
29Ł®(15·Ö)ŇŃÖŞŁş
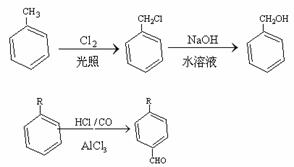
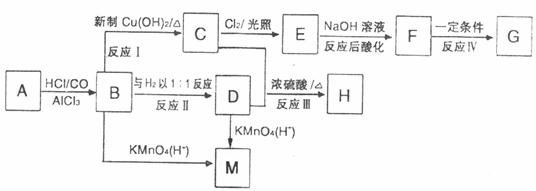
Čô´ÓAłö·˘żÉ·˘ÉúĎÂÍĽËůĘľµÄһϵÁĐ·´Ó¦Ł¬ĆäÖĐBµÄ·Ö×ÓʽΪ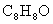 Ł¬Çұ˝»·ÉϵÄһԪȡ´úÎďÖ»ÓĐ2ÖÖŁ»GÎŞ¸ß·Ö×Ó»ŻşĎÎĘÔĚîĐ´ĎÂÁпհףş
Ł¬Çұ˝»·ÉϵÄһԪȡ´úÎďÖ»ÓĐ2ÖÖŁ»GÎŞ¸ß·Ö×Ó»ŻşĎÎĘÔĚîĐ´ĎÂÁпհףş
(1)Đ´łö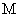 µÄ˝áąąĽňĘ˝ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
µÄ˝áąąĽňĘ˝ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
(2)Ö¸łö·´Ó¦˘óµÄ·´Ó¦ŔŕĐ͡ˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
(3)Đ´łöĎÂÁĐ·´Ó¦µÄ»ŻŃ§·˝łĚĘ˝Łş
 ˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
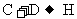 ˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
ˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
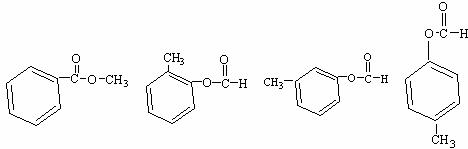
(4)ÓëC»ĄÎŞÍ¬·ÖŇěąąĚĺÇŇľůĘôÓÚőĄŔŕµÄ·ĽĎă×廯şĎÎﹲÓĐ6ÖÖŁ¬łýĎÂÁĐ4ÖÖÍ⣬ÁíÍâÁ˝ÖÖͬ·ÖŇěąąĚĺµÄ˝áąąĽňʽΪˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ˘ˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
28Ł®(15·Ö)ÇâŃő»ŻÍĘÇŇ»ÖÖłŁÓĂĘÔĽÁˇŁŔýČ磬ŔűÓĂĐÂÖĆÇâŃő»ŻÍŃéÖ¤ĆĎĚŃĚǵĻąÔĐÔˇŁ
IŁ®ĘµŃéĘŇÖĆȡĐÂÖĆÇâŃő»ŻÍĐü×ÇŇşµÄ˛Ů×÷·˝·¨ŁşÔÚĘÔąÜŔďĽÓČë10%µÄÇâŃő»ŻÄĆČÜŇş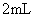 Ł¬µÎČë2%µÄÁňËáÍČÜŇş4µÎ-6µÎŁ¬Őńµ´Ľ´łÉˇŁŐâŃů˛Ů×÷µÄÄżµÄĘǡˇˇˇˇˇ ˇˇˇˇ
Ł¬µÎČë2%µÄÁňËáÍČÜŇş4µÎ-6µÎŁ¬Őńµ´Ľ´łÉˇŁŐâŃů˛Ů×÷µÄÄżµÄĘǡˇˇˇˇˇ ˇˇˇˇ
ˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇŁ
ĎÂĂćĘÇČý¸öŃĐľżĐÔѧϰ×é·Ö±đ´Ó˛»Í¬˛ăĂ濪չŃĐľżĐÔѧϰ»î¶ŻŁş
˘ňŁ®ŃĐľżĐÔѧϰС×éĽ×Łş¶Ô˝Ě˛ÄʵŃé˝áÂۡ°ŇŇČ©ÓëĐÂÖĆÇâŃő»ŻÍ·´Ó¦ÉúłÉµÄşěÉ«łÁµíĘÇ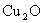 ˇ±ĚáłöÖĘŇÉŁ¬ËűĂÇČĎÎŞşěÉ«łÁµí˛»Ň»¶¨ĘÇŃő»ŻŃÇ͡ŁÎŞÁËČ·¶¨şěÉ«łÁµíµÄłÉ·ÖŁ¬żŞŐąÁËČçĎÂŃĐľżŁşĚáłö˛ÂĎ룺
ˇ±ĚáłöÖĘŇÉŁ¬ËűĂÇČĎÎŞşěÉ«łÁµí˛»Ň»¶¨ĘÇŃő»ŻŃÇ͡ŁÎŞÁËČ·¶¨şěÉ«łÁµíµÄłÉ·ÖŁ¬żŞŐąÁËČçĎÂŃĐľżŁşĚáłö˛ÂĎ룺
˛éÔÄ×ĘÁĎŁş˘ŮŃő»ŻŃÇÍĘôÓÚĽîĐÔŃő»ŻÎ˘Ú+1ĽŰµÄÍŔë×ÓÔÚËáĐÔĚőĽţŇ×·˘Éú×ÔÉíŃő»Ż»ąÔ·´Ó¦Ł»˘ŰÔÚżŐĆřÖĐ×ĆÉŐŃő»ŻŃÇÍÄÜÉúłÉŃő»ŻÍˇŁ
ÉčĽĆ·˝°¸Łş
·˝°¸1ŁşČˇ¸ĂşěÉ«łÁµíČÜÓÚ×ăÁżµÄϡĎőËáÖĐŁ¬ąŰ˛ěČÜŇşŃŐÉ«±ä»Ż
·˝°¸2ŁşČˇ¸ĂşěÉ«łÁµíČÜÓÚ×ăÁżµÄϡÁňËáÖĐŁ¬ąŰ˛ěĘÇ·ńÓвĐÔü
·˝°¸3ŁşłĆȡşěÉ«łÁµí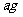 Ł¬ÔÚżŐĆřÖĐłä·Ö×ĆÉŐÖÁÍęČ«±äşÚŁ¬˛˘ÔÚ¸ÉÔďĆ÷ŔďŔäČ´Ł¬ÔŮłĆÖŘŁ¬·´¸´¶ŕ´ÎÖ±µ˝ąĚĚĺşăÖŘŁ¬łĆµĂÖĘÁżÎŞ
Ł¬ÔÚżŐĆřÖĐłä·Ö×ĆÉŐÖÁÍęČ«±äşÚŁ¬˛˘ÔÚ¸ÉÔďĆ÷ŔďŔäČ´Ł¬ÔŮłĆÖŘŁ¬·´¸´¶ŕ´ÎÖ±µ˝ąĚĚĺşăÖŘŁ¬łĆµĂÖĘÁżÎŞ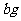 Ł¬±Č˝Ď
Ł¬±Č˝Ď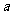 ˇ˘
ˇ˘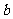 µÄ´óСąŘϵ
µÄ´óСąŘϵ
·˝°¸4ŁşČˇşěÉ«ąĚĚĺłÁµí×°ČëĘÔąÜŔĽÓČëËữµÄĎőËáŇřČÜŇşŁ¬ąŰ˛ěĘÇ·ńÓĐŇř°×É«ŇřÎöłö
ÄăČĎÎŞşĎŔíµÄ·˝°¸Ęǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
ˇˇˇˇ ˘óŁ®ŃĐľżĐÔѧϰС×éŇŇŐë¶ÔС×éĽ×µÄÖĘŇÉŁ¬ÉčĽĆеÄĚ˝ľż·˝°¸Ł¬×°ÖĂČçĎÂÍĽËůĘľˇŁÄăČĎÎŞŇŞ˛â¶¨ÉĎĘöşěÉ«łÁµíłÉ·Ö±ŘĐë˛â¶¨ĎÂÁĐÄÄĐ©ÎďŔíÁżŁşˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇŁ
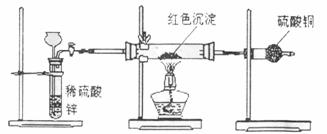
ˇˇˇˇ ˘ŮͨČëÇâĆřµÄĚĺ»ýŁ»˘Ú·´Ó¦Ç°Ł¬şěÉ«łÁµí+Ó˛ÖĘĘԹܵÄ×ÜÖĘÁżŁ»˘ŰÍęČ«·´Ó¦şóŁ¬şěÉ«ąĚĚĺ+Ó˛ÖĘĘԹܵÄ×ÜÖĘÁżŁ»˘ÜʵŃéÇ°Ł¬¸ÉÔďąÜµÄÖĘÁżŁ»˘ÝÓ˛ÖĘĘԹܵÄÖĘÁżŁ»˘ŢĐżÁŁµÄÖĘÁżŁ»˘ßϡÁňËáÖĐş¬ČÜÖʵÄÁżŁ»˘ŕʵŃéşóŁ¬¸ÉÔďąÜµÄÖĘÁż
˘ôŁ®ŃĐľżĐÔѧϰС×é±űÉĎÍř˛éÔÄĐÂÎŵĂÖŞˇ°2005Äęŵ±´¶ű»ŻŃ§˝±ĘÚÓčÁËČýλŃĐľżÂĚÉ«»ŻŃ§µÄżĆѧĽŇˇ±ˇŁÂĚÉ«»ŻŃ§Çżµ÷¶Ô»·ľłÓѺã¬ĘµĎÖÁăĹŷšŁˇ°±ä·ĎÎŞ±¦ˇ±·űşĎÂĚÉ«»ŻŃ§ŇŞÇóˇŁËűĂÇĘŐĽŻÉĎĘöşěÉ«łÁµíÓĂÓÚÖƱ¸»ŻŃ§ĘÔĽÁ--Ŕ¶·ŻˇŁÇëÄ㽫ËűĂÇÉčĽĆµÄŇ»¸öĽňµĄÇŇ·űşĎÂĚÉ«»ŻŃ§ŇŞÇóµÄʵŃé·˝°¸˛ąłäÍęŐűŁş
ÔÚżŐĆřÖĐłä·Ö×ĆÉոúěÉ«ąĚĚĺÖÁČ«˛ż×Ş»ŻłÉşÚÉ«Ńő»ŻÍŁ¬ÔŮĽÓČë×ăÁżˇˇˇˇ ˇˇˇˇˇˇˇˇ
(ĚîÎďÖĘĂűłĆ)łä·Ö·´Ó¦Ł¬ĽÓČČŐô·˘Ĺ¨Ëőˇ˘ˇˇˇˇ ˇˇˇˇˇˇˇˇˇ˘ąýÂˡ˘ˇˇˇˇ ˇˇˇˇˇˇˇˇŁ¬ÓĂÂËÖ˝Îü¸É»ňͨČë¶čĐÔĆřĚĺ´ř×ßË®·ÖĽ´żÉˇŁ
27Ł®(15·Ö)ĎÂÍĽ±íĘľ¸÷ÎďÖĘÖ®ĽäµÄת»ŻąŘϵˇŁŇŃÖŞŁşAˇ˘Dˇ˘Fˇ˘HľůÎŞµĄÖĘŁ¬XłŁÎÂĎÂÎŞÎŢÉ«ŇşĚ壬BÎŞµ»ĆÉ«ąĚĚ壬JČÜÓÚËáµĂµ˝»ĆÉ«ČÜŇşˇŁ
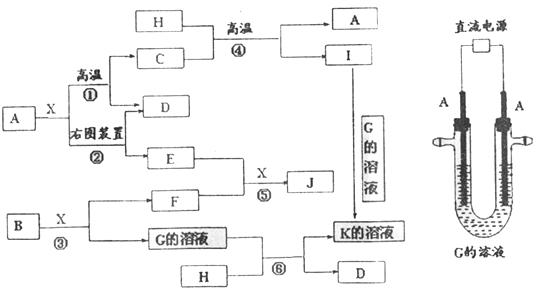
Çë°´ŇŞÇóĚîżŐŁş
(1)Đ´łöBµÄµç×ÓĘ˝Łşˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
(2)Đ´łöÉúłÉEµÄµçĽ«·´Ó¦Ę˝Łşˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ¬·´Ó¦˘ÝµÄĎÖĎóĘǡˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
(3)·´Ó¦˘ŮµÄ»ŻŃ§·˝łĚĘ˝Ęǡˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ¬ÔÚʵŃéĘŇÖĐŇý·˘·´Ó¦˘ÜµÄ˛Ů×÷Ęǡˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
(4)·´Ó¦˘ŢµÄŔë×Ó·˝łĚĘ˝Ęǡˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
26Ł®(15·Ö)ąýŃőŇŇËá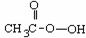 ĘÇąăÎŞĘąÓõÄĎű¶ľĽÁˇŁËüżÉÓÉ
ĘÇąăÎŞĘąÓõÄĎű¶ľĽÁˇŁËüżÉÓÉ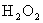 şÍ±ů´×Ëá·´Ó¦ÖĆȡŁ¬ËůŇÔÔÚąýŃőŇŇËáÖĐłŁş¬ÓвĐÁôµÄ
şÍ±ů´×Ëá·´Ó¦ÖĆȡŁ¬ËůŇÔÔÚąýŃőŇŇËáÖĐłŁş¬ÓвĐÁôµÄ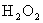 ˇŁ˛â¶¨˛úĆ·ÖĐąýŃőŇŇËáŨ¶Č
ˇŁ˛â¶¨˛úĆ·ÖĐąýŃőŇŇËáŨ¶Č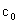 µÄ·˝·¨şÍ˛˝ÖčČçĎÂŁş
µÄ·˝·¨şÍ˛˝ÖčČçĎÂŁş
ˇˇˇˇˇˇˇˇ ȡ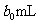 ´ý˛âŇşŁ¬ÓĂÁňËáĘąČÜŇşËữŁ¬ÔŮÓĂŨ¶ČÎŞ
´ý˛âŇşŁ¬ÓĂÁňËáĘąČÜŇşËữŁ¬ÔŮÓĂŨ¶ČÎŞ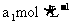 µÄ
µÄ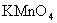 ±ę׼ČÜŇşµÎ¶¨ĆäÖеÄ
±ę׼ČÜŇşµÎ¶¨ĆäÖеÄ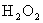 Ł¬şÄÓĂ
Ł¬şÄÓĂ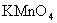 ČÜŇşµÄĚĺ»ýÎŞ
ČÜŇşµÄĚĺ»ýÎŞ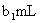 ˇŁ(¸Ă·´Ó¦ĽÇÎŞ˘ŮŁ¬µÎ¶¨ąýłĚÖĐ
ˇŁ(¸Ă·´Ó¦ĽÇÎŞ˘ŮŁ¬µÎ¶¨ąýłĚÖĐ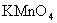 ˛»ÓëąýŃőŇŇËá·´Ó¦Ł¬
˛»ÓëąýŃőŇŇËá·´Ó¦Ł¬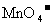 µÄ»ąÔ˛úÎďĘÇ
µÄ»ąÔ˛úÎďĘÇ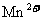 )ˇŁ
)ˇŁ
Áíȡ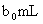 ´ý˛âŇşŁ®ĽÓČëąýÁżµÄ
´ý˛âŇşŁ®ĽÓČëąýÁżµÄ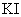 Ł¬˛˘ÓĂÁňËáĘąČÜŇşËữŁ¬´ËʱąýŃőŇŇËáşÍ˛ĐÁôµÄ
Ł¬˛˘ÓĂÁňËáĘąČÜŇşËữŁ¬´ËʱąýŃőŇŇËáşÍ˛ĐÁôµÄ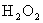 ¶ĽÄܸú
¶ĽÄܸú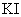 ·´Ó¦ÉúłÉ
·´Ó¦ÉúłÉ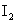 (Ç°şóÁ˝¸ö·´Ó¦·Ö±đĽÇÎŞ˘ÚşÍ˘Ű)ˇŁÔŮÓĂŨ¶ČÎŞ
(Ç°şóÁ˝¸ö·´Ó¦·Ö±đĽÇÎŞ˘ÚşÍ˘Ű)ˇŁÔŮÓĂŨ¶ČÎŞ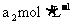 µÄ
µÄ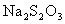 ±ę׼ČÜŇşµÎ¶¨ÉúłÉµÄ
±ę׼ČÜŇşµÎ¶¨ÉúłÉµÄ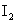 Ł¬şÄÓĂ
Ł¬şÄÓĂ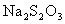 ČÜŇşĚĺ»ýÎŞ
ČÜŇşĚĺ»ýÎŞ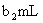 (·´Ó¦˘Ü
(·´Ó¦˘Ü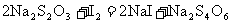 )ˇŁ
)ˇŁ
ˇˇˇˇ (1)Đ´łöÉĎĘö·´Ó¦˘Ůˇ˘˘Úˇ˘˘ŰµÄŔë×Ó·´Ó¦·˝łĚĘ˝
˘Ůˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇ˘Úˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇ˘Űˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
(2)ÓĂ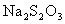 ±ę׼ČÜŇşµÎ¶¨
±ę׼ČÜŇşµÎ¶¨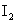 ʱŁ¬ŃˇÓõÄָʾĽÁĘǡˇˇˇˇˇ ˇˇˇˇˇˇˇŁÇë¸ůľÝÉĎĘöʵŃéĘýľÝĽĆËăąýŃőŇŇËáµÄŨ¶Č(ÓĂş¬
ʱŁ¬ŃˇÓõÄָʾĽÁĘǡˇˇˇˇˇ ˇˇˇˇˇˇˇŁÇë¸ůľÝÉĎĘöʵŃéĘýľÝĽĆËăąýŃőŇŇËáµÄŨ¶Č(ÓĂş¬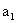 ˇ˘
ˇ˘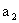 ˇ˘
ˇ˘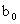 ˇ˘
ˇ˘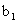 ˇ˘
ˇ˘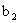 µÄ´úĘýĘ˝±íĘľ)
µÄ´úĘýĘ˝±íĘľ)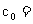 ˇˇˇˇ ˇˇˇˇˇˇˇŁ
ˇˇˇˇ ˇˇˇˇˇˇˇŁ
(3)ÎŞĽĆËă´ý˛âŇşÖĐąýŃőŇŇËáµÄŨ¶Č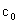 Ł¬ĽÓČëµÄ
Ł¬ĽÓČëµÄ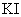 µÄÖĘÁżŇŃąýÁżµ«Ă»ÓĐ׼ȷłĆÁżŁ¬ĘÇ·ńÓ°Ďě˛â¶¨˝áąűˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇ(ĚĘǡ±»ňˇ°·ńˇ±)ˇŁ
µÄÖĘÁżŇŃąýÁżµ«Ă»ÓĐ׼ȷłĆÁżŁ¬ĘÇ·ńÓ°Ďě˛â¶¨˝áąűˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇ(ĚĘǡ±»ňˇ°·ńˇ±)ˇŁ
13Ł®łŁÎÂĎÂŁ¬ĎňŇ»¶¨Ěĺ»ý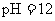 µÄ
µÄ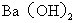 ČÜŇşÖĐŁ¬ÖđµÎĽÓČëŇ»¶¨ÎďÖʵÄÁżĹ¨¶ČµÄ
ČÜŇşÖĐŁ¬ÖđµÎĽÓČëŇ»¶¨ÎďÖʵÄÁżĹ¨¶ČµÄ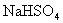 ČÜŇşŁ¬µ±ČÜŇşÖеÄ
ČÜŇşŁ¬µ±ČÜŇşÖеÄ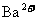 ǡşĂÍęČ«łÁµíʱŁ¬ČÜŇş
ǡşĂÍęČ«łÁµíʱŁ¬ČÜŇş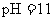 ˇŁČô·´Ó¦şóČÜŇşµÄĚĺ»ýµČÓÚ
ˇŁČô·´Ó¦şóČÜŇşµÄĚĺ»ýµČÓÚ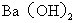 ČÜŇşÓë
ČÜŇşÓë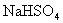 ČÜŇşĚĺ»ýÖ®şÍŁ¬Ôň
ČÜŇşĚĺ»ýÖ®şÍŁ¬Ôň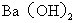 ČÜŇşşÍ
ČÜŇşşÍ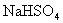 ČÜŇşµÄĚĺ»ýÖ®±ČĘÇŁş
ČÜŇşµÄĚĺ»ýÖ®±ČĘÇŁş
ˇˇˇˇ AŁ®1Łş9ˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ BŁ®1Łş1 ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ CŁ®1Łş2ˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®1Łş4
·ÇѡÔńĚâ
12Ł®ÓɶĚÖÜĆÚÔŞËŘąąłÉµÄÄłŔë×Ó»ŻşĎÎďÖĐŁ¬Ň»¸öŃôŔë×ÓşÍŇ»¸öŇőŔë×ÓşËÍâµç×ÓĘýÖ®şÍÎŞ20ˇŁĎÂÁĐ˵·¨ÖĐŐýČ·µÄĘÇ(ˇˇˇˇ )
ˇˇˇˇ AŁ®ľ§ĚĺÖĐŃôŔë×ÓşÍŇőŔë×Ó¸öĘýŇ»¶¨ĎŕµČ
BŁ®ľ§ĚĺÖĐŇ»¶¨ş¬ÓĐŔë×ÓĽüŁ¬żÉÄÜş¬ÓĐą˛ĽŰĽü
ˇˇˇˇ CŁ®Ëůş¬ÔŞËŘŇ»¶¨˛»ÔÚͬһÖÜĆÚŁ¬Ň˛˛»ÔÚµÚŇ»ÖÜĆÚ
ˇˇˇˇ DŁ®ľ§ĚĺÖĐŃôŔë×Ӱ뾶һ¶¨´óÓÚŇőŔë×Ӱ뾶
11Ł®Iˇ˘ÔÚŇ»¶¨Î¶ČĎÂŁ¬ĎňŇ»¸öČÝ»ý˛»±äµÄČÝĆ÷ÖĐŁ¬ĽÓČë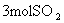 şÍ
şÍ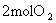 Ľ°ąĚĚĺ´ß»ŻĽÁŁ¬ĘąÖ®·˘Éú·´Ó¦Łş
Ľ°ąĚĚĺ´ß»ŻĽÁŁ¬ĘąÖ®·˘Éú·´Ó¦Łş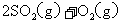

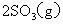 Ł»
Ł»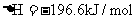 ˇŁĆ˝şâʱČÝĆ÷ÄÚĆřĚĺѹǿΪĆđʼʱµÄ90%ˇŁ
ˇŁĆ˝şâʱČÝĆ÷ÄÚĆřĚĺѹǿΪĆđʼʱµÄ90%ˇŁ
ˇˇ ˇˇ˘ňˇ˘±ŁłÖͬһ·´Ó¦Î¶ȣ¬ÔÚĎŕͬČÝ»ýµÄČÝĆ÷ÖĐŁ¬˝«ĆđĘĽÎďÖʵÄÁż¸ÄÎŞ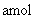
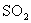 ˇ˘
ˇ˘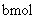
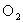 ˇ˘
ˇ˘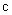
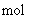
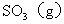
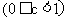 Ł¬·´Ó¦´ďµ˝Ć˝şâʱ
Ł¬·´Ó¦´ďµ˝Ć˝şâʱ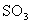 µÄĚĺ»ý·ÖĘýÎŞ
µÄĚĺ»ý·ÖĘýÎŞ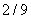 ˇŁIÓë˘ň·ĹłöµÄČČÁż±Č˝ĎŐýČ·µÄĘÇ(ˇˇˇˇ )
ˇŁIÓë˘ň·ĹłöµÄČČÁż±Č˝ĎŐýČ·µÄĘÇ(ˇˇˇˇ )
ˇˇˇˇ AŁ®Ň»¶¨ĎŕµČˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ BŁ®Ç°ŐßŇ»¶¨ĐˇÓÚşóŐß
ˇˇˇˇ CŁ®Ç°Őß´óÓÚ»ňµČÓÚşóŐߡˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®Ç°ŐßСÓÚ»ňµČÓÚşóŐß
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com