
18.等物质的量的下列化合物在相应条件下完全分解后得到氧气最多是 ( )
A.KClO3(加MnO2催化剂,加热) B.KMnO4(加热)
C.H2O2(水溶液,加MnO2催化剂) D.HgO(加热)
17.由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;
③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是 ( )
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
16.下述实验能达到预期目的的是 ( )
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入酸性KMnO4溶液中 |
证明SO2具有漂白性 |
|
B |
将Cl2通入NaBr溶液中 |
比较氯与溴的还原性强弱 |
|
C |
将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 |
研究温度对化学平衡的影响 |
|
D |
分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 |
研究催化剂对H2O2分解速率的影响 |
15.向含有0.078molFeCl2的溶液中通入0.009mol Cl2,再向其中加入含0.01mol X2O2-7的酸性溶液,使溶液的Fe2+恰好被氧化,且X2O2-7被还原为Xn+,则n值为 ( )
A.2 B.3 C.4 D.5
14.将V1mL 1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测得并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )
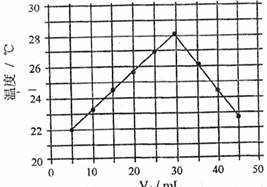
A.做该实验时环境温度为22℃
B.该实验表明有水生成的反应都是放热反应
C.NaOH溶液的浓度约为1.0mol/L
D.用该图表的数据即可粗略计算出HCl溶液和NaOH溶液的中和热
13.下列各组离子一定能大量共存的是( )
A.在含有大量AlO-2的溶液中:NH+4、Na+、Cl-、H+
B.在强碱性溶液中:Na+、SO2-3、NO-3、AlO2-
C.由水电离出的H+浓度为10-13mol/L的溶液中:NH+4、Cl-、Na+、NO-3
D.常温下,在c(OH-)=10-13mol/L的溶液中:Na+、Cl-、I-、NO-3
12.白磷和氧气可以发生反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P a kJ/mol、P-O b kJ/mol、P=O ckJ/mol、O-O d kJ/mol。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
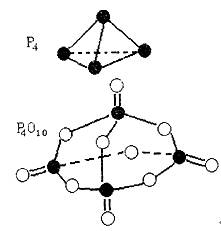
A.(6a+5d-4c-12b)kJ/mol
B.(4c+12b-6a-5d)kJ/mol
C.(4c+12b-4a-5d)kJ/mol
D.(4a+5d-4c-12b)kJ/mol
11.将质量分数为0.052(5.2%)的NaOH溶液1L(密度为1.06g/cm3)用铂电极电解,当溶液中NaOH的质量分数改变了0.010(1.0%)时停止电解,则此时溶液中应符合的关系是
( )
|
|
NaOH的质量分数 |
阳极析出物的质量/g |
阴极析出的质量/g |
|
A |
0.062(6.2%) |
19 |
152 |
|
B |
0.062(6.2%) |
152 |
19 |
|
C |
0.042(4.2%) |
1.2 |
9.4 |
|
D |
0.042(4.2%) |
9.4 |
1.2 |
10.按下述实验方法制备气体,合理又实用的是 ( )
A.锌粒与稀HNO3反应制备H2
B.向饱和NaCl溶液中滴加浓H2SO4制备HCl
C.亚硫酸钠与浓H2SO4反应制备SO2
D.大理石与浓H2SO4反应制备CO2
9.白酒、食醋、蔗糖、淀粉等均匀为家庭厨房中常用的物质,利用这些物质能完成的实验是:①检验自来水中是否含氯离子 ②鉴别食盐和小苏打 ③蛋壳能否溶于酸 ④白酒中是否含甲醇 ( )
A.①② B.①④ C.②③ D.③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com