
7.将3.48g四氧化三铁完全溶解在100mL1mol/L的硫酸中,然后加入K2Cr2O7溶液25mL,恰好使溶液中的铁元素全部转化为Fe3+,Cr2O72-全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度是 ( )
A.0.05mol/L B.0.1 mol/L C.0.2 mol/L D.0.3 mol/L
6.将a%的酒精和(100-a)%的乙醇溶液等体积混合后所得乙醇溶液的质量分数可为( )
A.大于50% B.小于50%
C.小于或等于50% D.大于或等于50%
5.向饱和的NaCl的溶液中通入足量的NH3后,再通入足量的CO2,则该溶液中还可能大量存在的离子组 ( )
A.Na+、Cl-、HCO3- B.HCO3-、H+、NH4+
C.NH4+、H+、CO32- D.Na+、CO32-、OH-
4.有两种有机物以一定比例混合,一定条件下在aL O2(足量)中燃烧,充分反应后恢复到原状态,再通过足量Na2O2层,得到相同条件下气体大于aL,下列混合物中符合此条件的是 ( )
A.CH4、C2H4 B.CH3OH、CH3COOH
C.C2H6、HCHO D.HCHO、HCOOH
3.氯水在下列场合中,既表现氧化性,又表现还原性的是 ( )
A.使品红溶液褪色 B.与烧碱溶液反应
C.与FeCl2溶液反应 D.与AgNO3溶液反应
2.Na2FeO4是一种高效多功能水处理剂,应用前景广阔。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。对此反应下列说法中不正确的是 ( )
A.Na2O2 在此反应中只做氧化剂
B.O2是氧化剂
C.Na2FeO4既是氧化产物又是还原产物
D.2molFeSO4发生反应时,共有10mol电子转移
1.下列观点你不赞成的是 ( )
A.氢气让人喜欢让人忧
B.煤为人类提供了能源和化工原料的同时,也埋下了祸根
C.煤气化能提高市民的生活质量,同时也是潜伏着的无形杀手
D.水虽然是取之不尽的,但是个别地区存在用水危机
34.(12分) 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代。处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
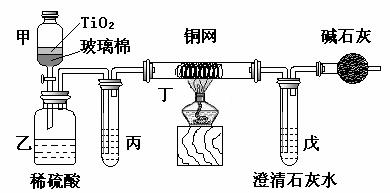
将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
⑴乙中反应的离子方程式为__________________________________
⑵乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是______(填字母)
a.饱和食盐水 b.饱和NaHCO3溶液 c.浓NaOH溶液 d.浓硫酸
⑶丁在实验中的作用是____________________________
装有碱石灰的干燥管的作用是____________________________
⑷戊中盛有含Ca(OH)20.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于________
请说明该测得值与实际处理的百分率相比偏高还是偏低_________?简要说明可能的原因________________________________________________________。
⑸请提出一个能提高准确度的建议(要有可操作性,不宜使操作变得过于复杂)
_________________________________________________________________________
33.(10分)下图是无机物A-M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是第三周期元素组成的单质中熔点最高的金属,K是一种气体。
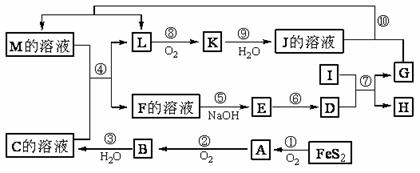
请填写下列空白:
(1)组成单质G的元素在周期表中的位置____________。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为________。
(3)在反应②、③、⑥、⑨中,既属于化合反应又能属于非氧化还原反应的是 (填写序号)。
(4)反应④的离子方程式是: 。
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是: 。
32.(10分)L、M、R、P、Q分别代表五种含不同化合价氮元素的常见物质,A、B分别代表两种含不同化合价的氯元素的物质(每种物质中,氮或氯元素的化合价只有一种),又知物质M中的氮元素的化合价要比物质Q中氮元素的化合价低。在一定条件下,它们会发生如下的转化(关系式未配平)。
①P+A→Q+B ②L+O2→M+H2O ③L+M→R+H2O ④B+H2O→A+O2
(1)若五种氮元素的物质中,有一种是硝酸,则硝酸是 ,理由是 。
(2)反应②必须在催化剂作用下,加热到一定温度时方能发生.此反应在化工生产上有重要用途。据此推断在同温、同压下,若物质R的密度比二氧化碳的密度小,则R的化学式为 。
(3)某学生写出下面三个含氮元素的物质的相互转化的关系式
A.M + P→N2O3 + H2O B.N2O +H2O → P + M C.M+L → Q + H2O
其中一定不可能实现的是 ,理由是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com