
16.某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:
A(g)+xB(g)  2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如下图所示。下列说法中正确的是 ( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如下图所示。下列说法中正确的是 ( )
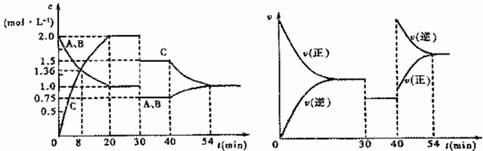
A.30min时降低温度,40min时升高温度
B.8min前A的平均反应速率为0.08mol·L-1·min-1
C.反应方程式中的x=1,正反应为吸热反应
D.该反应20min~30min的平均常数比30min~40min的平衡常数大
第Ⅱ卷 (非选择题 共52分)
15.氢化亚铁(CuH)是一种难容物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它。CuH不稳定,易分解;CuH在氯气中能燃烧;跟盐酸反应能产生气体,以下有关的推断中错误的是 ( )
A.“另一种反应物”一定具有还原性 B.CuH既可做氧化剂也可做还原剂
C.CuH+Cl2===CuCl+HCl(燃烧) D.CuH+HCl===CuCl+H2↑(常温)
1.3×10-35mol·L-1
C.因为H2SO4是强酸,故Cu2++H2S=CuS↓+2H+不能发生
D.除去工业废水中的Cu2+,可以选用FeS做沉淀剂
14.已知如下物质的溶度积常数:FeS:Ksp=6.3×10-18mol2·L-2;CuS:Ksp=1.3×10-36
mol2·L-2;ZnS:Ksp=1.6×10-24mol2·L-2。下列说法正确的是 ( )
A.同温度下,CuS的溶解度大于ZnS的溶解度
B.将足量CuSO4溶解在0.1mol·L-1的H2S溶液中,Cu2+能达到的最大浓度为
13.一种碳纳米管(氢气)二次电池原理如下图,该电池的电解质为6mol·L-1KOH溶液,下列说法不正确的是 ( )
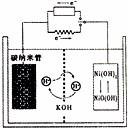
A.储存H2的碳纳米管放电时为负极,充电时为阴极
B.放电时负极附近pH减小
C.放电时电池正极的电极反应为:NiO(OH)+H2O+e-===Ni(OH) 2+OH-
D.放电时,电池反应为:2H2+O2===2H2O
12.下列离子方程式正确的是 ( )
A.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-===BaCO3↓+H2O
B.碳酸氢铵和氢氧化钠的反应:NH4+、+OH-===NH3↑+H2O
|
D.少量SO2通入Ca(ClO) 2溶液中:SO2+H2O+Ca2++2ClO-===CaSO3↓+2HClO
11.下列各组离子在给定条件下能大量共存的是 ( )
A.在pH=1溶液中:NH4+、K+、ClO-、Cl-
B.有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I-
C.加入铝粉能放出氢气的溶液中:K+、Ba2+、Cl-、Br-
D.在含有大量[Al(OH) 4] -的溶液中:NH4+、Na+、Cl-、H+
10.某同学为验证溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能得到的正确结论是( )
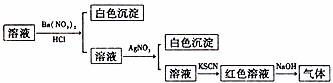
A.原溶液中一定含有SO42-离子 B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子
9.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的 是 ( )
A.由mXa+与nYb-,得m+a=n-b
B.X2-的还原性一定大于Y-
C.X、Y一定不是同周期元素
D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY
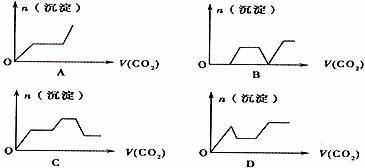
8.将足量的CO2不断通入KOH、Ba(OH) 2、K[Al(OH)4](KAlO2)的混合溶液中,生成沉淀与通入CO2的量的关系可表示为 ( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com