
13.常温时,以下4种溶液pH最小的是
A.0.01mol·L−1醋酸溶液
B.0.02mol·L−1醋酸与0.02mol·L−1 NaOH溶液等体积混合液
C.0.03mol·L−1醋酸与0.01mol·L−1 NaOH溶液等体积混合液
D.pH=2的盐酸与pH=12的NaOH溶液等体积混合液
第II卷 非选择题部分
12.下列各组离子一定能大量共存的是
A.含有大量Fe3+的溶液中:NH4+、Na+、I−、SCN−
B.在强碱溶液中:Na+、K+、AlO2−、CO32−
C.在c(H+)=1×10−13mol·L−1的溶液中:NH4+、Al3+、SO42−、NO3−
D.在pH=1的溶液中:K+、Fe2+、Cl−、NO3−
11.设阿伏加德常数为NA。则下列说法正确的是
A.7.8g Na2O2与足量水反应时,转移的电子数为0.2NA
B.25℃、1.01×105Pa条件下,11.2L丙炔分子中所含碳氢键数为2NA
C.常温下,2.7g铝分别与足量的盐酸或烧碱溶液反应时,失去的电子数都为0.3NA
D.常温下,1L 0.1mol·L−1CH3COOH溶液中含CH3COO−数为0.1NA
10.下列装置中,不能说明锌比铜活泼的是
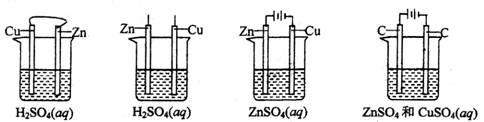
A B C D
9.下列离子方程式书写正确的是
A.金属钠与水反应:Na+2H2O==Na++2OH−+H2↑
B.大理石与稀盐酸反应:CO32−+2H+==CO2↑+H2O
C.氯化铁溶液与氨水反应:Fe3++3OH−==Fe(OH)3↓
D.碳酸氢钙溶液中加入少量烧碱溶液:Ca2++HCO3−+OH−==CaCO3↓+H2O
8.在下列条件下,两种气体的分子数一定相等的是
A.同质量不同密度的C2H4和CO B.同温度同体积的C2H6和NO
C.同温度同压强的CO和N2 D.同体积、同压强的N2和C2H4
7.美国康乃尔大学的魏考克斯(C. Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.因而称为释迦牟尼分子(所有原子在同一平面).有关该有机分子的说法正确的是
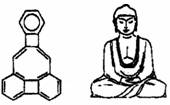
A.该有机物不属于芳香烃
B.该有机物属于苯的同系物
C.该有机物分子中含有22个碳原子
D.该有机物一氯代物只有3种
6.NaH是一种离子化合物,它跟水反应的方程式:NaH+H2O→NaOH+H2↑,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气.下列有关NaH的叙述错误的是
A.跟水反应时,水作氧化剂 B.NaH中氢离子半径比锂离子半径小
C.跟液氨反应时,有NaNH2生成 D.跟乙醇反应时,NaH被氧化
21、(8分)
2008年我国南方地区遭受了历史上罕见的特大的冰雪,交通堵塞,电网中断,给群众的生活带来很多困难。化学试剂氯化钙作为融雪剂在抗雪灾中起了一定的作用。氯化钙是用途广泛的化学试剂,可作干燥剂、冷冻剂、防冻剂等。为了测定某氯化钙样品中钙的含量,进行如下实验:
①准确称取氯化钙样品0.2312 g,放入烧杯中,加入适量6 mol/L的盐酸和适量蒸馏水使样品完全溶解,再滴加35.00 mL 0.25 mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。②过滤并洗涤①所得沉淀。③加入足量的10% H2SO4和适量的蒸馏水,④中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热加入0.05 mol/L KMnO4溶液16 .00mL,恰好完全反应。
回答下列问题:
(1)配平: MnO4-+ H2C2O4+ H+― Mn2++ CO2↑+ H2O
(2)0.05mol·L-1KMnO4标准溶液应置于 (选填“酸式”或“碱式”)滴定管中;判断滴定终点的现象为
。
(3)计算该氯化钙样品中钙元素的质量分数为 (精确到0.01%)。
20.(12分)
某学习小组用下图装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
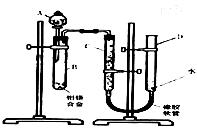
(1)B中发生反应的离子方程式为 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是 。然后将其洗涤,干燥,称重。
(3)实验按如下操作的顺序进行,请补充:
① 按上图连接好装置。
② 检查气密性,具体操作方法为
。
③ 将药品和水装入各仪器中,连接好装置,记录C的液面位置;
④ 由A向B中滴加足量试剂;
⑤ 待B中不再有气体产生并恢复至室温后,记录C的液面位置;记录C的液面位置时,除视线平视外,还应 。
⑥ 将B中剩余物质过滤,洗涤,干燥,称重。
(4)若实验用去铝镁合金的质量为a g,测得氢气体积为b ml(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为 。
(5)实验步骤⑥中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将 。
(填“偏大”、“偏小”、“不受影响”) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com