
29£®(10·Ö)ĪŖ·ĄÖ¹µāȱ·¦²”£¬Ķس£ŌŚŹ³ŃĪÖŠ¼ÓČė”°µā”±”£±ķÖŠŹĒŹ³ÓƵāŃĪ°ü×°ÉĻµÄ²æ·ÖĖµĆ÷£¬Ēėøł¾Ż“Ė±ķ£¬½įŗĻ»ÆѧѧæʵÄÖŖŹ¶£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
|
ÅäĮĻ |
¾«ŃĪ”¢µāĖį¼Ų”¢æ¹½į¼Į |
|
µāŗ¬Įæ |
20”×40mg/Kg |
|
“¢“ę·½·Ø |
ĆÜ·ā”¢±Ü¹ā”¢·Ą³± |
|
Ź³ÓĆ·½·Ø |
ÅėāæŹ±£¬“żŹ³Ę·Źģŗó¼ÓČėµāŃĪ |
(1)øł¾Żŗ¬µāŃĪµÄŹ³ÓĆ·½·ØæÉĶĘ²āĘä»ÆѧŠŌÖŹ”””””””””””””””””””””” ”£
(2)ŅŖ¼ģŃéŹ³ŃĪÖŠŹĒ·ńŗ¬ÓŠµāŌŖĖŲ£¬æÉŅŌŌŚŹ³ŃĪČÜŅŗÖŠ¼ÓČėµķ·Ūµā»Æ¼ŲČÜŅŗŗĶĻ”ĮņĖį£¬Čē¹ūČÜŅŗ±äĄ¶É«¼“æÉÖ¤Ć÷”£øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ”””””””””””””””””””””””””””””””” £¬ČōŅŖČ·ČĻŹ³ŃĪÖŠ»¹ŗ¬ÓŠK+£¬·½·ØŹĒ”””””””””””””””””””””””””””””””””””””””””””” ”£
(3)Ä³ŃŠ¾æŠ”×é¶ŌøƵāŃĪ½ųŠŠĮĖ·ÖĪö£ŗ³ĘČ”40.0gµāŃĪÅä³É100mlČÜŅŗ£¬Č”20.00mløĆČÜŅŗӌ׶ŠĪĘæÖŠ£¬Ļņ׶ŠĪĘæÖŠ¼ÓČė×ćĮæµā»Æ¼ŲČÜŅŗ£¬²¢¼ÓČė¼øµĪĻ”ĮņĖįŗĶµķ·ŪČÜŅŗ£¬»ģŗĻ¾łŌČŗó£¬ÓĆ0.001mol/L Na2S2O3ČÜŅŗ½ųŠŠµĪ¶Ø”£µĪ¶ØĒ°µĪ¶Ø¹ÜµÄŅŗĆę¶ĮŹżĪŖ2.10ml£¬µĪ¶Ø“ļµ½ÖÕµćŹ±µĪ¶Ø¹ÜµÄŅŗĆę¶ĮŹżĪŖ17.10ml.
ŅŃÖŖ£ŗ2 Na2S2O3 + I2 £½ Na2S4O6 + 2NaI
Ķعż¼ĘĖćÅŠ¶ĻøƵāŃĪµÄŗ¬µāĮæŹĒ·ńŌŚ20”×40mg/KgµÄ·¶Ī§ÄŚ£ŗ”””””””””””” ”£
28£®(15·Ö)ijŠ£»ÆѧæĪĶā»ī¶ÆŠ”×éĄūÓĆĻĀĶ¼×°ÖĆÖʱøĀČ»ÆĀĮ¹ĢĢ壬²¢ÓĆøĆ¹ĢĢåÅäÖĘĀČ»ÆĀĮČÜŅŗ”£×°ÖĆÖŠaĪŖ³¤²£Į§µ¼¹Ü£¬bĪŖ²£Į§»īČū”£ŹµŃéÖŠæɹ©Ń”ÓƵďŌ¼ĮÓŠ£ŗ¢Ł¶žŃõ»ÆĆĢ¹ĢĢ壬¢ŚĀĮ·Ū£¬¢ŪĀČ»ÆÄĘ¹ĢĢ壬¢ÜÅØĮņĖį£¬¢ŻÅØŃĪĖį£¬¢ŽÕōĮóĖ®£¬¢ß¼īŹÆ»Ņ”£×ŹĮĻ±ķĆ÷£ŗĀČ»ÆĀĮŹÜČČÖĮ180”ꏱ¼“Éż»Ŗ£¬ŌŚ³±ŹŖµÄæÕĘųÖŠŅ×Ė®½ā”£»Ų“šĻĀĮŠĪŹĢā£ŗ
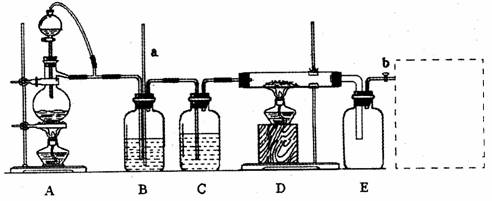
(1)¼ģ²éøĆ×°ÖĆĘųĆÜŠŌµÄ·½·ØŹĒ£ŗ”””””””””””””””””””””””””””””””””””””””””” ”£
(2) AÖŠĘųĢåÖʱøµÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ”””””””” ”””””””””£Čē¹ūæɹ©Ń”ŌńµÄŹŌ¼ĮÖŠĪŽÅØŃĪĖį£¬øĆŠ”×éĶ¬Ń§ÓĆŅŃ¹©ŹŌ¼ĮŅ²Ķź³ÉĮĖøĆŹµŃ飬ŌņA×°ÖĆÖŠŃ”ÓƵďŌ¼ĮŹĒ”””””””””””””””””” (ĢīŠņŗÅ)”£
(3)ŹµŃéÖŠB×°ÖƵÄ×÷ÓĆŹĒ”””””””””””””””””””””””””””””””””””””””””””””””” ”£
(4)D”¢E¼äµ¼¹Ü¶ĢĒŅ“Ö£¬ŌŅņŹĒ”””””””””””””””””””””””””””””””””””””””””” ”£
(5)ÓĆŹµŃéÖʵƵÄĀČ»ÆĀĮ¹ĢĢåÅäÖĘČÜŅŗµÄ·½·ØŹĒ”””””””””””””””””””””””””””””” ”£
(6)ĒėŌŚEŗóµÄŠéĻßæņÖŠ²¹³äĶźÉĘøĆ×°ÖĆ”””””””””””””””””””””””” ”””””””””””””””£øĆ×°ÖĆÖŠÓ¦Ź¢·ÅµÄŹŌ¼ĮŹĒ”””””””””””” ”£(“ÓĢāÖŠæɹ©ŹŌ¼ĮÖŠŃ”Ōń£¬ĢīŠņŗÅ)”£
27£®(19·Ö)ÓŠŅ»»ÆŗĻĪļX(²»ŗ¬½į¾§Ė®)£¬ĘäĖ®ČÜŅŗĪŖĒ³ĀĢÉ«£¬æÉ·¢ÉśČēĻĀµÄ×Ŗ»Æ¹ŲĻµ(²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļ“ÓĀŌ)”£ĘäÖŠB”¢D”¢E”¢F¾łĪŖĪŽÉ«ĘųĢ壬M”¢LĪŖ³£¼ūµÄ½šŹōµ„ÖŹ£¬CĪŖÄŃČÜÓŚĖ®µÄŗģŗÖÉ«¹ĢĢ唣ŌŚ»ģŗĻŅŗÖŠ¼ÓČėBaCl2ČÜŅŗæÉÉś³É²»ČÜÓŚĻ”ŃĪĖįµÄ°×É«³Įµķ£¬HŗĶM·“Ó¦æɷųö“óĮæµÄČČ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
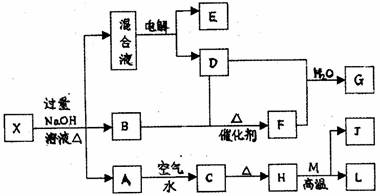
(1)BµÄµē×ÓŹ½ĪŖ”””””””””””””” £¬BĘųĢåµÄ¼ģŃé·½·ØĪŖ”””””””””””””””””””””””” ”£
(2)µē½ā»ģŗĻŅŗŹ±Ńō¼«·“Ó¦Ź½ĪŖ”””””””””””””””””””””””””””””””””””””””” ”£
(3)°“ŅŖĒ󊓳öÉĻŹö×Ŗ»Æ¹ŲĻµÖŠÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
¢Łŗ¬ÓŠLŌŖĖŲµÄ»ÆŗĻ·“Ó¦£ŗ”””””””””””””””””””””””””””””””””””””””” ”£
¢Śŗ¬ÓŠLŌŖĖŲµÄÖĆ»»·“Ó¦£ŗ”””””” ”””””””””””””””””””””””””””””””””””£
(4)LÓė¹żĮæGµÄĻ”ČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ”””””””””””””””””””””””””””””” ”£
(5)ĪļÖŹXµÄ»ÆѧŹ½ĪŖ”””””””””””””””””””””””””””” ”£
(6)ŅŃÖŖa g EĘųĢåŌŚDÖŠĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄ»ÆŗĻĪļŹ±£¬·Å³öb KJµÄČČĮ棬Š“³öEČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½£ŗ”””””””””””””””””””””””””””””””””””””””” ”£
26£®(16·Ö)A”¢B”¢C”¢D”¢EŹĒ¶ĢÖÜĘŚŌŖĖŲ£¬ÖÜĘŚ±ķÖŠAÓėB”¢BÓėCĻąĮŚ£¬CÓėAĶ¬Ö÷×壬AÓėCµÄ×īĶā²ćµē×ÓŹżÖ®±ČĪŖ2£ŗ3£¬BµÄ×īĶā²ćµē×ÓŹż±ČCµÄ×īĶā²ćµē×ÓŹżÉŁ1£¬³£¼ū»ÆŗĻĪļD2C2ÓėĖ®·“Ӧɜ³ÉCµÄµ„ÖŹ£¬ĒŅČÜŅŗÄÜŹ¹·ÓĢŖŹŌŅŗ±äŗģ”£
(1)EŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ”””””””””””” ”£
(2)BµÄĒā»ÆĪļÓėBµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·“Ӧɜ³ÉZ£¬ŌņZÖŠµÄ»Æѧ¼üĄąŠĶĪŖ”””” £¬B”¢CµÄĒā»ÆĪļ·Ö×Ó½įŗĻH+µÄÄÜĮ¦½ĻĒæµÄŹĒ(Š“»ÆѧŹ½)”””””””””” £¬ÓĆŅ»øöĄė×Ó·½³ĢŹ½¼ÓŅŌÖ¤Ć÷”””””””””””””””””””””” ”£
(3)Ņ»¶ØĮæµÄD2C2ÓėAC2·“Ó¦ŗóµÄ¹ĢĢåĪļÖŹĒ”ŗĆÓėŗ¬0.8molµÄĻ”ŃĪĖįĶźČ«·“Ó¦£¬²¢ŹÕ¼Æµ½0.25molµÄĘųĢ唣ŌņøĆ¹ĢĢåĪļÖŹµÄ×é³ÉŹĒ”””””””” ”£(ÓĆĪļÖŹµÄĮæ¼°»ÆѧŹ½±ķŹ¾)
(4)»ÆŗĻĪļEC2ĶØČėµ½BaCl2ŗĶHNO3µÄ»ģŗĻČÜŅŗ£¬Éś³É°×É«³ĮµķŗĶĪŽÉ«ĘųĢåBC£¬ÓŠ¹Ų·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ”””””””””””””””””””””””””””””””””””””””””””””””” ”£
13£®²»¾ĆĒ°£¬ĆĄ¹śŅ»øöŗ£¾üŗ½æÕÕ¾°²×°ĮĖŅ»ĢØ250KWµÄMCFCŠĶČ¼ĮĻµē³Ų£¬øƵē³ŲæÉĶ¬Ź±¹©Ó¦µēŗĶĖ®ÕōĘų£¬Ę乤×÷ĪĀ¶ČĪŖ600”ę~700”ę£¬ĖłÓĆČ¼ĮĻĪŖH2£¬µē½āÖŹĪŖČŪ½āµÄK2CO3£¬ŅŃÖŖøƵē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ2H2+O2==2H2O£¬øŗ¼«·“Ó¦ĪŖ£ŗH2+CO32--2e-==H2O+CO2£¬ŌņĻĀĮŠĶʶĻÖŠÕżČ·µÄŹĒ
”””” A£®Õż¼«·“Ó¦ĪŖ£ŗ4OH-===O2+2H2O+4e-
”””” B£®O2“ÓÕż¼«ĶØČė£¬·¢ÉśŃõ»Æ·“Ó¦
”””” C£®µē³Ų¹©Ó¦1molĖ®ÕōĘų£¬×ŖŅʵĵē×ÓŹż4mol
D£®øƵē³ŲµÄµē¼«Ć»ÓŠ²Ī¼Ó·“Ó¦
µŚ¢ņ¾ķ(·ĒŃ”ŌńĢā£¬¹²174·Ö)
12£®ŅŃÖŖijæÉÄę·“Ó¦ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬»Æѧ·½³ĢŹ½ĪŖA(g)+2B(g)£½3C(g)+D(g)£¬·“Ó¦·Å³öČČĮ攣Ķ¼ÖŠaĒśĻß“ś±ķŅ»¶ØĢõ¼žĻĀøĆ·“Ó¦µÄ¹ż³Ģ”£ČōŹ¹aĒśĻß±äĪŖbĒśĻߣ¬æɲÉČ”µÄ“ėŹ©ŹĒ
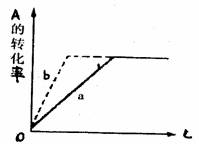
¢ŁŌö“óAµÄÅØ¶Č ¢ŚĖõŠ”ČŻĘ÷µÄČŻ»ż”” ¢Ū¼ÓČė“߻ƼĮ”” ¢ÜÉżøßĪĀ¶Č
”” ”””” A£®¢Ł¢Ū”””” ”””””””” B£®¢Ś¢Ü”””” ”””””” C£®¢Ś¢Ū”””””” ”””” D£®¢Ū¢Ü
11£®ŃŠ¾æŠŌѧĻ°Š”×é×öĶÓėÅØĮņĖį·“Ó¦ŹµŃ鏱£¬·¢ĻÖŹŌ¹Üµ×²æÓŠ°×É«¹ĢĢå²¢¼ŠŌÓÓŠÉŁĮæŗŚÉ«ĪļÖŹ”£µ¹Č„ŹŌ¹ÜÖŠµÄÅØĮņĖį£¬½«Ź£Óą¹ĢĢå(ŗ¬ÉŁĮæÅØĮņĖį)µ¹ČėŹ¢ÓŠÉŁĮæĖ®µÄÉÕ±ÖŠ£¬·¢ĻÖĖłµĆČÜŅŗĪŖĄ¶É«£¬ŗŚÉ«¹ĢĢåÄ©Čܽā”£¹żĀĖ”¢Ļ“µÓŗó£¬ĻņŗŚÉ«¹ĢĢåÖŠ¼ÓČė¹żĮæÅØĻõĖį£¬ŗŚÉ«¹ĢĢåČܽā£¬ČÜŅŗ³ŹĄ¶É«£¬ĖłµĆČÜŅŗ¼ÓBaCl2ČÜŅŗŗóÓŠ°×É«³ĮµķÉś³É”£ĻĀĮŠĖłµĆ½įĀŪÕżČ·µÄŹĒ
”””” A£®ĶÓėÅØĮņĖį·“Ó¦ĖłµĆ°×É«¹ĢĢåŹĒCuSO4”¤5H2O
”” ”””” B£®¼ÓBaCl2ČÜŅŗŗóĖłµĆ°×É«³ĮµķŹĒBaSO3
”” ”””” C£®°×É«¹ĢĢåÖŠ¼ŠŌÓµÄÉŁĮæŗŚÉ«ĪļÖŹŹĒCuO
”””””” D£®°×É«¹ĢĢåÖŠ¼ŠŌÓµÄÉŁĮæŗŚÉ«ĪļÖŹÖŠŗ¬ŌŖĖŲCu”¢S
10£®ĻĀĮŠø÷×éĄė×ÓŌŚÖø¶ØČÜŅŗÖŠÄÜ“óĮæ¹²“ęµÄŹĒ
”””” A£®ĪŽÉ«ČÜŅŗÖŠ£ŗK+”¢Na+”¢MnO4-”¢SO42-
”””” B£®PH£½11µÄČÜŅŗÖŠ£ŗCO32-”¢Na+”¢AlO2-”¢NO3-
”””” C£®¼ÓČėĀĮÄܷųöH2µÄČÜŅŗÖŠ£ŗCl-”¢HCO3-”¢SO42-”¢NH4+
”””” D£®ĖįŠŌČÜŅŗÖŠ£ŗFe2+”¢Al3+”¢NO3-”¢I-”¢Cl-
9£®ČōNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
¢Ł±ź×¼×“æöĻĀ£¬2.24LĖÄĀČ»ÆĢ¼ŗ¬Ģ¼Ō×ÓŹżĪŖ0.1NA
¢Ś±ź×¼×“æöĻĀ£¬a LµÄŃõĘųŗĶµŖĘųµÄ»ģŗĻĪļŗ¬ÓŠµÄ·Ö×ÓŹżĪŖa/22.4 NA
¢Ū60gSiO2¾§ĢåÖŠŗ¬ÓŠ2NAøöSi-O¼ü
¢ÜijĢõ¼žĻĀ£¬½«1mol N2ŗĶ3mol H2ŌŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦£¬Éś³ÉNH3·Ö×ÓŹżĪŖ2NA
¢Ż7.1gĀČĘųÓė×ćĮæµÄĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ0.1NA
”””” A£®¢Ł¢Ü”””” ”””””””” B£®¢Ś¢Ū”””” ”””””” C£®¢Ū¢Ż”””””” ”””” D£®¢Ś¢Ż
8£®ĻĀĮŠÓŠ¹Ų»·¾³ĪŹĢāµÄĖµ·Ø£¬²»ÕżČ·µÄŹĒ
”””” A£®æÕĘųÖŠ³ōŃõµÄĢå»ż·ÖŹż³¬¹ż10-4 %µÄæÕĘųÓŠĄūÓŚČĖĢå½”æµ
”””” B£®Č¼ĆŗŹ±£¬¼ÓČėŹŹĮæŹÆ»ŅŹÆ£¬æɼõÉŁ·ĻĘųÖŠSO2µÄĮæ
”””” C£®PHŠ”ÓŚ5”¢6µÄ½µĖ®Ķس£³ĘĪŖĖįÓź
D£®Ė®Äą”¢Ņ±½š¹¤³§³£ÓĆøßŃ¹µē³żČ„¹¤³§ŃĢ³¾£¬¼õÉŁ¶ŌæÕĘųµÄ·ØÖĪĪŪČ¾
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com