
16.(8分)为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,某课题研究小组的同学们设计了如下图的实验装置,分别进行了甲、乙两次实验。
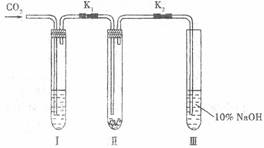
实验甲:干燥的二氧化碳和过氧化钠的反应。在干燥的试管II中装入Na2O2,在通入 CO2之前,关闭K1和K2。在试管I内装入试剂 X 后,打开K1和K2,通入CO2,几分钟后将带火星的木条插入试管III的液面上,观察到木条不复燃,且II中的淡黄色没有变化。
实验乙:潮湿的二氧化碳和过氧化钠的反应。在试管I内装入试剂Y,其他操作同实验甲。观察到木条复燃,且II中的淡黄色变为白色。
试回答下列问题:
(1)在装入Na2O2 后,通入CO2前,关闭K1和K2的目的是_________________________。
(2)在实验甲中,试剂X是_______________;在实验乙中,试剂Y是__________________。
(3)根据上述两个实验现象,得到的结论是________________________________________
________________________________________________________。
(4)为了确保实验现象的准确性,制备CO2所用的反应物最好选用__________________(填编号,多选扣分)。
A.大理石 B.小苏打 C.烧碱 D.盐酸 E.稀硫酸 F.稀硝酸
(5)CO2和Na2O2的反应机理可用示踪原子分析加以证明,请完成下列反应方程式:
Na2O2+Cl8O2+H218O →
15.(5分)某化学小组的同学到实验室学习。在实验桌上摆有下列仪器:
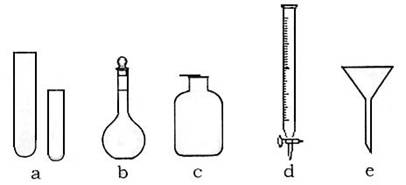
(1)甲同学想用 d 进行实验,请你说出该仪器(已经洗涤干净)使用时的第一步操作:
__________________________________________________________________________
(2)关于e的用途,乙同学说:组成防倒装置。你还能说出其他两种用途吗?
①________________________________________;
②________________________________________。
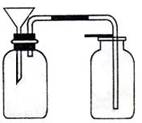
(3)丙同学想用下图装置以大理石和稀盐酸反应制取CO2。教师指出,这需要太多的稀盐酸,造成浪费。该同学选用了上面的一种仪器,加在装置上,解决了这个问题。请你把该仪器画在图中合适的位置。
14. 如下图所示装置,两玻璃管中盛满滴有石蕊溶液的NaCl 饱和溶液,c(I)、c (II) 为多孔石墨电极。断开接通S1 后,c(I)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,说明此时该装置形成了原电池。关于该原电池的叙述正确的是
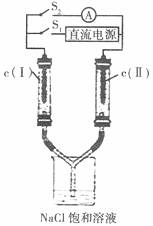
A.c (II)的电极名称是负极
B.外电路电流方向:c(I)→ c(II)
C.c(I)的电极反应式为:H2+2OH--2e- ===2H2O
D.溶液中的Na+向c(I)极移动
第II卷 (非选择题 共58分)
13. 短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A和C同主族,B原子的最外层电子数等于A原子次外层电子数。下列叙述中正确的是
A.原子半径:A<B<C
B.C 的氢化物稳定性大于A的氢化物的稳定性
C.三种元素的最高价氧化物的水化物均可由化合反应得到
D.高温下,A单质能置换出C单质
12.2008年9月11日,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件。当晚,三鹿集团承认婴幼儿奶粉受到三聚氰氨污染,并宣布召回市面上被污染的产品。三聚氰氨的分子结构如下图所示,关于三聚氨胶的说法正确的是
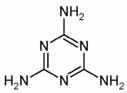
A.三聚氰氨含有苯环结构,属于芳香族化合物
B.三聚氰氨中的碳原子属于饱和碳原子
C.三聚氰氨在一定条件下可能会与氢气发生加成反应
D.三聚氰氨能与硝酸发生环上的取代反应
11. 在体积都为1 L,pH 都等于2的盐酸和醋酸溶液中,投入0.65g锌粒,则下图所示比较符合客观事实的是
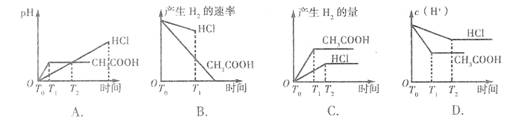
10. 取下列各组物质中的两种组分各 1mol,在足量氧气中充分燃烧,两者耗氧量不等的是
A.乙烯和乙醇 B.乙炔和乙醛
C.乙烷和乙酸甲酯 (CH3COOCH3) D.乙醇和乙酸
9. 常温下将稀NaOH溶液和稀CH3COOH溶液混合,不可能出现的结果是
A.pH>7, 且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)
B.pH>7,且c(Na+)+ c(H+)= c(CH3COO-)+ c(OH-)
C.pH<7, 且c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D.pH=7, 且c(CH3COO-)= c(Na+)>c(H+)= c(OH-)
8. 已知:H2O(g)===H2O(l) △H=-Q1kJ· mol-1
CH3OH(g)==CH3OH(l) △H=-Q2kJ· mol-1
2CH3OH(g)+3O2(g)=== 2CO2(g)+4H2O(g) △H=-Q3kJ· mol-1 (Q1、Q2、Q3均大于0) 若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)
A.Q1+Q2+Q3 B.0.5Q3-Q2+2Q1
C.0.5Q3+Q2-2Q1 D.0.5(Q1+Q2+Q3)
7. 下述实验能达到预期目的的是
|
编号 |
实验内容 |
实验目的 |
|
A |
将10gCuSO4•5H2O溶解在90g水中 |
配制质量分数为10%的CuSO4溶液 |
|
B |
将Cl2通入NaBr溶液中 |
比较氯和溴的氧化性强弱 |
|
C |
向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
制备Fe(OH)3胶体 |
|
D |
向某溶液中滴加BaCl2溶液有白色沉淀生成 |
证明该溶液中一定含有SO42-离子 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com