
21.为达到预期的试验目的,下列说法正确的是( )
A.欲配制质量分数为10%的ZnSO4溶液,将10gZnSO4·7H2O溶解在90g水中
B.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸
C.为鉴别KCl、AlCl3、MgCl2溶液,取三种溶液分别滴加NaOH溶液至过量
D.为减小中和滴定误差,锥形瓶必须洗净并干燥后才能使用
20.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有X元素.它们有如图所示的转化关系(部分产物及反应物已略去),下列判断正确的是( )
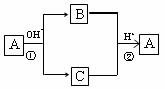
A.X元素可能为Al
B.X元素一定为非金属元素
C.反应①和反应②互为可逆反应
D.反应①和②不一定是氧化还原反应
19.下列化学用语正确的是( )
A.硫酸氢钾熔融的电离的方程式:KHSO4=K+ + H+ +SO42-
B.碳酸氢铵溶液与过量的氢氧化钠溶液共热:NH4++OH- NH3↑+H2O
NH3↑+H2O
C.钢铁发生吸氧腐蚀的正极反应式:4OH――4e―=2H2O+O2↑
D.常温下,用惰性电极电解饱和的碳酸钠溶液:2H2O 2H2↑+O2↑
2H2↑+O2↑
18.下列说法正确的是( )
A.同族元素的最外层电子数一定相等
B.非金属元素的最高正价和最低负价的绝对值的和都等于2或8
C.质子数和电子数分别都相等的两种微粒,可以是两种离子,也可以是两种分子,或一种分子一种离子
D.非金属元素形成的化合物中可以存在共价键,也可以存在离子键
17.X、Y、Z为短周期元素,Z的原子序数等于X、Y的原子序数之和,且Z离子比X离子多三个电子层,下列推断不正确的是( )
A.Y的原子半径大于Z的原子半径 B.X可能为金属元素
C.Y与Z不可能形成离子化合物 D.Z一定为非金属元素
16.下列离子方程式正确的是( )
A.二氧化硫气体通入到漂白粉溶液中:Ca2+ + 2ClO-+SO2+H2O=CaSO3↓+2HClO
B.硫酸镁溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
C.碳酸钙与醋酸反应:CaCO3+ 2CH3COOH=Ca2+ +2CH3COO-+H2O+CO2↑
D.铜片与稀硝酸:Cu+NO3-+4H+=Cu2+ +NO↑+2H2O
15.为提纯下列物质(括号内为少量杂质),所选用的除杂试剂和分离方法正确的是( )
|
|
提纯物质 |
除杂试剂 |
分离方法 |
|
A |
KCl溶液(FeCl3) |
氨水 |
过滤 |
|
B |
乙酸乙酯(乙酸) |
乙醇和浓硫酸 |
分液 |
|
C |
NaCl溶液(Na2S) |
AgCl |
过滤 |
|
D |
乙醇(H2O) |
金属钠 |
蒸馏 |
14.下列各组离子中,在碱性溶液中共存,在加入盐酸过程中会产生气体和沉淀的是( )
A.Na+、NO3-、Al3+、SO42- B.K+、Na+、NO3-、SiO32-
C. Na+、Br-、AlO2-、S2- D.SO42-、HCO3-、Ca2+、NH4+
13.将总物质的量为nmol的钠和铝(其中钠的物质的量分数为x),投入到一定量的水中充分反应,金属没有剩余,共收集到标况下的VL气体.下列关系式中正确的是( )
A.x=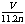 B.0<x≤0.5 C.33.6(1-x)=V D.11.2n<V≤22.4n
B.0<x≤0.5 C.33.6(1-x)=V D.11.2n<V≤22.4n
12. 下列叙述中正确的是( )
A.向饱和石灰水中加入少量CaO,恢复到原来温度,溶液中OH-浓度变小
B.Na2O2晶体中阴离子与阳离子的个数比为1:1
C.向Ba(OH)2溶液中滴加过量NaHSO4溶液的离子方程式:
Ba2+ + OH-+ H+ +SO42-=BaSO4↓+H2O
D.3.9gNa2O2与足量的水反应转移电子0.05mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com