
17.同温同压下,下列各组热化学方程式中,满足Q2>Q1的是
A.2H2(g) + O2(g) = 2H2O(g); △H =-Q1
2H2(g) + O2(g) = 2H2O(l); △H =-Q2
B.S(g)+O2(g)=SO2(g); △H =-Q1
S(s)+O2(g)=SO2(g); △H =-Q2
C.C(s)+O2(g)=CO2(g); △H =-Q1
C(s)+1/2O2(g)=CO(g); △H =-Q2
D. H2(g)+Cl2(g)=2HCl(g); △H =-Q1
1/2H2(g)+1/2Cl2(g)=HCl(g); △H =-Q2
16.某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2─、MnO4─、CO32─、SO42─中的若干种组成。取该溶液进行如下实验:(1)取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液;(2)在⑴所得溶液中加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;(3)在(2)所得溶液中加入过量Ba(OH)2溶液也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定存在的有:
A.SO42-、AlO2─、Na+ B.Na+、CO32─、AlO2─
C.CO32─、Na+、Al3+ D.MnO4─、Na+、CO32─
15.共价键、金属键、离子键和分子间作用力都是构成物质的粒子间的不同作用,含有以上所说的两种作用的晶体是
A.SiO2晶体 B.CCl4晶体 C.MgCl2晶体 D.Na2O晶体
14.含有非极性键的离子化合物是
A.C2H2 B.Mg3N2 C.(NH4)2S D.CaC2
13.R2O8n-离子在一定条件下可以把Mn2+离子氧化成MnO4-,若反应后R2O8n-离子变为RO42-离子。又知反应中氧化剂与还原剂的物质的量之比为5:2 ,则n的值是
A.1 B. 2 C.3 D.4
12.下列叙述正确的是
A.48 g O3气体含有6.02×1023个O3分子
B.常温常压下,4.6 g NO2气体含有1.81×1023个NO2分子
C.0.5 mol·L-1 CuCl2溶液中含有3.01×1023个Cu2+
D.标准状况下,33.6 L H2O含有9.03×1023个H2O分子
11.下列叙述正确的是
A.分子晶体中的每个分子内一定含有共价键
B.原子晶体中的相邻原子间只存在非极性共价键
C.离子晶体中可能含有共价键
D.金属晶体的熔点和沸点都很高
10.下列热化学方程式中的反应热下划线处表示燃烧热的是
A.NH3(g)+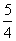 O2(g)
O2(g) NO(g)+
NO(g)+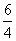 H2O(g); ΔH=-a kJ·mol-1
H2O(g); ΔH=-a kJ·mol-1
B.C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l); ΔH=-b kJ·mol-1
6CO2(g)+6H2O(l); ΔH=-b kJ·mol-1
C.2CO(g)+O2(g) 2CO2(g);
ΔH=-c
kJ·mol-1
2CO2(g);
ΔH=-c
kJ·mol-1
D.CH3CH2OH(l)+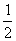 O2(g)
O2(g) CH3CHO(l)+H2O(l);ΔH=-d kJ·mol-1
CH3CHO(l)+H2O(l);ΔH=-d kJ·mol-1
9.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+ m,则X的最高正价一定为+ m
8.有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的c(Na+)/mol·L-1为
A.(y-2x)/a B.(y-x)/a C.(2y-2x)/a D.(2y-4x)/a
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com