
18ЃЎ(15Зж)вбжЊAЁЂBЁЂCЪЧШ§жжГЃМћЕФЙЬЬхЛЏКЯЮяЃЌбцЩЋЗДгІОљЯдЛЦЩЋЃЌЦфжаAгыCАДШЮвтБШР§ЛьКЯЃЌШмгкзуСПЕФЫЎжаЃЌЕУЕНЕФШмжЪвВжЛКЌгавЛжжЃЌВЂгаЮоЩЋЁЂЮоЮЖЕФЦјЬхDЗХГіЁЃСэAЁЂBЁЂCЁЂDжЎМфКЌгаШчЯТЕФзЊЛЏЙиЯЕЃК(ВПЗжЮяжЪЮДаДГі)
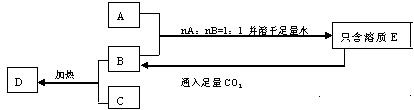
ЁЁ (1)аДГіЮяжЪЕФЛЏбЇЪНЃК
ЁЁЁЁ ЁЁAЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁ CЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)аДГіAЁЂBАДЮяжЪЕФСПжЎБШЮЊ1ЃК1дкУмБеШнЦїжаМгШШЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ (3)аДГіШмжЪEгызуСПCO2ЗДгІЕФРызгЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
17ЃЎ(12Зж)AЁЂBЁЂCЁЂDЁЂEЪЧдзгађЪ§вРДЮдіДѓЕФЮхжжЖЬжмЦкдЊЫиЁЃAдзгЕФЕчзгВуЪ§гыЫќЕФКЫЭтЕчзгзмЪ§ЯрЭЌЃЌAгыCЁЂBгыDЗжБ№ЮЊЭЌжїзхЃЌBКЭCЕФзюЭтВуЕчзгЪ§жЎКЭгыEЕФзюЭтВуЕчзгЪ§ЯрЭЌЁЃAгыEаЮГЩЕФЛЏКЯЮяЛЏбЇЪНЮЊAEЃЌЦфЗжзгжаКЌ18ИіЕчзгЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЁЁ (1)AКЭBСНдЊЫивВПЩвдаЮГЩ18ЕчзгЕФЛЏКЯЮяMЃЌдђMЕФЕчзгЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)гЩCКЭEЫљаЮГЩЕФЛЏКЯЮяжаКЌгаЕФЛЏбЇМќЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЃЌИУЛЏКЯЮяЪєгк
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁОЇЬх(ЬюОЇЬхРраЭ)ЁЃ
ЁЁ (3)гЩAЁЂBЁЂCЁЂDЫФжждЊЫиЫљаЮГЩЕФСНжжЛЏКЯЮяЯрЛЅжЎМфЗДгІЕФРызгЗНГЬЪНЮЊЃК
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ (4)BЁЂCЁЂEШ§жждЊЫиаЮГЩвЛжжбЮЃЌДЫбЮжаШ§жждзгИіЪ§БШЮЊ1ЁУ1ЁУ1ЃЌНЋИУбЮШмвКдкПеЦјжаТЖжУвЛЖЮЪБМфКѓ(ГфЗжЙтееЃЌВЛПМТЧЫЎЗжЕФЛгЗЂ)ЃЌШмвКЕФpHНќЫЦЮЊ7ЃЌдђИУЙ§ГЬЕФзмЗДгІЗНГЬЪНЮЊ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
16ЃЎАбвЛПщУОТСКЯН№ЭЖШыЕН1mol/L HClШмвКРяЃЌД§КЯН№ЭъШЋШмНтКѓЃЌЭљШмвКРяМгШы1mol/L NaOHШмвКЃЌЩњГЩГСЕэЕФЮяжЪЕФСПЫцМгШыNaOHШмвКЬхЛ§БфЛЏЕФЙиЯЕШчЯТЭМAЫљЪОЁЃЯТСаЫЕЗЈжаВЛе§ШЗЕФЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
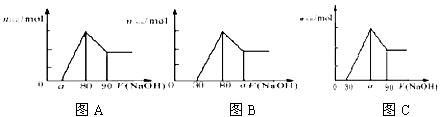
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ AЃЎ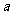 ЕФШЁжЕЗЖЮЇЮЊ0ЁмaЃМ50
ЕФШЁжЕЗЖЮЇЮЊ0ЁмaЃМ50
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ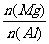 ЕФзюДѓжЕЮЊ2.5mol
ЕФзюДѓжЕЮЊ2.5mol
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎШєНЋЙиЯЕЭМИФЮЊBЭМЪБЃЌдђ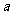 ЕФШЁжЕЗЖЮЇЮЊ80ЃМaЃМ90
ЕФШЁжЕЗЖЮЇЮЊ80ЃМaЃМ90
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎШєНЋЙиЯЕЭМИФЮЊCЭМЪБЃЌдђ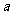 ЕФШЁжЕЗЖЮЇЮЊ75ЃМaЃМ90
ЕФШЁжЕЗЖЮЇЮЊ75ЃМaЃМ90
ЕкЂђОэ ЗЧбЁдёЬтВПЗж(змМЦ60Зж)
15ЃЎФГЭЌбЇЮЊМьбщШмвКжаЪЧЗёКЌгаГЃМћЕФЫФжжЮоЛњРызгЃЌНјааСЫЯТЭМЫљЪОЕФЪЕбщВйзїЁЃЦфжаМьбщЙ§ГЬжаВњЩњЕФЦјЬхФмЪЙКьЩЋЪЏШяЪджНБфРЖЁЃгЩИУЪЕбщФмЕУЕНЕФе§ШЗНсТлЪЧ(ЁЁЁЁ )
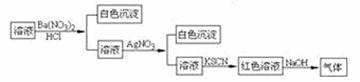
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ AЃЎдШмвКжавЛЖЈКЌгаSO42-РызгЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎдШмвКжавЛЖЈКЌгаNH4+
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎдШмвКжавЛЖЈКЌгаCl-РызгЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎдШмвКжавЛЖЈКЌгаFe3-Рызг
14ЃЎФГАзЩЋЙЬЬхПЩФмгЩЂйH4ClЂкAlCl3ЂлNaClЂмAgNO3ЂнKOHжаЕФвЛжжЛђМИжжзщГЩЃЌНЋДЫЙЬЬхЭЖШыЫЎжаЕУЕНГЮЧхШмвКЃЌИУШмвКПЩЪЙЬЊГЪКьЩЋЁЃШєЯђИУШмвКжаМгШыЯЁЯѕЫсжСЙ§СПЃЌгаАзЩЋГСЕэЩњГЩЁЃЖддЙЬЬхзщГЩЕФХаЖЯВЛе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎПЩФмДцдкЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎжСЩйгаЂкЂн
ЁЁЁЁЁЁ CЃЎЮоЗЈШЗЖЈЪЧЗёгаЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎжСЩйДцдкЂйЂмЂн
13ЃЎгУЖшадЕчМЋЪЕЯжЕчНтЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЕчНтЯЁСђЫсШмвКЃЌЪЕжЪЩЯЪЧЕчНтЫЎЃЌЙЪШмвКpHВЛБф
ЁЁЁЁЁЁ BЃЎЕчНтЯЁЧтбѕЛЏФЦШмвКЃЌвЊЯћКФOH-ЃЌЙЪШмвКpHМѕаЁ
ЁЁЁЁЁЁ CЃЎЕчНтСђЫсФЦШмвКЃЌдквѕМЋЩЯКЭбєМЋЩЯЮіГіВњЮяЕФЮяжЪЕФСПжЎБШЮЊ1ЁУ2
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЕчНтТШЛЏЭШмвКЃЌдквѕМЋЩЯКЭбєМЋЩЯЮіГіВњЮяЕФЮяжЪЕФСПжЎБШЮЊ1ЁУ1
12ЃЎЯТСаХХСаЫГађе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ Ђй ШШЮШЖЈадЃКH2OЃОHFЃОH2SЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЂкдзгАыОЖЃКNaЃОMgЃОO
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ Ђл ЫсадЃКH3PO4ЃОH2SO4ЃОHClO4ЁЁ ЁЁЁЁЁЁЁЁ ЂмНсКЯжЪзгФмСІЃКOH-ЃОCH3COO-ЃОCl-
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ AЃЎЂйЂлЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ BЃЎЂкЂмЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂйЂмЁЁЁЁ ЁЁ DЃЎЂкЂл
11ЃЎШЁЯрЭЌЬхЛ§ЕФKIЁЂNa2SЁЂFeBr2ШмвКЃЌЗжБ№ЭЈШызуСПЕФCl2ЃЌЕБЗДгІЧЁКУЭъГЩЪБЃЌЯћКФCl2ЕФЬхЛ§ЯрЭЌ(ЭЌЮТЁЂЭЌбЙЬѕМўЯТ)ЃЌдђKIЁЂNa2SЁЂFeBr2ШмвКЕФЮяжЪЕФСПХЈЖШжЎБШЪЧ(ЁЁЁЁ )
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ AЃЎ1:1:2ЁЁЁЁЁЁЁЁЁЁ BЃЎ2:1:3 ЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ6:3:2ЁЁЁЁЁЁ ЁЁ DЃЎ3:2:1
10ЃЎТШЦјЪЧвЛжжЛЏбЇаджЪКмЛюЦУЕФЗЧН№ЪєЕЅжЪЃЌЫќОпгаНЯЧПЕФбѕЛЏадЃЌЯТСаа№ЪіжаВЛе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎКьШШЕФЭЫПдкТШЦјРяОчСвШМЩеЃЌЩњГЩзиЛЦЩЋЕФбЬ
ЁЁЁЁЁЁ BЃЎФЦдкТШЦјжаШМЩеЃЌЩњГЩАзЩЋЕФбЬ
ЁЁЁЁЁЁ CЃЎДПОЛЕФH2дкCl2жаАВОВЕиШМЩеЃЌЗЂГіВдАзЩЋЛ№бцЃЌМЏЦјЦППкГЪЯжАзЩЋбЬЮэЁЃ
ЁЁЁЁЁЁ DЃЎТШЦјФмгыЫЎЗДгІЩњГЩДЮТШЫсКЭбЮЫсЃЌОУжУТШЫЎзюжеБфЮЊЯЁбЮЫс
9ЃЎRЁЂQЮЊЖЬжмЦкжаЕФСНжждЊЫиЃЌRдЊЫидзгЕФзюЭтВуЕчзгЪ§гыДЮЭтВуЕчзгЪ§жЎВюЕФОјЖджЕЕШгкЕчзгВуЪ§ЃЛQдЊЫиЕФдзгБШRдЊЫиЕФдзгЖр2ИіКЫЭтЕчзгЃЌдђЯТСаа№ЪіжаПЯЖЈВЛе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ AЃЎдзгАыОЖЃКR>QЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎRКЭQПЩаЮГЩРызгЛЏКЯЮя
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎRКЭQПЩаЮГЩЙВМлЛЏКЯЮяRQ2ЁЁ ЁЁЁЁЁЁЁЁ DЃЎRКЭQПЩаЮГЩЙВМлЛЏКЯЮяRQ3
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com