
6Θ°Μ·―ßΩΤ―ß–η“ΣΫη÷ζΜ·―ßΉ®”Ο”ο―‘ά¥Οη ωΘ§œ¬Ν–”–ΙΊΜ·―ß”Ο”ο’ΐ»ΖΒΡ «
AΘ°CO2ΒΡΖ÷Ή” ΫΘΚ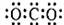 ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
CΘ°““œ©ΒΡΫαΙΙΦρ ΫΘΚC2H4
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
CΘ°““œ©ΒΡΫαΙΙΦρ ΫΘΚC2H4
BΘ°Cl-ΒΡΫαΙΙ Ψ“βΆΦΘΚ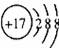 ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
DΘ°÷ ΝΩ ΐΈΣ37ΒΡ¬»‘≠Ή”ΘΚ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
DΘ°÷ ΝΩ ΐΈΣ37ΒΡ¬»‘≠Ή”ΘΚ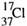
34Θ°(8Ζ÷)[Μ·―ß-”–ΜζΜ·―ßΜυ¥Γ]
ΓΓΓΓ M5œΥΈ§ «ΟάΙζΩΣΖΔΒΡ“Μ÷÷≥§–‘ΡήœΥΈ§Θ§œ¬Οφ «M5œΥΈ§ΒΡΚœ≥…¬ΖœΏ(”––©”ΠΈ¥ΉΔΟςΧθΦΰ)ΘΚ
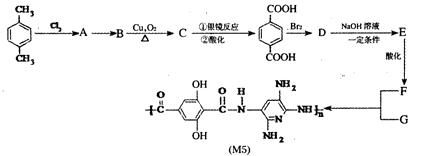
«κΜΊ¥πΘΚ
ΓΓ (1)–¥≥ωΚœ≥…M5ΒΞΧεFΒΡΫαΙΙΦρ ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (2)Ζ¥”Πάύ–ΆΘΚAΓζBΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§F+GΓζM5ΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (3)Ρ≥–©ΖΦœψΉε”–ΜζΈο «CΒΡΆ§Ζ÷“λΙΙΧεΘ§‘ρ’β–©ΖΦœψΉε”–ΜζΈο(≤ΜΑϋΚ§C)ΫαΙΙ÷–≤ΜΩ…Ρή”–ΓΓΓΓΓΓΓΓΓΓΓΓ (Χν–ρΚ≈)
ΓΓ ΓΓΓΓΓΓaΘ°ΝΫΗωτ«ΜυΓΓΓΓΓΓ bΘ°“ΜΗω»©ΜυΓΓΓΓΓΓΓΓΓΓΓΓ cΘ°ΝΫΗω»©ΜυΓΓΓΓΓΓΓΓΓΓΓΓ dΘ°“ΜΗωτ»Μυ
ΓΓ (4)–¥≥ωΜ·―ßΖΫ≥Χ ΫΘΚ
ΓΓΓΓΓΓΓΓ BΓζCΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§
DΓζEΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
33Θ°(8Ζ÷)[Μ·―ß-Έο÷ ΫαΙΙ”κ–‘÷ ]
ν―ΚΆν―ΒΡΚœΫπ“―±ΜΙψΖΚ”Ο”Ύ÷Τ‘λΒγ―ΕΤς≤ΡΓΔ»Υ‘λΙ«ςάΓΔΜ·ΙΛ…η±ΗΓΔΖ…ΜζΒ»ΚΫΧλΚΫΩ’≤ΡΝœΘ§±Μ”ΰΈΣΓΑΈ¥ά¥ άΫγΒΡΫπ τΓ±ΓΘ ‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΓΓ (1)ν―”–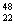 ΚΆ
ΚΆ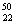 TiΝΫ÷÷‘≠Ή”Θ§ΥϋΟ«ΜΞ≥ΤΈΣΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΘTi‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «ΒΎΓΓΓΓ ΓΓΓΓΓΓΓΓ÷ήΤΎΘ§ΒΎΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΉεΘΜΜυΧ§‘≠Ή”ΒΡΒγΉ”≈≈≤Φ ΫΈΣΓΓΓΓ
TiΝΫ÷÷‘≠Ή”Θ§ΥϋΟ«ΜΞ≥ΤΈΣΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΘTi‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «ΒΎΓΓΓΓ ΓΓΓΓΓΓΓΓ÷ήΤΎΘ§ΒΎΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΉεΘΜΜυΧ§‘≠Ή”ΒΡΒγΉ”≈≈≤Φ ΫΈΣΓΓΓΓ
Α¥ΒγΉ”≈≈≤ΦTi‘ΣΥΊΒΡ‘ΣΥΊ÷ήΤΎ±μΖ÷«χ÷– τ”ΎΓΓΓΓΓΓΓΓΓΓ «χ‘ΣΥΊΓΘ
ΓΓ (2)ΤΪν―Υα±Β‘Ύ–Γ–Ά±δ―ΙΤςΓΔΜΑΆ≤ΚΆά©“τΤς÷–ΕΦ”–”Π”ΟΓΘΤΪν―Υα±ΒΨßΧε÷–ΨßΑϊΒΡΫαΙΙ»γœ¬ΆΦΥυ ΨΘ§ΥϋΒΡΜ·―ß Ϋ « ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
ΓΓ (3)œ÷”–Κ§Ti3+ΒΡ≈δΚœΈοΘ§Μ·―ß ΫΈΣ[TiCl(H2O)5]Cl2ΓΛH2OΓΘ≈δάκΉ”[TiCl(H2O)5]2+÷–Κ§”–ΒΡΜ·―ßΦϋάύ–Ά «ΓΓΓΓΓΓΓΓΓΓΓΓ Θ§ΗΟ≈δΚœΈοΒΡ≈δΧε «ΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
32Θ°(8Ζ÷)[Μ·―ß-Μ·―ß”κΦΦ θ]
ΚΘΥ°÷–»ήΫβΝΥ¥σΝΩΒΡΤχΧεΈο÷ ΚΆΗς÷÷―ΈάύΓΘ»Υάύ‘Ύ¬ΫΒΊ…œΖΔœ÷ΒΡ100Εύ÷÷‘ΣΥΊΘ§‘ΎΚΘΥ°÷–Ω…“‘’“ΒΫ80Εύ÷÷ΓΘΚΘ―σ «“ΜΗω‘ΕΈ¥Άξ»ΪΩΣΖΔΒΡΨό¥σΜ·―ßΉ ‘¥±ΠΩβΘ§ΚΘ―σΉ ‘¥ΒΡΉέΚœάϊ”ΟΨΏ”–Ζ«≥ΘΙψάΪΒΡ«ΑΨΑΓΘ
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΓΓ (1)’τΝσΖ® «»ΥάύΉν‘γ Ι”ΟΒΡΒ≠Μ·ΚΘΥ°ΒΡΖΫΖ®Θ§ΦΦ θΚΆΙΛ“’±»ΫœΆξ±ΗΘ§ΒΪ”…”Ύ Ι”Ο¥σΝΩ»ΦΟΚΘ§“ρ¥ΥΡήΚΡΕύΓΔ≈≈ΈέΝΩ¥σΓΘΈΣΩΥΖΰ’τΝσΖ®ΚΘΥ°Β≠Μ·ΒΡ»±œίΘ§«κΡψΕ‘’τΝσΖ®Β≠Μ·ΚΘΥ°ΒΡΙΛ“’Χα≥ω“ΜΧθΗΡΫχΫ®“ιΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (2) Ι”ΟάκΉ”ΫΜΜΜ ς÷§”κΥ°÷–ΒΡάκΉ”Ϋχ––ΫΜΜΜ“≤ «≥Θ”ΟΒΡΥ°¥ΠάμΦΦ θΓΘΨέ±ϊœ©ΥαΡΤ «“Μ÷÷άκΉ”ΫΜΜΜ ς÷§Θ§–¥≥ωΨέ±ϊœ©ΥαΡΤΒΞΧεΒΡΫαΙΙΦρ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (3)Ω’Τχ¥Β≥ωΖ® «ΡΩ«Α¥”ΚΘΥ°÷–Χα»ΓδεΒΡ≥Θ”ΟΖΫΖ®Θ§Νς≥Χ»γœ¬(Ωύ¬±ΘΚΚΘΥ°’τΖΔΫαΨßΖ÷άκ≥ω ≥―ΈΒΡΡΗ“Κ)ΘΚ
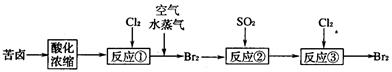
ΓΓΓΓ ΔΌΖ¥”ΠΔΎΒΡάκΉ”ΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘΜ
ΓΓΓΓ ΔΎ¥”Ζ¥”ΠΔέΚσΒΡ»ή“Κ÷–Ζ÷άκ≥ωΒΞ÷ δεΒΡΖΫΖ® «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
31Θ°(16Ζ÷)
“―÷ΣΘΚΦνΫπ τΜρΦνΆΝΫπ τ(ΔρΉε)”κH2‘ΎΗτΨχΩ’ΤχΦ”»» ±“Σ“‘ΖΔ…ζΖ¥”ΠΘ§…ζ≥…άκΉ”–ΆΫπ τ«βΜ·ΈοΘ§»γNaHΓΔCaH2Β»Θ§ΥϋΟ«“Ή”κΥ°Ζ¥”ΠΓΘœ÷”–ΦΉΓΔ““ΝΫΈΜΆ§―ßΖ÷±π…ηΦΤΝΥ÷Τ±ΗCaH2ΒΡ Β―ιΘ§ΉΑ÷Ο»γΆΦΥυ Ψ(Ζ÷±π“‘–ρΚ≈ΔώΓΔΔρ±μ Ψ)Θ§ΧζΦήΧ®Β»Φ–≥÷ΙΧΕ®“«Τς“―¬‘»ΞΓΘ
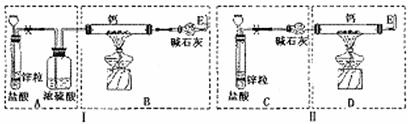
«κΜΊ¥πœ¬Ν–Έ Χβ
ΓΓ (1)–Ω”κ―ΈΥαΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΓΓ (2)ΉνΚσ Β―ιΫαΙϊœ‘ ΨΘ§ΝΫΈΜΆ§―ßΒΡ Β―ιΉΑ÷Ο…ηΦΤΕΦ”–»±œίΓΘ
ΓΓΓΓΓΓΓΓ ΉΑ÷ΟΔώΒΡ≤ΜΉψ÷°¥Π «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§
ΉΑ÷ΟΔρΒΡ≤ΜΉψ÷°¥Π « ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘΜ
ΓΓ (3)«κΡψ¥”ΝΫΧΉΉΑ÷Ο÷–―Γ»ΓΡψ»œΈΣΚœάμΒΡ≤ΩΖ÷Θ§Α¥¥”ΉσΒΫ”“ΒΡΥ≥–ρΉιΉΑ“ΜΧΉ÷Τ»ΓCaH2ΒΡΚœάμΉΑ÷Ο(”Ο–ρΚ≈AΓΔBΓΔCΓ≠Γ≠±μ Ψ)ΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΓΓ (4)Φλ≤ιΆξΉΑ÷ΟΒΡΤχΟή–‘ΚσΘ§ΈΣΝΥ±Θ÷Λ≤ζΤΖΒΡ¥ΩΕ»ΚΆ Β―ιΑ≤»Ϊ±Ί–κœ»ΓΓΓΓΓΓΓΓ Θ§»ΜΚσ‘Ό
ΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ§≤≈ΡήΒψ»ΦΨΤΨΪΒΤΦ”»»ΓΘΆ§―υΘ§ΈΣΝΥΑ≤»ΪΘ§Ζ¥”ΠΩΣ ΦΚσΘ§‘ΎEΩΎ¥Π”ΠΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΓΓΓΓ (5)Ψϋ ¬ΚΆΤχœσ“ΑΆβΉς“Β≥Θ”ΟCaH2Ήω…ζ«βΦΝΘ§ Ι÷°”κΥ°Ζ¥”Π≤ζ…ζH2Θ§ΤδΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
[―ΓΉω≤ΩΖ÷]
Ι≤8ΗωΧβΘ§ΩΦ…ζ±Ί–κ¥”÷–―Γ‘ώ1ΗωΈοάμΧβΓΔ1ΗωΜ·―ßΧβΚΆ1Ηω…ζΈοΧβ‘Ύ¥πΧβ÷ΫΙφΕ®ΒΡ«χ”ρΉς¥πΓΘ
30Θ°(14Ζ÷)
A-JΖ÷±π±μ Ψ÷–―ßΜ·―ß÷–≥ΘΦϊΒΡ“Μ÷÷Έο÷ Θ§ΥϋΟ«÷°ΦδœύΜΞΙΊœΒ»γœ¬ΆΦΥυ Ψ(≤ΩΖ÷Ζ¥”ΠΈοΓΔ…ζ≥…ΈοΟΜ”–Ν–≥ω)Θ§«““―÷ΣGΈΣ÷ςΉε‘ΣΥΊΒΡΙΧΧ§―θΜ·ΈοΘ§AΓΔBΓΔCΓΔDΓΔEΓΔFΝυ÷÷Έο÷ ÷–ΨυΚ§Ά§“Μ÷÷‘ΣΥΊΓΘ«κΧν–¥œ¬Ν–Ω’ΑΉΘΚ
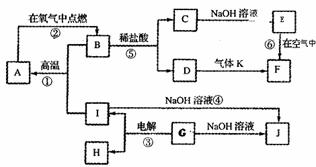
ΓΓ (1)AΓΔBΓΔCΓΔDΓΔEΓΔFΝυ÷÷Έο÷ ÷–ΒΡΚ§”–Ά§“Μ÷÷‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΈΜ÷ΟΓΓΓΓΓΓΓΓΓΓ Θ§
ΓΓ (2)–¥≥ωΦλ―ιD»ή“Κ÷–―τάκΉ”ΒΡΖΫΖ®ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (3)–¥≥ωΖ¥”ΠΔήΒΡάκΉ”ΖΫ≥Χ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (4)»τ28gAΒΞ÷ ‘ΎΉψΝΩΒΡ―θΤχ÷–ΉΤ…’Θ§Ζ¥”ΠΖ≈≥ωΒΡ»»ΝΩΈΣQkJ(QΘΨ0)Θ§–¥≥ω’βΗωΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΓΓ (5)»τœρΤχΧεKΒΡΥ°»ή“Κ÷–Φ”»κ―ΈΥαΘ§ ΙΤδ«ΓΚΟΆξ»ΪΖ¥”ΠΘ§ΥυΒΟ»ή“ΚΒΡpHΓΓΓΓΓΓ 7
ΓΓΓΓ (ΧνΓΑΘΨΓ±ΓΔΓΑΘΦΓ±ΜρΓΑ=Γ±)Θ§”ΟάκΉ”ΖΫ≥Χ Ϋ±μ ΨΤδ‘≠“ρΘΚΓΓΓΓΓΓ ΓΓΓΓΘΜ»τœρΤχΧεKΒΡ0.1mol/LΥ°»ή“Κ÷–Φ”»κpH=1ΒΡΝρΥαΘ§«“Α±Υ°”κΝρΥαΒΡΧεΜΐ±»ΈΣ1ΘΚ1Θ§‘ρΥυΒΟ»ή“Κ÷–Κ§ΗςάκΉ”Έο÷ ΒΡ÷ ΝΩ≈®Ε»”…¥σΒΫ–ΓΒΡΙΊœΒ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΘ
29Θ°(12Ζ÷)
“‘ΚΘΥ°÷–≥ΘΦϊΈο÷ AΈΣ‘≠ΝœΩ…“‘ΖΔ’ΙΚήΕύ÷÷ΙΛ“ΒΘ§œ¬ΆΦ÷–ΑϋΚ§ΝΥ÷–―ßΩΈ±Ψ÷–Ϋι…ήΒΡΦΗ÷÷Μυ±ΨΙΛ“Β…ζ≤ζΘ§«κΗυΨίΈο÷ ÷°ΦδΒΡΉΣΜ·ΙΊœΒΜΊ¥πœ¬Ν–Έ ΧβΘΚ
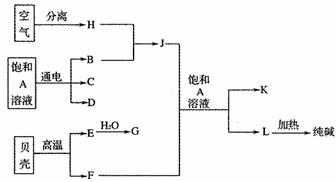
ΓΓ (1)CΚΆDΓΔCΚΆGΖ¥”ΠΕΦΩ…“‘÷Τ»ΓœϊΕΨΦΝΓΘCΚΆGΖ¥”Π÷Τ»ΓΒΡœϊΕΨΦΝ÷–”––ß≥…Ζ÷ΒΡΜ·―ß ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΓΓ (2)–¥≥ωΒγΫβA»ή“ΚΒΡΜ·―ßΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΓΓ (3)»τ ΙΙΛ“ΒΚœ≥…JΖ¥”ΠΒΡΤΫΚβœρ…ζ≥…JΒΡΖΫœρ“ΤΕ·Θ§Ω…≤…»ΓΒΡ¥κ ©”–ΓΓΓΓΓΓΓΓΓΓ (ΧνΉ÷ΡΗ¥ζΚ≈)ΘΜ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ AΘ°…ΐΗΏΈ¬Ε»ΓΓΓΓ BΘ°‘ω¥σ―Ι«ΩΓΓΓΓΓΓΓΓΓΓΓΓ CΘ° Ι”Ο¥ΏΜ·ΦΝΓΓΓΓΓΓΓΓ DΘ°“ΚΜ·Ζ÷άκ
ΓΓ (4)ΫΪFΚΆJΆ®»κAΒΡ±ΞΚΆ»ή“Κ÷–ΒΡΥ≥–ρΈΣ ΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ AΘ°œ»Ά®»κFΚσΆ®»κJΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°œ»Ά®»κJΚσΆ®»κF
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°Ά§ ±Ά®»κΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°ΟΜ”–œ»ΚσΥ≥–ρ“Σ«σ
ΓΓ (5)ΆΦ÷–Υυ ΨΙΛ“Β÷ΤΖ®ΜώΒΟΒΡ¥ΩΦν÷–≥ΘΚ§”–NaCl‘”÷ Θ§”Οœ¬ ωΖΫΖ®Ω…“‘≤βΕ®―υΤΖ÷–NaClΒΡ÷ ΝΩΖ÷ ΐΓΘ
ΓΓΓΓ 
ΔΌΦλ―ι≥ΝΒμ «Ζώœ¥Β”Η…ΨΜΒΡΥυ”ΟΒΫΒΡ ‘ΦΝ «ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§
ΔΎ―υΤΖ÷–NaClΒΡ÷ ΝΩΖ÷ ΐΒΡ ΐ―ß±μ¥ο ΫΈΣΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
3Θ°ΒΎΔρΨμΥυ”–ΧβΡΩΒΡ¥πΑΗΩΦ…ζ–κ”ΟΚΎ…ΪΜράΕ…ΪΗ÷± ΓΔ‘≤÷ι± ‘Ύ¥πΧβ÷ΫΙφΕ®ΈΜ÷Ο…œΘ§‘Ύ ‘ΧβΨμ…œ¥πΧβΈό–ßΓΘ
(±ΊΉω≤ΩΖ÷)
15Θ°ΗυΨίœ¬ΆΦ Β―ιœ÷œσΘ§ΥυΒΟΫα¬έ≤Μ’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
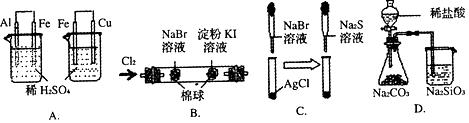
|
Β―ι |
Β―ιœ÷œσ |
Ϋα¬έ |
|
AΘ° |
ΉσΙΐ…’±≠÷–Χζ±μΟφ”–Τχ≈ίΘ§”“±Ώ…’±≠÷–Ά≠±μΟφ”–Τχ≈ί |
ΜνΕ·–‘ΘΚAlΘΨFeΘΨCu |
|
BΘ° |
Ήσ±ΏΟόΜ®±δΈΣ≥»…ΪΘ§”“±ΏΟόΜ®±δΈΣάΕ…Ϊ |
―θΜ·–‘ΘΚCl2ΘΨBr2ΘΨI2 |
|
CΘ° |
ΑΉ…ΪΙΧΧεœ»±δΈΣΒ≠ΜΤ…ΪΘ§Κσ±δΈΣΚΎ…Ϊ(Ag2S) |
»ήΫβ–‘ΘΚAgClΘΨAgBrΘΨAg2S |
|
DΘ° |
ΉΕ–ΈΤΩ÷–”–ΤχΧε≤ζ…ζΘ§…’±≠÷–“ΚΧε±δΜκΉ« |
Υα–‘ΘΚHClΘΨH2CO3ΘΨH2SiO3 |
ΒΎΔρΨμ(±ΊΉω128Ζ÷+―ΓΉω24Ζ÷Θ§Ι≤152Ζ÷)
|
14Θ°œ¬Ν–άκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ ΓΓ)
ΓΓΓΓΓΓ AΘ°ΙΐΝΩΧζΖέ»ή”ΎœΓHNO3÷–ΘΚFe+NO3-+4H+=Fe3++NOΓϋ+2H2O
ΓΓΓΓΓΓ BΘ°Ιΐ―θΜ·ΡΤΙΧΧε”κΥ°Ζ¥”ΠΘΚ2O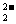 +2H2O=4OH-+O2Γϋ
+2H2O=4OH-+O2Γϋ
ΓΓΓΓΓΓ CΘ°¥Έ¬»ΥαΗΤ»ή“Κ÷–Ά®»κΙΐΝΩΕΰ―θΜ·ΧΦΘΚ
ΓΓΓΓΓΓ Ca2++2ClO-+CO2+H2O===CaCO3Γΐ+2HClO
ΓΓΓΓΓΓ DΘ°ΙΐΝΩNaHSO4»ή“ΚΦ”»κΒΫBa(OH)2»ή“Κ÷–ΘΚ
ΓΓΓΓΓΓ
2H++SO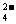 +Ba2++2OH-=2H2O+BaSO4Γΐ
+Ba2++2OH-=2H2O+BaSO4Γΐ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com