
9.下列离子方程式书写正确的是: ( )
A.碳酸氢钾水解:HCO3-+H2O H3O++CO32-
H3O++CO32-
B.向硝酸银溶液中加入过量氨水:Ag++NH3·H2O=AgOH↓+NH4+
C.浓度均为0.1mol·L-1的氢氧化钡溶液与碳酸氢铵溶液等体积混合
Ba2++2OH-+NH4++ HCO3-=BaCO3↓+NH3·H2O+H2O
D.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3-
8.设阿伏加德罗常数为NA,下列说法正确的是: ( )
A.1mol Cl2与足量Fe反应,转移的电子数为3NA
B.20g重水(D2O)中含有的中子数为8 NA
C.常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA
D.标准状况下,22.4L已烷中共价键数目为19NA
7.下列是某学生自己总结的一些规律,其中正确的是: ( )
A.氧化物不可能是还原产物,只可能是氧化产物
B.有些化学反应不属于化合、分解、置换、复分解中的任何一种反应
C.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
D.将Mg(HCO3)2溶液加热,最终得到Mg(OH)2沉淀,由此可知溶解度
Mg(OH)2> Mg(HCO3)2
6.焰火“脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。下列说法中正确的是: ( )
A.非金属单质燃烧时火焰均为无色 B.所有金属及其化合物灼烧时火焰均有颜色
C.焰色反应均应透过蓝色钴玻璃观察 D.NaCl与Na2CO3灼烧时火焰颜色相同
27.(18分)某化学活动小组设计以下装置,进行不同的实验。其中a为用于鼓入空气的气囊,b为螺旋状铜丝,c为喷有少量碱液的棉花,d中盛有冰水。
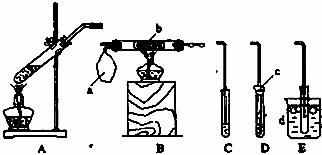
(1)若用A装置做乙醇与乙酸发生酯化反应的实验,则还需连接的仪器是(填序号) ,该仪器中应加入的试剂是 。从实验安全角度考虑,A装置试管中除加入反应液外,还需加入的物质是 。
(2)该小组同学欲做浓硫酸与铜反应的实验,并检验产生的二氧化硫。他们应选用的装置是(填序号) ,用于检验产物二氧化硫应选用的试剂是 ,
(3)该小组同学欲做乙醇氧化成乙醛的实验,他们应选用的装置是(填序号) 。
写出乙醇催化氧化生成乙醛的化学方程式 。
(4)该小组同学欲用A装置做铜与浓硝酸反应的实验,请你判断该实验是否可行(填“是”或“否”), 。写出铜与浓硝酸反应的离子方程式 。
选考题(每科选做1题,共做3题)
26.(9分) A、B、C、D、E、F六种中学常见的物质,皆由短周期元素组成,有如图的转化关系:
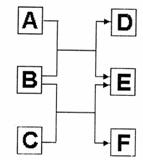
(1)若A、C、E皆为氧化物,且常温下A为无色液体,E为有毒气体。
①B、D、F皆为非金属单质,且D为气体。则A的电子式为 。
②B与C反应生成E和F的化学方程式为
(2)若B是由两种短周期元素组成的离子化合物,
A、C为氧化物,E为气体单质,D、F是均有三种元素组成的离子化合物,它们的水溶液均呈碱性,相同浓度时D溶液的pH大于F溶液的pH值。则:B和C反应生成E和F的化学方程式为 ,
列举该反应的一种用途 。
25.(16分)氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
□ +□C+□N2 □Si3N4+□CO
□Si3N4+□CO
(1)补充并配平上述反应的化学方程式(填写化学式和化学计量数)。
(2)该反应的平衡常数表达式为K =_______________________;升高温度时平衡常数减小,则其反应热DH________零(填“大于”、“小于”或“等于”);若在一定温度下,当上述反应达到平衡时增加氮气的流量,平衡常数将 (填“增大”、“减小”或“不变”)。
(3)当制得14g Si3N4时,碳将 (填“得到”或“失去”) mol电子, 增加碳的用量时平衡 (填“正向移动”、“逆向移动”或“不移动”)。
(4)氮化硅作为新型材料,具有耐高温、耐腐蚀、抗氧化、耐磨损等优异性能。但作为结构材料,它还存在抗机械冲击强度低、容易发生脆性断裂等缺点。为此工业上常以氮化硅作为基体,加入碳化硅作为添加剂来制造复合材料。以下属于复合材料的是 。
A.玻璃钢 B.钢筋混凝土 C.聚苯乙烯塑料 D.搪瓷
13.常温下,0.1mol·L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是 ( )
A.该溶液中由水电离出的c(H+)=1×10-13mol·L-1
B.由pH=3的HA与pH=11的NaOH溶液等体积混合,溶液中
c(Na+)>c(A-)>c(OH-)>c(H+)
C.浓度均为0.1mol/L的HA和NaA溶液等体积混合,若溶液呈酸性,则
c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-)
D.0.1mol·L-1HA溶液与0.05mol·L-1NaOH溶液等体积混合后所得溶液中
c(H+)+c(Na+)=c(OH-)+c(A-)
第Ⅱ卷(必考题129分,选考题45分,共174分)
必考题(共 道题)
12.下列实验仪器使用及操作正确的是 ( )
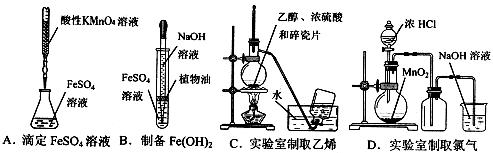
11.最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应为:
Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是 ( )
A.该电池Zn为负极,ZnO为正极,MnO2为催化剂
B.导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn
C.该电池的正极反应为:MnO2+e-+H2O=MnO(OH)+OH-
D.电池工作时正极发生氧化反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com