
12.如图所示,不同温度和压强下,在固定容积的密闭容器中对可逆反应:
4L(g) 2M(g)+N(g);△H>0平衡状态的影响(
2M(g)+N(g);△H>0平衡状态的影响( ),图中Y轴可以表示的涵义是:
),图中Y轴可以表示的涵义是:
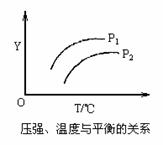
A.体系中物质L的百分含量
B.体系中总的气体分子数目
C.气体混合物的平均相对分子质量
D.气体混合物的密度
11.将1mol H2(g)和2mol I2(g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+ I2(g) 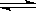 2HI(g); △H<0 ,并达到平衡。HI的体积分数ω(HI)随时间变化如图(Ⅱ)所示,若改变反应条件,ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是
2HI(g); △H<0 ,并达到平衡。HI的体积分数ω(HI)随时间变化如图(Ⅱ)所示,若改变反应条件,ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是
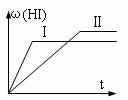
A.恒温恒容条件下,加入适当催化剂
B.恒温条件下,缩小反应容器体积
C.恒容条件下升高温度
D.恒温条件下,扩大反应容器体积
10.某温度下,在一容积可变的容器中,反应 2A(g) + B(g) 2C(g)达到平衡时,A、B 和C的物质的量分别为 4 mol、2 mol和 4 mol 。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
2C(g)达到平衡时,A、B 和C的物质的量分别为 4 mol、2 mol和 4 mol 。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
A.均减半 B.均加倍 C.均增加 1 mol D.均减少 1 mol
9.将4g铝、铁合金粉末溶于足量盐酸中,加入过量氢氧化钠溶液,过滤后在滤液中通入足量二氧化碳,再将沉淀滤出,经洗涤、干燥、灼烧后得到固体粉末的质量仍为4 g,原合金中铁的质量分数最接近
A.30% B.47% C.53% D.70%
8.在固定容积的密闭容器中,可逆反应2X + Y(g) Z(s) 已达到平衡,此时升高温度则气体混合物的密度增大。下列叙述正确的是
Z(s) 已达到平衡,此时升高温度则气体混合物的密度增大。下列叙述正确的是
A.若X为非气态,则正反应为吸热反应
B.正反应为放热反应,X为气态
C.在平衡混合物中加入少量Z,则平衡向左移动
D.压强变化对该平衡没有影响
7.在25℃时,有80g饱和Ba(OH)2溶液,向其中加入纯BaO粉末a g,反应后温度恢复到25℃,下列有关该溶液的说法正确的是
A.溶液中c(Ba2+)将增大 B.溶液的pH将增大
C.溶液中Ba2+总数将减少 D.溶液中c(OH-)减少
6.下列各组离子能在指定溶液中,大量共存的是
①无色溶液中:K+,Cl-,Na+,H2PO4-,PO43-,SO42-
②PH=11的溶液中:CO32-,Na+,AlO2-,NO3-,S2-,SO32-
③水电离的H+浓度C(H+)=10-12mol·L-1的溶液中:Cl-,HCO3-,NO3-,NH4+,S2O32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使石蕊变红的溶液中:Fe3+, NO3-,Na+,SO42-
⑥酸性溶液中:Fe2+,Al3+,NO3-,I-,Cl-,S2-
A.①②③④⑤⑥ B.①②⑥ C.②④⑤ D.①②⑤
5.制取Fe(OH)2并使之能久存,可采取的操作有:①加入一些植物油,②溶解FeSO4配成溶液,③把蒸馏水加热煮沸并密封冷却,④加入少量铁屑,⑤加入少量CCl4,⑥向FeSO4溶液中滴入足量氨水,⑦把盛有氨水的滴管伸入FeSO4溶液中后再挤出氨水。其中必须进行的操作及其正确顺序是
A.③②④①⑦ B.③②⑤⑥④ C.③②④⑤⑦ D.②④①⑦⑤
4.已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下
(1)CuSO4 + Na2CO3
主要:Cu2+ + CO32-+ H2O → Cu(OH)2↓+CO2↑ 次要:Cu2+ + CO32-→CuCO3↓
(2)CuSO4 + Na2S
主要:Cu2+ + S2-→ CuS↓ 次要:Cu2+ + S2-+ 2H2O→Cu(OH)2↓+ H2S↑
据此,下列几种物质溶解度大小比较中,正确的是
A.Cu(OH)2 > CuCO3 > CuS B.CuCO3 > Cu(OH)2 > CuS
C.CuS > CuCO3 > Cu(OH)2 D.CuS > Cu(OH)2 > CuCO3
3.下列实验操作正确的是
①用带橡皮塞的棕色试剂瓶存放浓硫酸
②检查容量瓶是否漏水的方法是:往容量瓶中加水,塞好瓶塞,将容量瓶倒过来,若不漏水,将瓶塞旋转180°,再倒过来,看是否漏水
③配置氯化铁溶液时,将一定量氯化铁溶解在较浓的盐酸中,再用水稀释到所需浓度
④可用FeCl3溶液除去试管内难以刷去的铜迹
⑤欲测某溶液的pH,需先用蒸馏水润湿pH试纸,再用洁净、干燥的玻璃棒蘸取该溶液滴在试纸上,并与标准比色卡比较
⑥分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
⑦蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口附近
⑧滴定管装液前,应该检查是否漏水
A.①④ B.②④⑤ C.①③ D.②③④⑥⑦⑧
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com