
17.下列各种溶液中,可能大量共存的离子组是
A.pH=0的溶液中: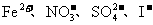
B.由水电离出的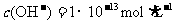 的溶液中:
的溶液中: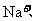
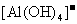 、
、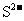 、
、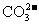
C.含有大量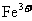 的溶液中:
的溶液中: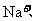
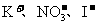
D.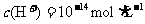 的溶液中:
的溶液中: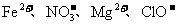
16.常温下,关于溶液的稀释说法正确的是
A.将1L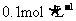 的
的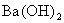 溶液加水稀释为2L,pH=13
溶液加水稀释为2L,pH=13
B.pH=3的醋酸溶液加水稀释100倍,pH=5
C.pH=4的H2SO4加水稀释100倍,溶液中由水电离产生的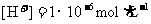
D.pH=8的NaOH溶液加水稀释100倍,其pH=6
15.下图是恒温下某反应的化学反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是
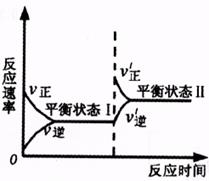
A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ
C.该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ
D.同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等
14.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为: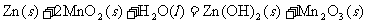 。则下列说法正确的是
。则下列说法正确的是
A.电池工作时,MnO2发生还原反应
B.电池负极的电极反应式为: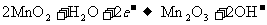
C.电池工作时,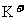 移向负极
移向负极
D.电池工作时,电路中每通过0.2mol电子,锌的质量理论上减少6.5g
13.已知HF、CH3COOH均为弱酸,酸性强弱顺序为HF>CH3COOH。下列说法不正确的是
A.浓度均为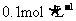 的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强
的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强
B.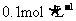 CH3COOH溶液,加水稀释过程中,所有离子浓度均减小
CH3COOH溶液,加水稀释过程中,所有离子浓度均减小
C.NaF溶液中含有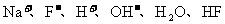 六种微粒
六种微粒
D.NaF溶液中加入少量NaOH固体,溶液中[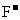 ]变小
]变小
12.已知31g红磷(P,固体)在氧气中燃烧生成P4O10固体放出738.5kJ热量,31g白磷(P4,固体)在氧气中燃烧生成P4O10固体放出745.8kJ热量。下列判断正确的是
A.白磷在氧气中燃烧的热化学方程式是: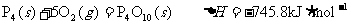
B.红磷转化成白磷时放出热量
C.红磷比白磷稳定
D.31g红磷中蕴含的能量为738.5kJ
11.蒸干并灼烧下列物质的水溶液,仍能得到该物质的是
A.氯化铝 B.碳酸氢钠 C.硫酸亚铁 D.碳酸钠
10.将1molCO和1molNO2充入密闭容器中,在催化剂存在下发生反应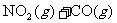

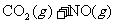 并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是
并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是
A.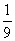 B.
B.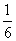 C.
C.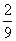 D.
D.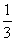
9.已知镁粉与冷水几乎不反应,与热水反应缓慢。市场上购买的“即热饭盒”底部有两层,一层装水,另一层是镁粉与铁粉的混合物,当水与金属粉末接触时会发生反应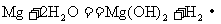 。则下列说法不正确的是
。则下列说法不正确的是
A.“即热饭盒”的工作原理是将化学能转化为热能
B.上述反应中,反应物的总焓大于生成物的总焓
C.铁粉的作用是催化剂
D.上述反应的反应热Q为正值
8.某学生想制作一种家用环保型消毒液发生器,用石墨做电极电解饱和NaCl溶液。通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液设计了如下图的装置,则对电源电极名称和消毒液的主要成分判断正确的是
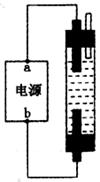
A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极,b为阳极;HClO和NaCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com