
6. œ¬¡–∏˜◊ÈŒÔ÷ º‰∑¥”¶ø…ƒÐ∞¸¿®∂ý≤Ω∑¥”¶£¨∆‰◊еƒ¿Î◊”∑Ω≥Ã Ω’˝»∑µƒ «
A£ÆNaClO»Ð“∫÷–Õ®»Îπ˝¡øSO2£∫ClO-+SO2+H2O===HClO+HSO3-
B£ÆAlCl3»Ð“∫÷–Õ∂»Îπ˝¡øNa£∫Al3++4Na+2H2O===AlO2-+4Na++2H2 °¸
C£ÆFeBr2»Ð“∫÷–Õ®»Î…Ÿ¡øCl2£∫2Fe2++4Br- +3Cl2===2Fe3++2Br2+6Cl-
D£ÆœÚ√˜∑ػГ∫÷–µŒº”Ba(OH)2£¨«°∫√ πSO42-≥¡µÌÕÍ»´£∫
2A13++3SO42-+3Ba2++6OH-===2A1(OH)3 °˝ +3BaSO4 °˝
5. œ¬¡– µ—È≤Ÿ◊˜’˝»∑µƒ «
A£Æ”√¥…€·€ˆ◊∆…’∏˜÷÷ƒ∆µƒªØ∫œŒÔ
B£Æ”√25mL¡øÕ≤¡ø»°5.2mLœ°¡ÚÀ·
C£Æ»°”√Ω Ùƒ∆ ±£¨”¶Ω´ £œ¬µƒ¥Ûøȃ∆∑≈ªÿ‘≠∆ø£¨ µ—ÈΩ· ¯£¨”ýœ¬µƒƒ∆–º”¶”√““¥º¥¶¿Ì
D£Æ÷–∫ÕµŒ∂® ±£¨”¶”√¥˝≤‚“∫»Ûœ¥µŒ∂®πÐ∫Õ◊∂–Œ∆ø
4. “ª∂®Œ¬∂»œ¬µƒº”»ðµÁΩ‚÷ AmBn‘⁄ÀƻГ∫÷–¥ÔµΩ≥¡µÌ»ÐΩ‚∆Ω∫‚ ±£¨∆‰∆Ω∫‚≥£ ˝
Ksp=cm(An+)•cn (Bm-)£¨≥∆Œ™ƒ—»ÐµÁΩ‚÷ µƒ»Ð∂»ª˝°£‘⁄25°Ê ±£¨AgClµƒ∞◊…´–¸◊«“∫÷–£¨“¿¥Œº”»Îµ»≈®∂»µƒKI»Ð“∫∫ÕNa2S»Ð“∫£¨π€≤ÏµΩµƒœ÷œÛ «œ»≥ˆœ÷ª∆…´≥¡µÌ£¨◊Ó∫Û…˙≥…∫⁄…´≥¡µÌ°£“—÷™”–πÿŒÔ÷ µƒ—’…´∫Õ»Ð∂»ª˝»Áœ¬£∫
|
ŒÔ÷ |
AgCl |
AgI |
Ag2S |
|
—’…´ |
∞◊ |
ª∆ |
∫⁄ |
|
Ksp(25°Ê) |
1.8°¡10-10 |
1.5°¡10-16 |
1.8°¡10-50 |
œ¬¡–– ˆ≤ª’˝»∑µƒ «
A£Æ»Ð∂»ª˝–°µƒ≥¡µÌø…“‘◊™ªØŒ™»Ð∂»ª˝∏¸–°µƒ≥¡µÌ
B£Æ25°Ê ±£¨±•∫ÕAgCl°¢AgI°¢Ag2S»Ð“∫÷–À˘∫¨Ag+µƒ≈®∂»œýÕ¨
C£Æ»Ùœ»º”»Î◊„¡øNa2S »Ð“∫£¨‘Ÿº”»ÎKI»Ð“∫£¨‘ڌު∆…´≥¡µÌ≤˙…˙
D£Æ25°Ê ±£¨AgCl πÃÑ⁄µ»ŒÔ÷ µƒ¡ø≈®∂»µƒNaCl°¢CaCl2»Ð“∫÷–µƒ»Ð∂»ª˝œýÕ¨
3. œ¬¡–Àµ∑®≤ª’˝»∑µƒ «
A£Ææ≤µÁ≥˝≥æ¿˚”√¡ÀΩ∫ÃÐ∑¢…˙µÁ”浃–‘÷
B£Æ“∫∞±°¢“∫¬»°¢“∫謻ªØ«‚∂º «∑«µÁΩ‚÷
C£ÆÀ˘”–µƒ÷√ªª∑¥”¶∂º «—ıªØªπ‘≠∑¥”¶
D£Æ πø’∆¯÷–”Œ¿Î赃µ™◊™ªØŒ™∫¨µ™ªØ∫œŒÔµƒ∑Ω∑®Ω–◊ˆµ™µƒπÃ∂®
2. ¿˚”√∫À怱‰∑¢µÁ£¨3He «◊Ó«ÂΩý◊Ó∞≤»´µƒ¿ÌœÎŒÔ÷ £¨µÿ«Ú…œµ™‘™Àÿ÷˜“™“‘4He–Œ Ω¥Ê£¨3HeΩˆ”–15∂÷◊Û”“°£∂¯‘¬«Ú…œµƒ3He”– ˝∞ŸÕÚ∂÷÷Æ∂ý£¨ø…π©»´ ¿ΩÁø™≤…500ƒÍ°£œ¬¡–Àµ∑®’˝»∑µƒ «
¢Ÿ3He°¢4HeµƒªØ—ß–‘÷ ª˘±æœýÕ¨
¢⁄3He°¢4Heæþ”–œýÕ¨µƒ÷–◊” ˝
¢€3He∫À怱‰ «ªØ—ß±‰ªØ
¢Ð3He“∫ªØ «ŒÔ¿Ì±‰ªØ
¢ð3He°¢4He–Œ≥…µƒµ•÷ ÷–æ˘∫¨”–∑«º´–‘º¸
¢Þ3He°¢4He∑÷±◊È≥…µƒ∆¯Ãµ•÷ £¨‘⁄œýÕ¨Ãıº˛œ¬√Ð∂»÷Ʊ»Œ™3£∫4
°°°°°° A£Æ ¢Ÿ¢⁄¢ð°° °°°° B£Æ ¢Ÿ¢Ð¢Þ°° °° C£Æ ¢⁄¢€¢ð°°°° °°°°°° °°D£Æ ¢€¢Ð¢Þ
1. 2008 ƒÍ8‘¬8»’÷¡24»’£¨29ΩÏ∞¬‘Àª·‘⁄±±æ©¬°÷ÿ柖–°£œ¬¡–”–πÿ2008ƒÍ±±æ©∞¬‘Àª·µƒ–˚¥´±®µ¿÷–√ª”–√˜œ‘ ß µµƒ «
A£Æ∞¬‘Àª·“™Õª≥ˆ°∞¬Ã…´∞¬‘À°±¿ÌƒÓ£¨ «÷∏∞¬‘À≥°πðΩ®…Ëæ˘ π”√ÃÏ»ª≤ƒ¡œ£¨≤ª π”√∫œ≥…≤ƒ¡œ
B£Æ∞¬‘Àª·∆⁄º‰π´Ωª≥µ¥Û¡ø≤…”√±˚ÕÈ°¢ø’∆¯º∞≤¨∆¨◊È≥…µƒ»º¡œµÁ≥ÿ£¨∏√µÁ≥ÿ÷–Õ®»Î±˚Õȵƒ“ªº´ «µÁ≥ÿµƒ’˝º´
C£Æ”Œ”æπð°∞ÀÆ¡¢∑Ω°±≤…”√ ETFE[æ€∑˙““œ©(C2H2F2)n]ÀСœƒ§◊˜Œ™¡¢√ÊŒ¨ª§Ω®÷˛ÃÂœµµƒ≤ƒ¡œ£¨À¸ Ù”⁄ÃÏ»ª∏þ∑÷◊”≤ƒ¡œ
D£Æ∞¬‘Àª·Ω±≈∆…œ√Êœ‚«∂°∞”Ò°±£¨∆‰÷˜“™ªØ—ß≥…∑÷Œ™∫¨ÀÆ∏∆√浃πËÀ·—Œ£¨ø…”√—ıªØŒÔ–Œ Ω±Ì æ£¨»Á2CaO•5MgO• 8SiO2•H2O
33£Æ(8∑÷)[ªØ—ß--”–ª˙ªØ—ߪ˘¥°]
Ã˛A 2.9gÕÍ»´»º…’…˙≥…8.8g 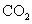 ∫Õ4.5g
∫Õ4.5g 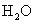 £¨À¸µƒ“ª¬»»°¥˙≤˙ŒÔB∫ÕC∑÷±”ΫøºÓµƒ¥º»Ð“∫π≤»»£¨∂º÷ªƒÐµ√µΩ”–ª˙ªØ∫œŒÔD°£«Î∏˘æðœ¬ÕºÀ˘ æ∏˜”–ª˙ŒÔ÷ƺ‰µƒ◊™ªØÃÓø’£∫
£¨À¸µƒ“ª¬»»°¥˙≤˙ŒÔB∫ÕC∑÷±”ΫøºÓµƒ¥º»Ð“∫π≤»»£¨∂º÷ªƒÐµ√µΩ”–ª˙ªØ∫œŒÔD°£«Î∏˘æðœ¬ÕºÀ˘ æ∏˜”–ª˙ŒÔ÷ƺ‰µƒ◊™ªØÃÓø’£∫

°°°° (1)Aµƒ∑÷◊” ΩŒ™______________£ª
°°°° (2)–¥≥ˆΩ·ππºÚ Ω£∫C___________________£¨E________________£ª
°°°° (3)B°˙D°¢G°˙H∑¢…˙∑¥”¶µƒ∑¥”¶¿ý–Õ“¿¥Œ «_____________°¢_____________£ª
°°°° (4)–¥≥ˆF°˙GµƒªØ—ß∑Ω≥à Ω______________________________°£
32£Æ(8∑÷)[ªØ—ß--ŒÔ÷ Ω·ππ”Ζ‘÷ ]
A°¢B°¢C°¢DÀƒ÷÷‘™Àÿ¥¶”⁄Õ¨“ª÷Ð∆⁄£¨‘⁄Õ¨◊‘™Àÿ£¨Aµƒ∆¯Ã¨«‚ªØŒÔµƒ∑–µ„◊Ó∏þ£¨Bµƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀƪ،ԵƒÀ·–‘‘⁄Õ¨÷Ð∆⁄÷– «◊Ó«øµƒ£¨CµƒµÁ∏∫–‘ΩÈ”⁄A°¢B÷ƺ‰£¨D”ÎBœý¡⁄°£
°°°° (1)C‘≠◊”µƒº€µÁ◊”≈≈≤º ΩŒ™____________________£ª
°°°° (2)A°¢B°¢C»˝÷÷‘™Àÿ‘≠◊”µƒµ⁄“ªµÁ¿ÎƒÐ”…¥ÛµΩ–°µƒÀ≥–Ú «(–¥‘™Àÿ∑˚∫≈)______£ª
°°°° (3)Bµƒµ•÷ ∑÷◊”÷–¥Ê‘⁄______∏ˆ¶–º¸£ª
°°°° (4)D∫ÕB–Œ≥…“ª÷÷≥¨”≤°¢ƒÕƒ•°¢ƒÕ∏þŒ¬µƒ–¬–ÕªØ∫œŒÔ£¨∏√ªØ∫œŒÔ Ù”⁄_______æßã¨∆‰”≤∂»±»Ω∏’ Ø_____________(ÃÓ°∞¥Û°±ªÚ°∞–°°±)
°°°° (5)Aµƒ∆¯Ã¨«‚ªØŒÔµƒ∑–µ„‘⁄Õ¨◊Â÷–◊Ó∏þµƒ‘≠“Ú «_________________°£
31£Æ(8∑÷)[ªØ—ß--ªØ—ߔκº ı]
°°°° «Î∏˘æð𧓵÷∆¡ÚÀ·µƒ”–πÿ÷™ ∂ªÿ¥œ¬¡–Œ £∫
°° (1)ª∆Ã˙øÛ‘⁄∑–Ã⁄¬Ø÷–∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™___________________________£ª
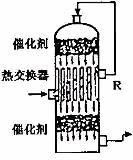
(2)‘⁄¡ÚÀ·π§“µ…˙≤˙÷–£¨Œ™¡À”–¿˚”⁄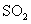 µƒ◊™ªØ£¨«“ƒÐ≥‰∑÷¿˚”√»»ƒÐ£¨≤…”√¡À÷–º‰”–»»Ωªªª∆˜µƒΩ”¥• “(º˚œ¬Õº)°£∞¥¥À√б’ÃÂœµ÷–∆¯Ãµƒ¡˜œÚ£¨‘Ú‘⁄R¥¶¡˜≥ˆµƒ∆¯ÃÂ÷–≥˝
µƒ◊™ªØ£¨«“ƒÐ≥‰∑÷¿˚”√»»ƒÐ£¨≤…”√¡À÷–º‰”–»»Ωªªª∆˜µƒΩ”¥• “(º˚œ¬Õº)°£∞¥¥À√б’ÃÂœµ÷–∆¯Ãµƒ¡˜œÚ£¨‘Ú‘⁄R¥¶¡˜≥ˆµƒ∆¯ÃÂ÷–≥˝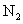 Õ‚µƒ÷˜“™◊È≥…Œ™________(ÃÓ–Ú∫≈)£ª
Õ‚µƒ÷˜“™◊È≥…Œ™________(ÃÓ–Ú∫≈)£ª
°°°°°°°°
A£Æ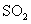 °°°°°°°°°°
°°°°°°°° B£Æ
°°°°°°°°°°
°°°°°°°° B£Æ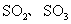
°°°°°°°°
C£Æ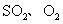 °°°° °°°°°°°°°° D£Æ
°°°° °°°°°°°°°° D£Æ
°° (3)Ω”¥•∑®÷∆¡ÚÀ·π˝≥Ã÷–£¨∑¥”¶2SO2(g)+ O2(g)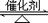 2SO3(g) °˜H<0
2SO3(g) °˜H<0
°°°°°°°° ‘Úœ¬¡–”–πÿÕºœÒ’˝»∑µƒ «_______________(◊¢£∫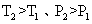 £¨ÃÓ–Ú∫≈)£ª
£¨ÃÓ–Ú∫≈)£ª
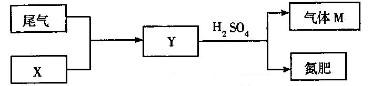
(4)œ¬Õº «π§“µ÷∆¡ÚÀ·Œ≤∆¯µƒ◊€∫œ¿˚”√£¨∆¯ÃÂMªÿ ’∫Ûø…Ω¯»ÎΩ”¥• “—≠ª∑…˙≤˙£¨«Î∏˘æðÕº æ≈–∂œX «(ÃÓ√˚≥∆)_____£¨–¥≥ˆY”ΡÚÀ·∑¥”¶…˙≥…MµƒªØ—ß∑Ω≥à Ω___________°£
30£Æ(13∑÷)ƒ≥—–æø–‘—ßœ∞–°◊È∂‘π˝¡øÃø∑€”ΗıªØÃ˙∑¥”¶µƒ∆¯ÃÂ≤˙ŒÔ≥…∑÷Ω¯––—–æø°£
°° (1)÷≥ˆºŸ…Ë£∫∏√∑¥”¶µƒ∆¯ÃÂ≤˙ŒÔ»´≤ø∂º «∂˛—ıªØú
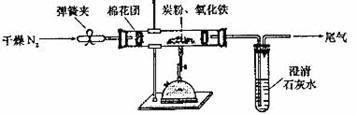
(2)…˺∆∑Ω∞∏£∫»ÁÕºÀ˘ æ£¨Ω´“ª∂®¡øµƒ—ıªØÃ˙‘⁄∏Ùæ¯ø’∆¯µƒÃıº˛œ¬”Îπ˝¡øÃø∑€ÕÍ»´∑¥”¶£¨≤‚¡ø≤Œº”∑¥”¶µƒÃº‘™Àÿ”Ηı‘™Àÿµƒ÷ ¡ø±»
(3)≤È‘ƒ◊ ¡œ£∫µ™∆¯≤ª”Îú°¢—ıªØÃ˙∑¢…˙∑¥”¶°£ µ—È “ø…“‘”√¬»ªØÔß±•∫ջГ∫∫Õ—«œıÀ·ƒ∆(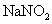 )±•∫ջГ∫ªÏ∫œº”»»∑¥”¶÷∆µ√µ™∆¯°£«Î–¥≥ˆ∏√∑¥”¶µƒ¿Î◊”∑Ω≥à Ω_____£∫
)±•∫ջГ∫ªÏ∫œº”»»∑¥”¶÷∆µ√µ™∆¯°£«Î–¥≥ˆ∏√∑¥”¶µƒ¿Î◊”∑Ω≥à Ω_____£∫
(4) µ—È≤Ÿ◊˜º∞ µ—Èœ÷œÛ£ª
¢Ÿ∞¥…œÕº¡¨Ω”◊∞÷√£¨≤¢ºÏ≤È◊∞÷√µƒ∆¯√Ж‘£¨≥∆»°3.20g—ıªØÃ˙”Î2.00gÃø∑€ªÏ∫œæ˘‘»°£∑≈»Î48.48gµƒ”≤÷ ≤£¡ßπÐ÷–£ª
°°°°°°°° ¢⁄º”»»«∞£¨œ»Õ®“ª∂Œ ±º‰¥øæª∏…‘Ôµƒµ™∆¯£ª
°°°°°°°° ¢€Õ£÷πÕ®»Î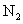 ∫Û£¨º–Ωٵت…º–£¨º”»»“ª∂Œ ±º‰£¨≥Œ«Â ت“ÀƱ‰ªÎ◊«£ª
∫Û£¨º–Ωٵت…º–£¨º”»»“ª∂Œ ±º‰£¨≥Œ«Â ت“ÀƱ‰ªÎ◊«£ª
°°°°°°°° ¢Ð¥˝∑¥”¶Ω· ¯£¨‘ŸÕ®“ª∂Œ ±º‰µƒµ™∆¯£¨»ª∫Û¿‰»¥÷¡ “Œ¬£¨≥∆µ√”≤÷ ≤£¡ßπÐ∫ÕπÃÃÂ◊Ð÷ ¡øŒ™52.24g°£
°° (5) ˝æ𥶿̣∫æ≠º∆À„£¨≤Œº”∑¥”¶µƒÃº‘™Àÿ÷ ¡øŒ™0.48g£¨—ı‘™Àÿ÷ ¡øŒ™0.96g°£µ√≥ˆ‘≠ºŸ…Ë≤ª≥…¡¢£¨¿Ì”… «_________________________________________________°£
°° (6)µ√≥ˆΩ·¬€£∫∏˘æð ˝æ𥶿ÌΩ·π˚≈–∂œ£¨∑¥”¶≤˙…˙µƒ∆¯Ã «_____________________£¨
°°°°°°°° ∏√ µ—È÷–∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™_______________________________________°£
°° (7) µ—È”≈ªØ£∫∏˘æ𠵗ȵ√≥ˆµƒΩ·¬€”¶∂‘∏√ µ—È◊∞÷√Ω¯“ª≤ΩÕÍ…∆£¨«Îƒ„¥”œ¬ÕºÀ˘ æ◊∞÷√÷–—°»°±ÿ“™◊∞÷√£¨∂‘ µ—Ⱥ”“‘∏ƒΩ¯___________________________________°£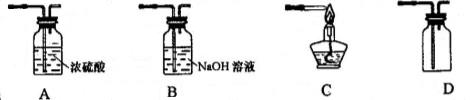
[—°◊ˆ≤ø∑÷]
π≤8∏ˆ–°Ã‚£¨øº…˙±ÿ–Î¥”÷–—°‘Ò2∏ˆŒÔ¿Ì°¢1∏ˆªØ—ßÃÂ∫Õ“ª∏ˆ…˙ŒÔ‘⁄¥Ã‚ø®πÊ∂®µƒ«¯”Ú◊˜¥°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com