
7£Æœ¬¡–¿Î◊”∑Ω≥Ã Ω’˝»∑µƒ «
A£Æ±Ω∑”ƒ∆»Ð“∫÷–Õ®»Î…Ÿ¡øCO2£∫C6H5O“ª ÆCO2+H2O°˙C6H5OH Æ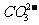 £ª
£ª
B£ÆNa2CO3»Ð“∫÷–Õ®»Îπ˝¡øCO2£∫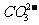 +CO2+H2O=2HCO3“ª
+CO2+H2O=2HCO3һ
C£ÆNH4ClπÃÔÎCa(OH)2πÃêÏ∫œ÷∆NH3£∫NH4++OH- NH3°¸+H2O
NH3°¸+H2O
D£ÆSO2∆¯ÃÂÕ®»ÎNaClO»Ð“∫÷–£∫SO2+2ClO“ª ÆH2O===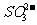 +2HClO
+2HClO
6£Æœ¬¡–±Ì æŒÔ÷ Ω·ππµƒªØ—ß”√”ÔªÚƒ£–ÕÕº’˝»∑µƒ «
A£ÆCO2µƒ±»¿˝ƒ£–Õ °°°°°°°°°°
B£ÆH2O2µƒµÁ◊” Ω£∫
°°°°°°°°°°
B£ÆH2O2µƒµÁ◊” Ω£∫
C£ÆHClOµƒΩ·ππ Ω£∫H“ªO“ªCl°°°°°° D£Æ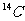 µƒ‘≠◊”Ω·ππ æ“‚Õº£∫
µƒ‘≠◊”Ω·ππ æ“‚Õº£∫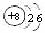
28£Æ(14∑÷)œ¬Õº±Ì æ∏˜ŒÔ÷ º‰µƒ◊™ªØπÿœµ°£“—÷™A°¢HŒ™¿Î◊”ªØ∫œŒÔ£¨HæßÃÂ÷–“ı°¢—Ù¿Î◊”µƒ∏ˆ ˝±»Œ™2£∫1£¨≥£”√◊˜∏…‘Ôº¡£¨D°¢EŒ™µ•÷ °£
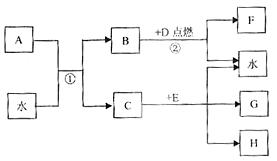
°°°° «Îªÿ¥£∫
°° (1)–¥≥ˆ∑¥”¶¢ŸµƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°° £ª“—÷™Bµƒ»º…’»» «1300kJ°§mol-1£¨–¥≥ˆ∑¥”¶¢⁄µƒ»»ªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°° °£
°° (2)G∫ÕHµƒªÏ∫œŒÔÀ◊≥∆°°°°°°°°°° £¨‘⁄ø’∆¯÷–“◊ ß–ß–Ë√Ð∑‚±£¥Ê£¨∆‰‘≠“Ú(”√ªØ—ß∑Ω≥à Ω)±Ì æ°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°° (3)E∫ÕNO2‘⁄ “Œ¬œ¬ø…“‘ªØ∫œ…˙≥…“ª÷÷–¬µƒ∆¯Ã¨ªØ∫œŒÔ°£ µ—È≤‚÷™£∫»°E∫ÕNO2ªÏ∫œ∆¯ÃÂ5L£¨µ±EÀ˘’ºÃª˝∑÷ ˝∑÷±Œ™20%°¢60%£¨∑¥”¶∫Û∆¯ÃµƒÃª˝æ˘Œ™4L(À˘”–∆¯ÃÂê˝‘⁄œýÕ¨Ãıº˛œ¬≤‚µ√)°£…˙≥…µƒ∆¯Ã¨ªØ∫œŒÔµƒ∑÷◊” Ω°°°°°°°°°° £¨∑¥”¶µƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°° °£
27£Æ(14∑÷)A°¢B°¢C°¢DŒ™∫¨”–œýÕ¨µÁ◊” ˝µƒ∑÷◊”ªÚ¿Î◊”°£Õ®≥£◊¥øˆœ¬£¨DŒ™ŒÞ…´“∫ð£
°°°° “—÷™£∫¢ŸA+B C+D°°°° ¢⁄C+D+º◊+NaCl==±˚°˝+““°° ¢€±˚
C+D°°°° ¢⁄C+D+º◊+NaCl==±˚°˝+““°° ¢€±˚ ¥øºÓ+º◊°¸+D
¥øºÓ+º◊°¸+D
«Îªÿ¥£∫
°° (1)º◊µƒµÁ◊” Ω°°°°°°°°°°°°°°°° °£
°° (2)𧓵”¶”√…œ ˆ∑¥”¶¢⁄¢€÷∆±∏¥øºÓ£¨ƒ≥ªÓ∂Ø–°◊È∏˘æð¥À‘≠¿Ì£¨Ω´∆¯Ãº◊Õ®»Î∫¨Cµƒ±•∫Õ ≥—ŒÀÆ÷–÷∆±∏±˚£¨ µ—È◊∞÷√»Áœ¬ÕºÀ˘ æ(Õº÷–º–≥÷°¢πÃ∂®”√µƒ“«∆˜Œ¥ª≠≥ˆ)°£
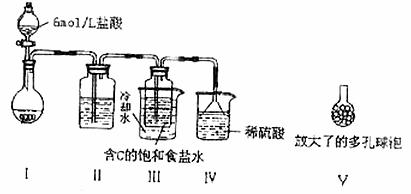
¢ŸI◊∞÷√÷–∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
¢⁄II◊∞÷√÷–À˘ ¢∑≈µƒ ‘º¡ «°°°°°°°°°°°° £¨IV◊∞÷√÷–œ°¡ÚÀ·µƒ◊˜”√ «
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
¢€»ÙΩ´V◊∞÷√”ÎIII◊∞÷√÷–≥§µºπÐœ¬∂Àœý¡¨Ω”£¨”≈µ„ «°°°°°°°°°°°°°°°°°°°°°°°° °£
°° (3)C»Ð”⁄ÀƵƒπ˝≥Ã÷–∑¢…˙µƒ∑¥”¶Œ™(”√ªØ—ß”√”Ô±Ì æ)°°°°°°°°°°°° °£π§“µ…œ…˙≤˙Cµƒ∑¥”¶ «“ª∏ˆø…ƒÊ∑¥”¶£¨ µº …˙≤˙÷–£¨Œ™Ã·∏þ‘≠¡œµƒ¿˚”√¬ £¨ø…≤…»°µƒ¥Î © «
°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
26£Æ(16∑÷)X°¢Y°¢Z°¢WÀƒ÷÷‘™Àÿ‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û£¨X «µÿø«÷–∫¨¡ø◊Ó∂ýµƒΩ Ù‘™Àÿ£¨Y‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝ «¥ŒÕ‚≤„µÁ◊” ˝µƒ“ª∞Σ¨W‘™Àÿµƒ‘≠◊”–Ú ˝ «X‘™Àÿµƒ¡Ω±∂°£Zµ•÷ ø…∑¢…˙»Áœ¬∑¥”¶£∫Z+OH-=Z2-+ZO2-3+H2O(Œ¥≈‰∆Ω)£¨MŒ™Zµƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀƪ،԰£
°°°° «Îªÿ¥£∫
°° (1)X”ÎMµƒ≈®»Ð“∫∑¥”¶±ÿ–κ”»»£¨‘≠“Ú «°°°°°°°°°°°°°°°°°°°°°° °£
°° (2)πÿ”⁄Yµƒ”–πÿ– ˆ’˝»∑µƒ «(ÃÓ–Ú∫≈)°°°°°°°° °£
°°°°°°°° ¢ŸYµ•÷ «π‚µºœÀŒ¨µƒ÷˜“™‘≠¡œ
¢⁄Yµƒ∆¯Ã¨«‚ªØŒÔ±»¡ÚªØ«‚Œ»∂®
¢€Yµƒ◊Ó∏þº€—ıªØŒÔ–Œ≥…µƒæßÃÂŒ™‘≠◊”æßÃÂ
¢ÐYµƒ◊Ó∏þº€—ıªØŒÔø…“‘∫ÕÀÆ◊˜”√…˙≥…œý”¶µƒÀ·
°° (3)𧓵…˙≤˙µ•÷ Xµƒ‘≠¿Ì «(”√ªØ—ß∑Ω≥Ã Ω±Ì æ)°°°°°°°°°°°°°°°°°°°°°° °£
°°°°°°°° –¥≥ˆXµƒ◊Ó∏þº€—ıªØŒÔµƒÀƪ،ԔÎNaOH»Ð“∫∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω°°°°°°°°°°°° °£
°° (4)‘⁄…Ÿ¡øWµ•÷ ”ÎMµƒœ°»Ð“∫∑¥”¶∫Ûµƒ»Ð“∫÷–£¨º”»Î◊„¡øH2O2£¨∑¥”¶œ÷œÛŒ™
°°°°°°°° °°°°°°°°°°°°°°°°°°£¨–¥≥ˆ∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°° °£
°° (5)≥£Œ¬œ¬ƒ≥µ•÷ Œ™“∫裨96g∏√µ•÷ ƒÐ”Î28gWµ•÷ «°∫√ÕÍ»´∑¥”¶£¨Ω´À˘µ√≤˙ŒÔ»Ð”⁄ÀÆ≈‰≥…500mL»Ð“∫£¨«ÛÀ˘µ√»Ð“∫÷–Ω Ù¿Î◊”≈®∂»°°°°°° °°°°°°°°°°°£
25£Æ(16∑÷)ƒ≥”–ª˙ªØ∫œŒÔA“Ú∆‰æþ”–¬È◊Ì◊˜”√£¨≥£”√◊˜æ÷≤ø¬È◊̺¡∫Õ’ÚÕ¥º¡°£À¸µƒ∑÷◊” ΩŒ™C10H12O2£¨∆‰∑÷◊”ƒ£–Õ»Áœ¬ÕºÀ˘ æ(Õº÷–«Ú”ΫÚ÷ƺ‰µƒ¡¨œþ¥˙±ÌªØ—ߺ¸£¨»Áµ•º¸°¢À´º¸µ»)°£«Îªÿ¥£∫
°° (1)∏˘æðœ¬Õºƒ£–Õ–¥≥ˆ”–ª˙ŒÔAµƒΩ·ππºÚ Ω°°°°°°°° °£
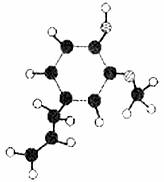
°° (2)1molA”Î◊„¡øµƒ≈®‰ÂÀÆ∑¥”¶◊Ó∂ýø…ƒÐœ˚∫ƒ°°°°°° molBr2°£”–ª˙ŒÔA≤ªƒÐ∑¢…˙µƒªØ—ß∑¥”¶”–(ÃÓ–Ú∫≈°°°°°° °£)
¢Ÿº”≥…∑¥”¶°°°° ¢⁄ı•ªØ∑¥”¶°°°° ¢€ÀÆΩ‚∑¥”¶°°°° ¢Ðœ˚»•∑¥”¶°°°°
¢ðº”æ€∑¥”¶°°°° ¢Þ—ıªØ∑¥”¶
°° (3)¬˙◊„œ¬¡–Ãıº˛µƒAµƒÕ¨∑÷“ÏππÔ–°°°°°°°° ÷÷£¨–¥≥ˆ∆‰÷–“ª÷÷µƒΩ·ππºÚ Ω°°°°°° °£
°°°°°°°° ¢ŸƒÐ”ÎNaHCO3»Ð“∫∑¥”¶£ª¢⁄±Ωª∑…œµƒ“ª¬»»°¥˙ŒÔ”–1÷÷°£
°° (4)“—÷™£∫
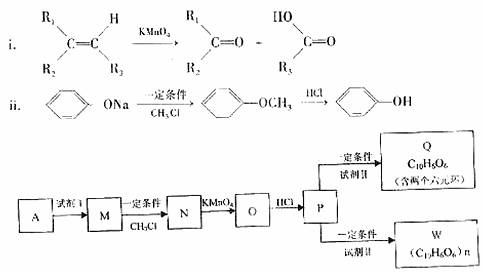
¢Ÿ ‘º¡I≤ªø…—°”√µƒ «(ÃÓ◊÷ƒ∏)°°°°°°°° £ª
a£ÆCH3COONa»Ð“∫°°°° b£ÆNaOH»Ð“∫°°°° c£ÆNaHCO3»Ð“∫°° d£ÆNa2CO3»Ð“∫
¢⁄…œ ˆ◊™ªØπ˝≥Ã÷–£¨≤Ω÷ËM°˙Nµƒƒøµƒ «°°°°°°°°°°°°°° £ª
¢€–¥≥ˆP…˙≥…QµƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°° £ª
¢Ð–¥≥ˆWµƒΩ·ππºÚ Ω°°°°°°°°°°°°°°°°°°°°°°°° °£
12£Æ64gÕ≠”Γª∂®≈®∂»µƒœıÀ·∑¥”¶£¨Õ≠ÕÍ»´»ÐΩ‚…˙≥…NO∫ÕNO2(≤ªøº¬«…˙≥…N2O4)ªÏ∫œ∆¯ÃÂ33.6 L(À˘”–∆¯ÃÂê˝æ˘‘⁄±Í◊º◊¥øˆœ¬≤‚µ√)°£œ¬¡–Àµ∑®’˝»∑µƒ «°°°°°°°° (°°°° )
°° °° A£ÆNOµƒÃª˝Œ™28L
|
°° °° C£ÆªÏ∫œ∆¯Ãµƒ∆Ωæ˘œý∂‘∑÷◊”÷ ¡ø‘ºŒ™43.3
°° °° D£Æ»Ù π…˙≥…µƒ∆¯ÃÂÕÍ»´±ªÀÆŒ¸ ’£¨–Ë“™22.4L O2
µ⁄¢ÚæÌ(∑«—°‘ÒÂπ≤180∑÷)
Àµ√˜£∫∑«—°‘ÒÂ≤ø∑÷«Î∞¥Ã‚ƒø“™«Û◊˜¥°£Ω‚¥Ã‚”¶–¥≥ˆ±ÿ“™µƒŒƒ◊÷Àµ√˜°¢∑Ω≥à Ω∫Õ÷ÿ“™À„≤Ω÷Ë£¨÷ª–¥≥ˆ◊Ó∫Û¥∞∏µƒ≤ªƒÐµ√∑÷°£”– ˝÷µº∆À„µƒÃ‚£¨¥∞∏÷–±ÿ–Î√˜»∑–¥≥ˆ ˝÷µ∫Õµ•Œª°£
11£Æ≥£Œ¬œ¬£¨πÿ”⁄œ¬¡–»Ð“∫µƒ– ˆ¥ÌŒÛµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£ÆCH3COOH∑÷◊”ø…“‘¥Ê‘⁄”⁄pH=8µƒºÓ–‘»Ð“∫÷–
°°°°°° B£Æ1mol£ØL∞±ÀÆ”Î0 5mol/L∞±ÀÆ÷–c(OH-)÷Ʊ» «2£∫l
°°°°°° C£Æº◊À·»Ð“∫∫Õ“ª∂®¡øNaOH»Ð“∫«°∫√ÕÍ»´∑¥”¶£¨»Ð“∫÷–c(HCOO-)<c(Na+)
°° D£Æµ»Ãª˝µ»pHµƒ¥◊À·∫Õ—ŒÀ·∑÷±º”ÀÆœ° Õ÷¡a mL∫Õb mL£¨œ° Õ∫ۻГ∫pHæ˘Œ™5‘Úa>b
10£ÆX°¢YŒ™∂Ã÷Ð∆⁄‘™Àÿ£¨Xµƒ‘≠◊”∞Îæ∂–°”⁄Y°£œ¬¡–– ˆ’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°° °° A£Æ‘≠◊”–Ú ˝Y¥Û”⁄X
°° °° B£ÆX‘™Àÿµƒ◊Ó∏þ’˝º€“ª∂®¥Û”⁄Y‘™Àÿµƒ◊Ó∏þ’˝º€
°°°°°° C£Æ»ÙX‘™Àÿ–Œ≥…µƒµ•÷ «X2£¨Y‘™Àÿµƒµ•÷ “ª∂® «Y2
°°°°°° D£Æ»ÙX°¢Y‘≠◊”µÁ◊”≤„ ˝œýÕ¨£¨Yµƒ ßµÁ◊”ƒÐ¡¶“ª∂®«ø”⁄X
9£Æœ¬¡–– ˆ’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°° A£ÆFe(OH)£¨≤ª»Ð”⁄ÀÆ≤ªƒÐÕ®π˝ªØ∫œ∑¥”¶÷±Ω”µ√µΩ
°° B£ÆH2O°¢H2SÀÊ◊≈œý∂‘∑÷◊”÷ ¡øµƒ‘ˆ¥Û£¨∑–µ„÷Ω•…˝∏þ
°° C£Æ÷ª∫¨“ª÷÷‘™ÀÿµƒŒÔ÷ ø…ƒÐŒ™ªÏ∫œŒÔ
°° D£ÆŒÔ÷ Bµƒ±•∫ջГ∫ΩµµÕŒ¬∂» ±“ª∂®”–BŒÔ÷ Œˆ≥ˆ
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com