
27.(15分)已知物质M由X、Y两种短周期且同周期元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6。M与其他物质的转化关系如下(部分产物已略去):
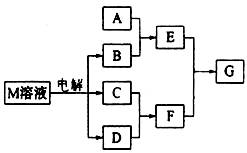
(1)已知元素Z与Y是最外层电子数相同的短周期元素,那么Z与Y分别与氢形成的氢化物中沸点较高的是 (填化学式),原因是 ;
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则E溶液与F反应的离子方程式是 ;
(3)若A是与X、Y同周期元素的一种常见金属单质,且A与B溶液能够反应,则其化学方程式是 ;
(4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则G的电子式是 ;
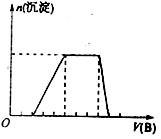
(5)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32-、、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子是 。
26.(13分)氧化还原反应实际包含氧化和还原两个过程,下面是一个还原过程的反应式:
NO3-+4H++3e-=NO↑+2H2O
KMnO4、NaHCO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述的还原过程发生。
(1)写出并配平该氧化还原反应的化学方程式 ;
(2)反应中硝酸体现了 、 的性质;
(3)若反应中产生标准状况下11.2L气体,则转移电子的物质的量是 ;
(4)现称取含有杂质的甲样品(杂质与硝酸不反应)5.4g,恰好与100mL、1.4mol/L的硝酸溶液完全反应,则该样品的纯度为 ;
(5)若1mol甲与某浓度硝酸反应时,被还原的硝酸的物质的量增加,原因是 。
13.已知柠檬醛的结构简式为:
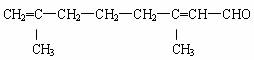
根据你所学的知识判断下列说法不正确的是 ( )
A.它可被催化加氢,最后产物的化学式为C10H20O
B.它可使酸性KMnO4溶液褪色
C.它可使溴水褪色
D.它可与银氨溶液反应
第Ⅱ卷(共10题,共174分)
12.在一密闭容器中,反应:aA(g) bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度是原来的40%则: ( )
bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度是原来的40%则: ( )
A.平衡向逆反应方向移动了 B.物质A的转化率减少了
C.物质B的质量分数增加了 D.a>b
11.如图某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用硫酸钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔知滤纸上写“嫦娥奔月”,会出现红色字迹,据此下列叙述正确的是 ( )
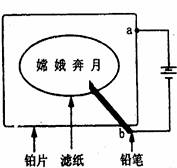
A.铅笔端作阴极,铂片端发生还原反应
B.铅笔端有少量钠生成
C.硫酸钠溶液不可用硝酸钾溶液代替
D.铂片端发生的电极反应为:40H--4e-=2H2O+O2↑
10.下列溶液中有关微粒的物质的量浓度关系正确的是 ( )
A.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合液中
c(Na+)>c(Cl-)>c(CH3COOH)
B.相同条件下等物质的量浓度的(1)NaCl 溶液中;(2)NaOH溶液中;(3)HCl溶液中由水电离出的c(H+):(3)>(1)>(2)
C.PH相等的(1)NH4Cl;(2)(NH4)2SO4;(3)NH4HSO4三种溶液中,c(NH4+)的大小顺序为:(1)=(2)>(3)
D.0.1mol/L醋酸钡溶液中:c(Ba2+)>c(CH3COO-)>c(OH-)>c(H+)
9.下列提纯物质的方法中正确的是 ( )
A.除去KCl中的K2CO3,加入过量的BaCl2溶液后过滤
B.除去苯中的苯酚,加入足量的溴水后过滤
C.除去乙酸中混有的乙醇,加入生石灰后蒸馏
D.除去蛋白质溶液中少量的氯化钠,将装有混合物的半透膜放入流水中渗析
8.下列说法正确的是 ( )
A.原子晶体中只存在非极性共价键
B.稀有气体形成的晶体一定属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.含有金属阳离子的晶体一定是离子晶体
7.下列离子方程式书写正确的是 ( )
A.酸性条件下KIO3溶液和KI溶液反应生成I2:IO3-+5I-+3H2O=3I2+6OH-
B.AgNO3溶液中加入足量氨水:Ag++NH3·H2O= AgOH↓+NH4+
C.等物质的量浓度,等体积的氢氧化钡溶液与明矾溶液混合:
3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓
D.将少量SO2通入到澄清石灰水中:SO2+Ca(OH)2=Ca2++SO32-+H2O
6.设NA为阿伏加德罗常数,下列说法正确的是 ( )
A.2L 1mol/L NaF溶液中含Na+和F-均为2NA
B.在常温常压下,22gCO2含有的共用电子数均为2NA
C.0.1mol OH-的质子数与0.1mol H2O的电子数均为NA
D.在标准状况下,5.6辛烷中碳原子数为2NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com